Водородный генератор своими руками – схема, конструкция установки, чертежи
Удорожание энергоносителей стимулирует поиск более эффективных и дешевых видов топлива, в том числе на бытовом уровне. Более всего умельцев–энтузиастов привлекает водород, чья теплотворная способность втрое превышает показатели метана (38.8 кВт против 13.8 с 1 кг вещества). Способ добычи в домашних условиях, казалось бы, известен – расщепление воды путем электролиза. В действительности проблема гораздо сложнее. Наша статья преследует 2 цели:
- разобрать вопрос, как сделать водородный генератор с минимальными затратами;
- рассмотреть возможность применения генератора водорода для отопления частного дома, заправки авто и в качестве сварочного аппарата.
Краткая теоретическая часть
Водород, он же hydrogen, – первый элемент таблицы Менделеева – представляет собой легчайшее газообразное вещество, обладающее высокой химической активностью. При окислении (то бишь, горении) выделяет огромное количество теплоты, образуя обычную воду. Охарактеризуем свойства элемента, оформив их в виде тезисов:
Охарактеризуем свойства элемента, оформив их в виде тезисов:
- Горение водорода – процесс экологически чистый, никаких вредных веществ не выделяется.
- Благодаря химической активности газ в свободном виде на Земле не встречается. Зато в составе воды его запасы неиссякаемы.
- Элемент добывается в промышленном производстве химическим способом, например, в процессе газификации (пиролиза) каменного угля. Зачастую является побочным продуктом.
- Другой способ получения газообразного водорода – электролиз воды в присутствии катализаторов – платины и прочих дорогих сплавов.
- Простая смесь газов hydrogen + oxygen (кислород) взрывается от малейшей искры, моментально высвобождая большое количество энергии.
Раньше водородом наполняли баллоны дирижаблей, которые нередко взрывалисьДля справки. Ученые, впервые разделившие молекулу воды на hydrogen и oxygen, назвали смесь гремучим газом из-за склонности к взрыву. Впоследствии она получила название газа Брауна (по фамилии изобретателя) и стала обозначаться гипотетической формулой ННО.
Из вышесказанного напрашивается следующий вывод: 2 атома водорода легко соединяются с 1 атомом кислорода, а вот расстаются весьма неохотно. Химическая реакция окисления протекает с прямым выделением тепловой энергии в соответствии с формулой:
2H2 + O2 → 2H2O + Q (энергия)
Здесь кроется важный момент, который пригодится нам в дальнейшем разборе полетов: hydrogen вступает в реакцию самопроизвольно от возгорания, а теплота выделяется напрямую. Чтобы разделить молекулу воды, энергию придется затратить:
2H2O → 2H2 + O2 — Q
Это формула электролитической реакции, характеризующая процесс расщепления воды путем подведения электричества. Как это реализовать на практике и сделать генератор водорода своими руками, рассмотрим далее.
Создание опытного образца
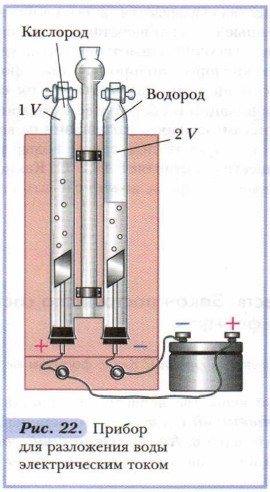
Чтобы вы поняли, с чем имеете дело, для начала предлагаем собрать простейший генератор по производству водорода с минимальными затратами. Конструкция самодельной установки изображена на схеме.
Конструкция самодельной установки изображена на схеме.
Из чего состоит примитивный электролизер:
- реактор – стеклянная либо пластиковая емкость с толстыми стенками;
- металлические электроды, погружаемые в реактор с водой и подключенные к источнику электропитания;
- второй резервуар играет роль водяного затвора;
- трубки для отвода газа HHO.
Важный момент. Электролитическая водородная установка работает только от постоянного тока. Поэтому в качестве источника питания применяйте сетевой адаптер, автомобильное зарядное устройство или аккумулятор. Электрогенератор переменного тока не подойдет.
Принцип работы электролизера следующий:
- К двум электродам, погруженным в воду, подводится напряжение, желательно от регулируемого источника. Для улучшения реакции в емкость добавляется немного щелочи либо кислоты (в домашних условиях – обычной соли).
- В результате реакции электролиза со стороны катода, подключенного к «минусовой» клемме, станет выделяться водород, а возле анода – кислород.

- Смешиваясь, оба газа по трубке поступают в гидрозатвор, выполняющий 2 функции: отделение водяного пара и недопущение вспышки в реакторе.
- Из второй емкости гремучий газ ННО подается на горелку, где сжигается с образованием воды.
Чтобы своими руками сделать показанную на схеме конструкцию генератора, потребуется 2 стеклянных бутылки с широкими горлышками и крышками, медицинская капельница и 2 десятка саморезов. Полный набор материалов продемонстрирован на фото.
Из специальных инструментов потребуется клеевой пистолет для герметизации пластиковых крышек. Порядок изготовления простой:
- Плоские деревянные палочки скрутите саморезами, располагая их концами в разные стороны. Спаяйте головки шурупов между собой и подсоедините провода – получите будущие электроды.
- Проделайте отверстие в крышке, просуньте туда разрезанный корпус капельницы и провода, затем герметизируйте с 2 сторон клеевым пистолетом.
- Поместите электроды в бутылку и завинтите крышку.

- Во второй крышке просверлите 2 отверстия, вставьте трубки капельниц и накрутите на бутылку, заполненную обычной водой.
Для запуска генератора водорода налейте в реактор подсоленную воду и включите источник питания. Начало реакции ознаменуется появлением пузырьков газа в обеих емкостях. Отрегулируйте напряжение до оптимального значения и подожгите газ Брауна, выходящий из иглы капельницы.
Второй важный момент. Слишком высокое напряжение подавать нельзя — электролит, нагревшийся до 65 °С и более, начнет интенсивно испаряться. Из-за большого количества водяного пара разжечь горелку не удастся. Подробности сборки и запуска импровизированного водородного генератора смотрите на видео:
О водородной ячейке Мейера
Если вы сделали и испытали вышеописанную конструкцию, то по горению пламени на конце иглы наверняка заметили, что производительность установки чрезвычайно низкая. Чтобы получить больше гремучего газа, нужно изготовить более серьезное устройство, называемое ячейкой Стэнли Мейера в честь изобретателя.
Принцип действия ячейки тоже основан на электролизе, только анод и катод выполнены в виде трубок, вставляющихся одна в другую. Напряжение подается от генератора импульсов через две резонансные катушки, что позволяет снизить потребляемый ток и увеличить производительность водородного генератора. Электронная схема устройства представлена на рисунке:
Примечание. Подробно о работе схемы рассказывается на ресурсе http://www.meanders.ru/meiers8.shtml.
Для изготовления ячейки Мейера потребуется:
- цилиндрический корпус из пластмассы или оргстекла, умельцы нередко используют водопроводный фильтр с крышкой и патрубками;
- трубки из нержавеющей стали диаметром 15 и 20 мм длиной 97 мм;
- провода, изоляторы.
Нержавеющие трубки крепятся к основанию из диэлектрика, к ним припаиваются провода, подключаемые к генератору.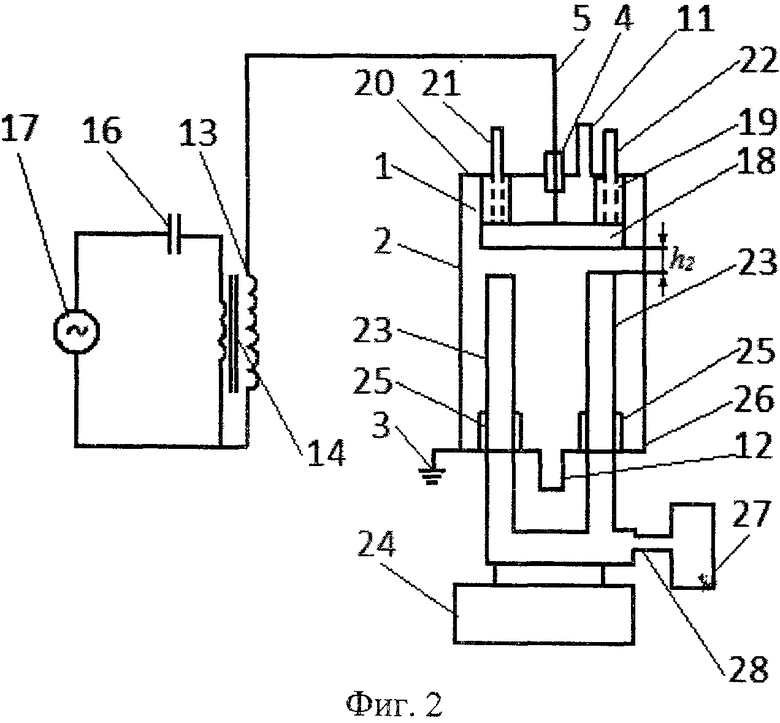 Ячейка состоит из 9 или 11 трубок, помещенных в пластиковый либо плексигласовый корпус, как показано на фото.
Ячейка состоит из 9 или 11 трубок, помещенных в пластиковый либо плексигласовый корпус, как показано на фото.
Соединение элементов производится по всем известной в интернете схеме, куда входит электронный блок, ячейка Мейера и гидрозатвор (техническое название – бабблер). В целях безопасности система снабжена датчиками критического давления и уровня воды. По отзывам домашних умельцев, подобная водородная установка потребляет ток порядка 1 ампера при напряжении 12 В и обладает достаточной производительностью, хотя точные цифры отсутствуют.
Принципиальная схема включения электролизераРеактор из пластин
Высокопроизводительный генератор водорода, способный обеспечить работу газовой горелки, выполняется из нержавеющих пластин размером 15 х 10 см, количество – от 30 до 70 шт. В них просверливаются отверстия под стягивающие шпильки, а в углу выпиливается клемма для присоединения провода.
Кроме листовой нержавейки марки 316 понадобится купить:
- резина толщиной 4 мм, стойкая к воздействию щелочи;
- концевые пластины из оргстекла либо текстолита;
- шпильки стяжные М10—14;
- обратный клапан для газосварочного аппарата;
- фильтр водяной под гидрозатвор;
- трубы соединительные из гофрированной нержавейки;
- гидроокись калия в виде порошка.
Пластины нужно собрать в единый блок, изолировав друг от друга резиновыми прокладками с вырезанной серединой, как показано на чертеже. Получившийся реактор плотно стянуть шпильками и подключить к патрубкам с электролитом. Последний поступает из отдельной емкости, снабженной крышкой и запорной арматурой.
Схема водородной установки мокрого типаПримечание. Мы рассказываем, как сделать электролизер проточного (сухого) типа. Реактор с погружными пластинами изготовить проще – резиновые прокладки ставить не нужно, а собранный блок опускается в герметичную емкость с электролитом.
Последующая сборка генератора, производящего водород, выполняется по той же схеме, но с отличиями:
- На корпусе аппарата крепится резервуар для приготовления электролита.
 Последний представляет собой 7—15% раствор гидроокиси калия в воде.
Последний представляет собой 7—15% раствор гидроокиси калия в воде. - В «бабблер» вместо воды заливается так называемый раскислитель – ацетон либо неорганический растворитель.
- Перед горелкой обязательно ставится обратный клапан, иначе при плавном выключении водородной горелки обратный удар разорвет шланги и «бабблер».
Для питания реактора проще всего задействовать сварочный инвертор, электронные схемы собирать не нужно. Как устроен самодельный генератор газа Брауна, расскажет домашний мастер в своем видео:
Выгодно ли получать водород в домашних условиях
Ответ на данный вопрос зависит от сферы применения кислородно-водородной смеси. Все чертежи и схемы, публикуемые различными интернет-ресурсами, рассчитаны на выделение газа HHO для следующих целей:
- использовать hydrogen в качестве топлива для автомобилей;
- бездымно сжигать водород в отопительных котлах и печах;
- применять для газосварочных работ.

Главная проблема, перечеркивающая все преимущества водородного топлива: затраты электричества на выделение чистого вещества превышают количество энергии, получаемое от его сжигания. Что бы ни утверждали приверженцы утопичных теорий, максимальный КПД электролизера достигает 50%. Это значит, что на 1 кВт полученной теплоты затрачивается 2 кВт электроэнергии. Выгода – нулевая, даже отрицательная.
Вспомним, что мы писали в первом разделе. Hydrogen – весьма активный элемент и реагирует с кислородом самостоятельно, выделяя уйму тепла. Пытаясь разделить устойчивую молекулу воды, мы не можем подвести энергию непосредственно к атомам. Расщепление производится за счет электричества, половина которого рассеивается на подогрев электродов, воды, обмоток трансформаторов и так далее.Важная справочная информация. Удельная теплота сгорания водорода втрое выше, чем у метана, но – по массе. Если сравнивать их по объему, то при сжигании 1 м³ гидрогена выделится всего 3.6 кВт тепловой энергии против 11 кВт у метана.
Ведь водород – легчайший химический элемент.
Теперь рассмотрим гремучий газ, полученный электролизом в самодельном водородном генераторе, как топливо для вышеперечисленных нужд:
- Конечная цена установки, низкая производительность и КПД делает крайне невыгодным сжигание водорода для отопления частного дома. Чем «наматывать» счетчик электролизером, проще поставить любой из электрокотлов – ТЭНовый, индукционный либо электродный.
- Чтобы заменить 1 л бензина для автомобиля, потребуется 4766 литров чистого водорода или 7150 л гремучего газа, треть которого составляет кислород. Самый завравшийся изобретатель в интернете еще не сделал электролизер, способный обеспечить подобную производительность.
- Газосварочный аппарат, сжигающий hydrogen, компактнее и легче баллонов с ацетиленом, пропаном и кислородом. Плюс температура пламени до 3000 °С позволяет работать с любыми металлами, стоимость получения горючего здесь особой роли не играет.
Для справки.
Чтобы сжигать гидроген в отопительном котле, придется основательно переработать конструкцию, поскольку водородная горелка способна расплавить любую сталь.
Заключение
Гидроген в составе газа ННО, полученный из самодельного водородного генератора, пригодится для двух целей: экспериментов и газосварки. Даже если отбросить низкий КПД электролизера и затраты на его сборку вместе с потребляемым электричеством, на обогрев здания попросту не хватит производительности. Это касается и бензинового двигателя легковой машины.
Энергия водорода и её производство различными способами
Со школьных уроков химии и физики известно, что энергия водорода сосредоточенная в этом газе довольно значительна. Искры достаточно, чтобы воспламенить смесь нормального воздуха и водорода полученного в результате опыта на школьных уроках.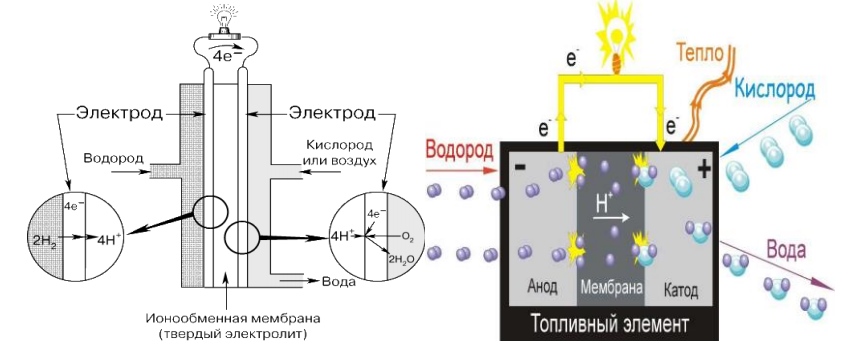
В отличие от многих других процессов горения, продукт реакции абсолютно безвреден с экологической точки зрения, поэтому люди изучают промышленное производство и энергию водорода.
Так как человечеству необходимы все больше энергии чистая водородная энергия пришлась бы кстати.
Топливные элементы могут генерировать столь востребованную электроэнергию из этого газа. Неудивительно, что многие люди с видением глобальной водородной экономики видят в этом решение наших текущих климатических проблем.
Энергия водорода может в то же время помочь нам избавиться от загрязнения воздуха, кислотных дождей и других экологических проблем, вызванных другими источниками.
Жюль Верн увидел потенциал энергии водорода еще в 1874 году в романе «Таинственный остров», и вопрос в том, почему процветающая водородная промышленность еще не развилась.
Ответ прост: этот газ не встречается в природе в чистом виде и нужно преобразование энергии. Энергетика и комплекс технических процессов необходим прежде чем его можно выделить и использовать как водородную энергию.
Энергетика и комплекс технических процессов необходим прежде чем его можно выделить и использовать как водородную энергию.
Но даже если водородная промышленность еще только на чертежной доске, вторичная энергия водорода все еще интересна как альтернативный источник для некоторых областей применения.
Что представляет первый элемент периодической системы
Водород является наиболее распространенным компонентом в нашей Солнечной системе и имеет около 75% массы и более 90% всех атомов. Наше Солнце и большие газовые планеты Юпитер, Сатурн, Уран и Нептун состоят в основном из этого газа. На Земле этот газ встречается гораздо реже. Его доля в общем весе Земли составляет только около 0,12%. Хотя водород чаще встречается в земной коре, его практически нет в чистом виде. Он почти всегда химически связан и наиболее частым соединением является вода.
Водород – самый маленький и легкий атом. Как чрезвычайно легкий газ, он был использован для наполнения газовых баллонов дирижаблей жесткой формы как Цеппелины, в течение первой половины девятнадцатого века. Катастрофа в Гинденбурге в США в 1937 году, где предположительно произошел электростатический заряд который вызвал возгорание, положил трагический конец перспективам использования водорода в дирижаблях.
Основное применение водорода сегодня находится в химической промышленности. В качестве источника энергия водорода в настоящее время широко используется, в основном, в авиационном и космическом секторе.
Водород как источник энергии используется для привода реактивных двигателей самолетов.
В космических полетах жидкий водород используется в качестве ракетного топлива. Например, запуск космического челнока потребляет около 1,4 млн литров жидкого водорода весом более 100 тонн создавая температуру горения до 3200° C.
Производство
Водородная энергетика использует несколько способов производства водорода.
Газ сначала должен быть получен в чистом виде, прежде чем энергия из него может быть получена. Это требует легкодоступного недорогого сырья, содержащего этот химический элемент. Кроме воды (H2O), которая состоит из водорода (H) и кислорода (O) могут быть применены смеси углерода. Это в первую очередь природный газ или метан (CH4). Мазут и уголь также состоят из водорода (H) и углерода (C), но имеют гораздо более высокую долю углерода, чем природный газ.
Из углеводородов
Современные промышленные методы получения водорода почти исключительно используют ископаемые топливо, как природный газ, сырую нефть или уголь, как сырье. Такие методы, как паровой риформинг или частичное окисление паром для получения водорода из ископаемых углеводородов. Этот процесс химически отделяет углерод который после этого превращается в окись углерода (CO). Эти методы добычи водорода не являются идеальным вариантом с целью активной защиты климата.
В основном, упомянутый способ производства водорода из ископаемых источников работает при высоких температурах обработки.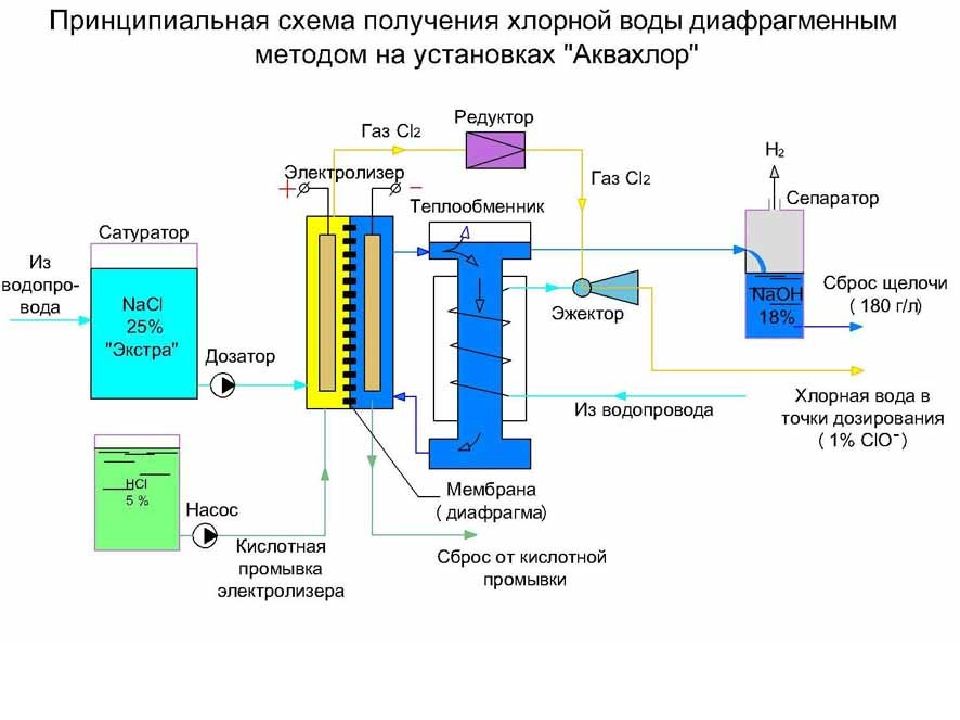 Это требует большого количества внешних ресурсов.
Это требует большого количества внешних ресурсов.
Поэтому для получения водорода необходимы другие методы, с тем чтобы он был экологически чистым и безопасным. Идеальным способом является электролиз.
Методом электролиза
Немецкий химик Иоганн Вильгельм Риттер впервые использовал электролиз для получения водорода еще в 1800 году. С помощью электрической энергии, электролиз разлагает воду на водород и кислород.
Особенностью электролиза может быть то, что если электроэнергия добыта из возобновляемых источников, то производство водорода во всем цикле может выделять только углекислый газ.
С помощью этого метода два электрода погружают в проводящий водный электролит. Это может быть смесь воды и серная кислота или гидроксид калия (KOH). Аноды и катоды проводят постоянный ток в электролитах и на них образуются газы водород и кислород. Хотя электролиз уже достиг высокого уровня технического развития, как экологически совместимый вариант производства кислорода, другие альтернативные методы также разрабатываются.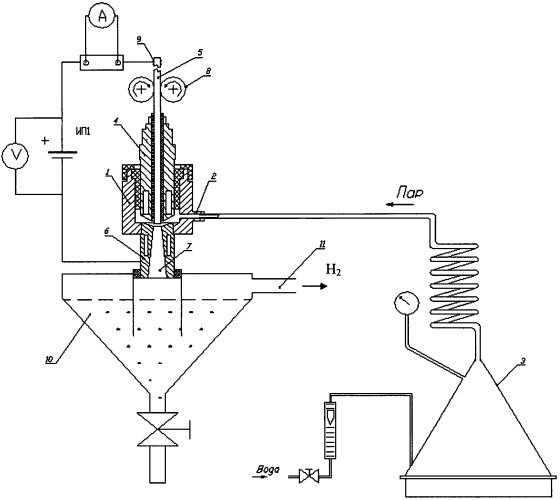
Термохимический метод
При температуре выше 1700° C вода непосредственно разлагается на водород и кислород. Однако эти температуры требуют дорогостоящих термостойких средств. Необходимую температуру можно уменьшить ниже чем 1000° С через различные сопряженные химические реакции.
Биологическое получение
Другие методы включают фотобиологическое производство водорода. Суть этого метода в том, что некоторые водоросли во время роста при нехватке серы производят водород. Это типа биореакторов использующих свет для разложения воды.
Хранение и транспортировка
После получения водорода он должен храниться и транспортироваться потребителю. В принципе, мы знакомы с хранением и транспортировкой горючих газов.
Водород – очень легкий газ с очень минимальной плотностью, но имеет относительно высокое значение энергоемкости. При сравнении с природным газом он требует гораздо больших объемов хранения, хотя накопленный водород намного легче.
Произведенный водород можно сохранить под высоким давлением и сжать для того чтобы уменьшить необходимые объемы хранения.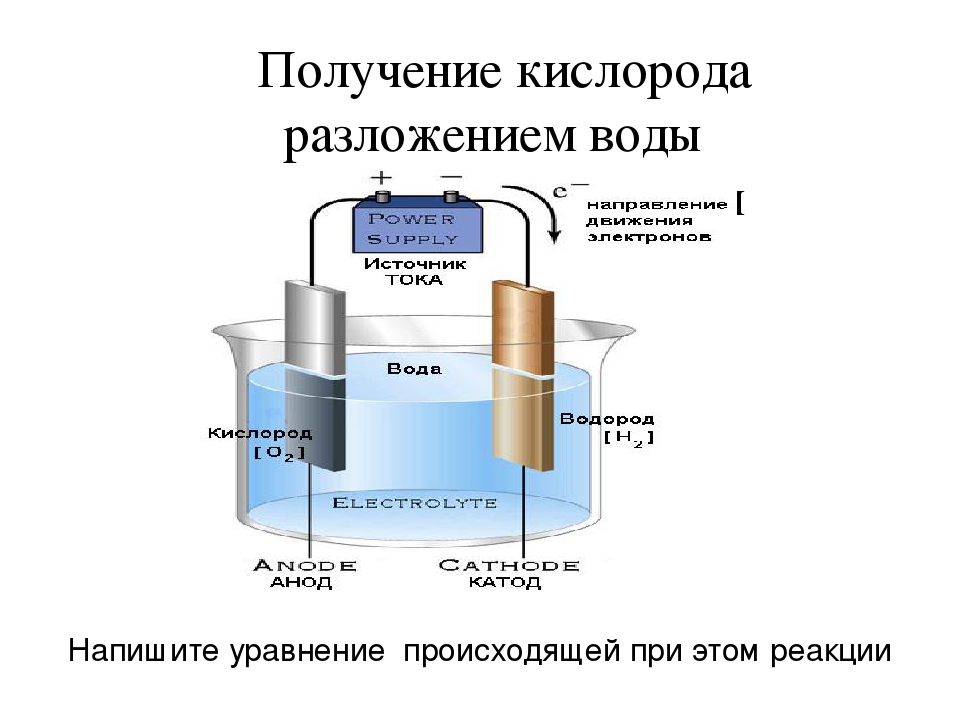
Для достижения таких низких температур требуется определенное количество энергии. От 20 до 40% энергии, хранящейся в водороде, используется для его сжижения.
В принципе, те же технологии, которые используются в секторе природного газа могут быть использованы для сжижения, транспортировки и хранения. Этот первый элемент периодической системы можно транспортировать либо в трубопроводах, либо на специальных танкерах и грузовых судах. В то время как трубопроводы, как правило, транспортируют газообразную форму, танкеры предпочтительны для жидкого водорода. В отличие от водорода, природный газ уже становится жидким при минус 162 ° C. Опыт работы в газовой отрасли может быть использован для хранения и транспортировки водородной энергии.
Будущее применение
Топливные элементы считаются ключом как будет использоваться энергия водорода в будущем, поскольку они могут преобразовывать его непосредственно в электрическую энергию. Теоретически это приводит к более высокой эффективности, чем при сжигании в обычных тепловых электростанциях.
Теоретически это приводит к более высокой эффективности, чем при сжигании в обычных тепловых электростанциях.
Принцип работы топливных элементов известен уже очень давно.
Есть некоторые споры о том, кто на самом деле изобрел топливный элемент:
- Немецко-швейцарский химик Кристиан Фридрих провел первые тесты в технологии топливных элементов в 1838 году.
- Английский физик сэр Уильям Роберт Гроув построил первый топливный элемент в 1839 году.
- Впоследствии такие известные ученые, как Анри Беккерель и Томас Эдисон, стали участвовать в их дальнейшем развитии. Однако это была довольно слабо продвинутая стадия развития.
- Наконец, в середине двадцатого века была достигнута задача, позволившая применение и основное использование топливных элементов.
Топливные элементы, в основном, предполагают реверсирование электролиза. Топливный элемент всегда содержит два электрода. В зависимости от типа топливного элемента, чистый водород (H2) или топливо содержащее углеводороды подают через анод и чистый кислород (О2 ) или воздух в качестве окислительного материала через катод. Электролит отделяет анод и катод. Электроны текут по большой цепи и создают электрическую энергию.
Электролит отделяет анод и катод. Электроны текут по большой цепи и создают электрическую энергию.
С 1990-х годов разработка топливных элементов идет полным ходом. Автомобильные производители и энергокомпании приняли технологию и ищут способ получить прибыль от положительного применения водорода как источника энергии.
Установка производства водорода, назначение, технология, схема
Назначение
Установка производства водорода предназначена для обеспечения техническим водородом вновь вводимых установок:
- изомеризации,
- гидроочистки,
- гидрокрекинга,
- каталитического риформинга.
Строительство установки производства водорода позволит:
- ликвидировать недостающую потребность в водороде на НПЗ
- производить водород высокой чистоты (не менее 99,5 % об.), что сокращает объём газа в последующих схемах потребления водорода;
- улучшить экологические условия на территории предприятия за счёт применения в качестве топлива обессеренного газа с блока КЦА.
Методы производства водорода
- паровая конверсия метана и природного газа;
- газификация угля;
- электролиз воды;
- пиролиз;
- частичное окисление;
- биотехнологии.
Сырье и продукты
На российских НПЗ наиболее распространенным методом получения водорода является паровая конверсия углеводородов (СУГ, нафты, природного газа).
Продуктами являются чистый водород с концентрацией >99% об., а также отдувочный газ, который чаще всего используется в качестве топлива для печей.
Катализаторы
Наиболее часто используемыми в промышленности катализаторами для процесса паровой конверсии являются катализаторы на основе никеля, однако в ряде специфических процессов допускается использование благородных металлов платиновой группы.
Технологическая схема
В состав установки производства водорода входят следующие блоки и узлы:
- блок подготовки и очистки сырья;
- блок предриформинга;
- блок парового риформинга;
- блок конверсии и охлаждения конвертированного газа;
- блок очистки водородсодержащего газа по технологии КЦА;
- блок утилизации тепла продуктовых потоков и дымовых газов.

Очистка сырья
Природный газ поступает в подогреватель, нагревается до температуры 40 °С. Для гидрирования сернистых соединений, содержащихся в сырье, до сероводорода, требуется небольшое количество водорода.
С этой целью часть водорода, полученного на установке, подается в качестве рециркуляционного водорода в поток сырья. Смесь сырья и рециркулирующего водорода, последовательно поступая в теплообменники, нагревается до температуры 380 °С, необходимой для предварительной очистки сырья.
Подогретая газосырьевая смесь поступает в реактор гидрообессеривания, где происходит гидрирование соединений серы до H2S. Газосырьевая смесь из реактора последовательно проходит через адсорберы, где происходит улавливание хлоридов (НСl) и сернистых соединений (H2S). В каждом из этих реакторов имеется три слоя катализатора:
В каждом из этих реакторов имеется три слоя катализатора:
- модифицированный оксид алюминия для удаления НСl,
- оксид цинка,
- слой специального катализатора для эффективного и глубокого удаления H2S.
Предриформинг
Очищенная газосырьевая смесь смешивается с перегретым паром высокого давления. Соотношение расходов регулируется с поддержанием заданного мольного соотношения водяного пара и углерода. Величина значения этого соотношения зависит от типа сырья, подаваемого на установку.
Далее парогазовая смесь нагревается до температуры реакции 475 °С – 500 °С, в змеевике подогрева сырья предриформинга, расположенном в конвекционной секции печи парового риформинга и направляется в реактор предриформинга.
Предриформинг служит для превращения тяжелых углеводородов, содержащихся в сырье, в метан, а также для частичного проведения реакций риформинга, при этом эффективность процесса повышается.
В зависимости от типа перерабатываемого сырья, может наблюдаться увеличение или снижение общей температуры по реактору. Так при переработке бензинов увеличивается общая температура по реактору, за счет преобладания протекания реакций с экзотермическим эффектом, а при переработке природного газа температура по реактору падает, за счет протекания реакций с эндотермическим эффектом.
Так при переработке бензинов увеличивается общая температура по реактору, за счет преобладания протекания реакций с экзотермическим эффектом, а при переработке природного газа температура по реактору падает, за счет протекания реакций с эндотермическим эффектом.
Риформинг
Парогазовая смесь нагревается до температуры 650 °С в змеевике подогрева сырья риформинга, расположенном в конвекционной секции печи парового риформинга, и затем поступает в коллектор, расположенный в радиантной секции печи парового риформинга.
В радиантной секции печи парового риформинга смесь сырья и пара поступает в катализаторные трубы, находящиеся в радиантной секции печи парового риформинга Н-1, проходит сверху вниз катализаторные трубы. В результате реакции, протекающей на катализаторе, загруженном в катализаторные трубы, получается равновесная смесь, состоящая из Н2, СО, СO2, СН4 и Н2O.
Для предотвращения образования кокса и отложения его на катализаторе технологический пар подается в избытке, превышая стехиометрическое количество, требуемого на реакцию.
Полученный конвертированный газ (парогазопродуктовая смесь) выходит из печи парового риформинга при температуре 888 °С и далее направляется в теплообменник. В теплообменнике происходит охлаждение питательной воды до температуры 320-343 °С, регенерированное тепло используется для генерирования насыщенного пара высокого давления.
Общий тепловой эффект реакций парового риформинга является в сильной степени эндотермическим, поэтому для достижения требуемой степени конверсии необходим подвод тепла.
Конструкция печи парового риформинга
Печь парового риформингаПечь имеет сложную конструкцию, разработанную с учетом технологических требований процесса с целью обеспечения безопасной эксплуатации и хорошими технико-экономическими показателями. Для обеспечения расчетной степени конверсии без перегрева внешней поверхности поддерживается необходимая температура газа в катализаторных трубах. Благодаря небольшому диаметру труб увеличивается площадь теплообменной поверхности и улучшается перемешивание газа в слое катализатора. В результате печи риформинга работают при максимальных давлениях и температурах.
По конструкции печь состоит из двух одинаковых радиантных камер, работающих параллельно, и расположенной над ними общей конвекционной камеры. Процесс паровой конверсии метана осуществляется в реакционных трубах при температуре 780-888 °С за счет внешнего обогрева.
Конверсия окиси углерода и охлаждение синтез-газа
Водородсодержащий газ после парового риформинга и охлаждения поступает в реактор высокотемпературной конверсии, где избыточный пар превращает большую часть СО в С02 и Н2 при прохождении через слой катализатора.
Синтез-газ, подвергнутый конверсии, охлаждается, отдавая тепло потокам системы выработки водяного пара. Далее частично охлажденный синтез-газ поступает в воздушный, а затем на доохлаждение в водяной холодильник, где охлаждается до температуры 35 °С и поступает в сепаратор для разделения смеси на неочищенный водород и технологический конденсат.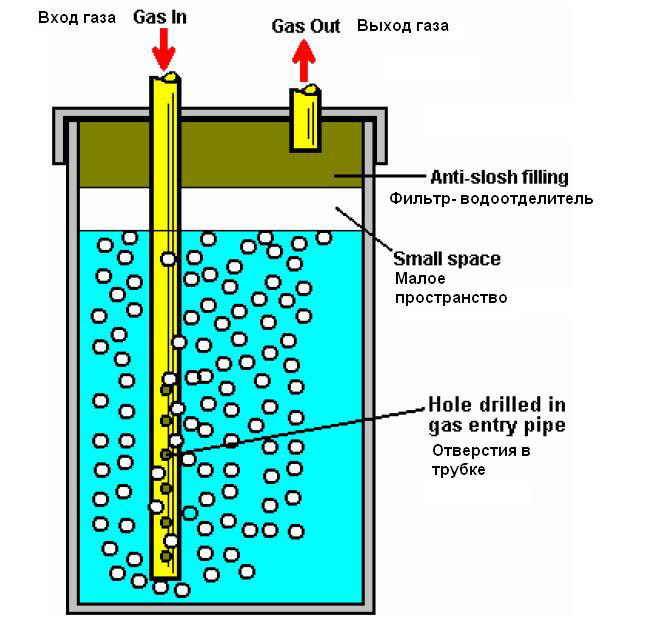
Технологический конденсат смешивается с химочищенной водой, поступающей из сетей завода и направляется в деаэратор, а неочищенный водород подается в блок короткоцикловой адсорбции.
Короткоцикловая адсорбция водородсодержащего газа
Поток неочищенного водородсодержащего газа поступает в блок короткоцикловой адсорбции (КЦА), где происходит удаление примесей в процессе циклической адсорбции. Для выполнения заданной степени концентрирования водорода и удаления примесей в процессе используются многочисленные адсорбционные слои. Принятая схема блока позволяет извлечь водород с концентрацией 99,5 % (об.) из конвертированного газа, а сбросной газ направляется в качестве топлива в реакторную печь.
Блок короткоцикловой адсорбции (КЦА)В блоке КЦА происходит очистка конвертированного водородсодержащего газа от примесей метана, окислов углерода путем адсорбции загрязнений на адсорбенте при высоком давлении и десорбции при низком давлении.
Блок утилизации тепла дымовых газов
В блоке утилизации тепла дымовых газов и продуктовых потоков производится водяной пар высокого давления за счет охлаждения дымовых газов и продуктовых потоков. Одновременно с этим предусмотрено использование тепла дымовых газов для нагрева питательной воды, перегрева производимого водяного пара и подогрева воздуха, подаваемого к горелкам печи.
Одновременно с этим предусмотрено использование тепла дымовых газов для нагрева питательной воды, перегрева производимого водяного пара и подогрева воздуха, подаваемого к горелкам печи.
Материальный баланс
| Наименование продукта | Измерение | Сутки | |
| един. | итого | % | |
| Входы | |||
| Сырьевой газ | т | 276,00 | 22,30 |
| Расход пара ВД в предриформинг | т | 633,60 | 51,20 |
| Расход пара ВД в риформинг | т | 327,90 | 26,50 |
| Сумма сырья | т | 1 237,50 | 100,00 |
| Выходы | |||
| Водород с установки | т | 89,70 | |
| Расход отдувочного газа с блока КЦА на печь | т | 605,10 | |
| Расход технологического конденсата | т | 542,70 | |
| Сумма продуктов | т | 1 237,50 | |
Достоинства и недостатки
Недостатки
- Высокие выбросы дымовых газов в атмосферу
- Высокие капитальные затраты
- Высокая стоимость перегретого водяного пара
Достоинства
- Наиболее проработанный и распространенный вид производства водорода в нефтехимической промышленности
- Относительно низкие температуры процесса
- Вариативность проекта установки в зависимости от требований заказчика
Существующие установки
Спрос на водород растет в связи с переходом на потребление более чистых и легких нефтяных топлив, в то время как нефтяное сырье становится все тяжелее. В связи с этим трудно представить современный НПЗ без установки производства водорода. УПВ может отсутствовать только в составе НПЗ, работающих по профилю первичной переработки нефти. Стоит отметить, что для производств, обладающих развитой архитектурой вторичных процессов, ресурсов одной УПВ может быть недостаточно.
В связи с этим трудно представить современный НПЗ без установки производства водорода. УПВ может отсутствовать только в составе НПЗ, работающих по профилю первичной переработки нефти. Стоит отметить, что для производств, обладающих развитой архитектурой вторичных процессов, ресурсов одной УПВ может быть недостаточно.
Молодой парень придумал, как из воды добыть водород
Парень сделал установку для получения водорода
Роман Урсу. В этом видео хотел показать, как можно из 10 лезвий для бритья сделать небольшой генератор, который будет извлекать из воды водород. Для начала понадобится блок питания от 5 до 12 вольт, силы тока от 0,5 до 2 ампер. Медные провода, стеклянная баночка с герметичной винтовой крышкой. Пластиковая бутылка, кусок пластмассовой линейки. Две капельницы. 10 лезвий. Пищевая соль.
Инструменты: паяльник, клеевый пистолет, канцелярский нож.
Приступим к работе. Залудим края лезвий. Далее всё устанавливаем на линейку. Обратите внимание, расстояние между лезвиями минимально, они не должны соприкасаться. Слишком большое пространство между ними оставлять не надо, иначе потребуется мощный блок питания.
Обратите внимание, расстояние между лезвиями минимально, они не должны соприкасаться. Слишком большое пространство между ними оставлять не надо, иначе потребуется мощный блок питания.
Берем проводки и припаиваем через одно лезвие. Схема подключения идентична с аккумуляторными пластинами.
Действительно ли установка может вырабатывать водород?
Генератор водорода готов. Теперь заправим его и протестируем. В качестве топлива используется соляной раствор. Несколько ложек соли и вода из-под крана. Иногда используют разбавители, растворители, пищевую соду. От раствора зависит от температуры пламени. В пластиковую бутылку наливаем воду без примесей. Обратите внимание, чтобы крышечки и соединения не пропускали газа. Настал ответственный момент. Подключить провода к блоку питания и проверить, как добывается водород.
Металлическую крышку заменил на другую, предыдущая была не герметична. Мастер советует использовать банки с крышками поплотнее. Вместо клеевого пистолета использовать холодную сварку, так как силикон со временем смягчается.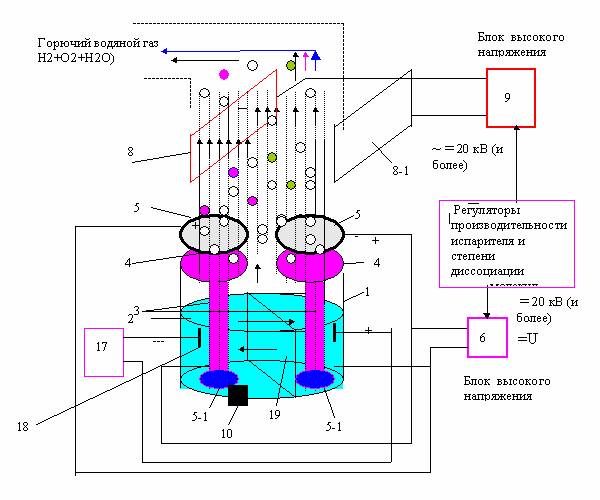 В целом всё отлично работает.
В целом всё отлично работает.
Как сделать генератор водорода? Конвертер воды в топливо? С помощью электрического воздействия с использованием простой воды можно получить газ и собирать в специальный контейнер и использовать этот газ (водород) для питания двигателей или других приборов. Мы сделаем генератор водорода! Я предлагаю сделать дома! Наблюдая за видеоуроком нам просто нужно найти способ использовать газ, который мы получили от водорода!
Обсуждение
Радж Айер
Год назад
1. Вы генерируете смесь h3 + 02 в соотношении 2: 1. 2. Для чистого газообразного водорода вы должны использовать бутылку с раствором каустической соды, в которую добавляются алюминиевые кусочки. Такая компоновка будет работать, обеспечивая хорошие объемы газа при низком давлении. Однако будьте осторожны, чтобы избежать пламени. Однажды у меня был взрыв, когда я экспериментировал в детстве. Вспышка бутылки и коррозионная щелочь были разбросаны по всему дому. Алюминий превращается в высоковязкую желатиновую соль, называемую натриево-мета-алюминатом. 3. Я хочу, чтобы вы придумали конструкцию, которая разделяет катод и анод, используя некоторую мембрану, которая может выдерживать температуры 100 градусов +, потому что при более высоких токах вода нагревается. 4. Вы не должны наносить много соли в воду. Щепотка соли в 1 литре более чем достаточна для проведения. Если вы используете больше соли, вы фактически генерируете водород вместе с хлором на аноде. Вода будет щелкать, так как ионы натрия будут реагировать с водой с образованием NaOH. Хлор будет генерировать на аноде и разъедать электрод. Поэтому вам нужно использовать углеродные электроды.
Дуайт Уилбанкс
Год назад
Несколько мыслей. Мысль 1, если лезвия были вертикальными, пузыри будут течь на вершину быстрее. Отделившись от ваших тарелок, ваши тарелки снова контактируют с вашим электролитом и могут начать делать следующий пузырь. Вторая мысль касается эффективности напряжения. Идеальное напряжение составляет от 2 до 2,5 вольт, так как вы опускаетесь ниже этого напряжения, производство падает. Когда вы поднимаете выше идеала, вы все равно получаете больше пузырьков, но, кроме того, выделяется больше тепла. Чем дальше от идеала, тем меньше эффективность. Если у вас 5-вольтовый источник, вы должны использовать нейтральную пластинку (много объяснений Google). Итак, пластина 1 положительна, пластина 2 не прикреплена ни к чему, пластина 3 отрицательна, затем повторите. Общая разница в 5 вольт разделяется на два отдельных сегмента в 2,5 вольта. Очевидно, что ваша цель состоит не в том, чтобы сделать самый эффективный инструмент промышленного класса, но с очень небольшими изменениями в вашем дизайне вы можете повысить эффективность. Поскольку соединений меньше, его фактически немного меньше работает как побочный эффект.
Вторая мысль касается эффективности напряжения. Идеальное напряжение составляет от 2 до 2,5 вольт, так как вы опускаетесь ниже этого напряжения, производство падает. Когда вы поднимаете выше идеала, вы все равно получаете больше пузырьков, но, кроме того, выделяется больше тепла. Чем дальше от идеала, тем меньше эффективность. Если у вас 5-вольтовый источник, вы должны использовать нейтральную пластинку (много объяснений Google). Итак, пластина 1 положительна, пластина 2 не прикреплена ни к чему, пластина 3 отрицательна, затем повторите. Общая разница в 5 вольт разделяется на два отдельных сегмента в 2,5 вольта. Очевидно, что ваша цель состоит не в том, чтобы сделать самый эффективный инструмент промышленного класса, но с очень небольшими изменениями в вашем дизайне вы можете повысить эффективность. Поскольку соединений меньше, его фактически немного меньше работает как побочный эффект.
piranha031091
2 года назад
Вам НИКОГДА не следует делать это с помощью стеклянного контейнера: в этом контейнере вы получите взрывоопасную смесь водорода и кислорода, поэтому у вас есть очень важная вероятность возникновения обратного огня, который заставит контейнер взорваться. Если он сделан из стекла, взрыв вызовет стеклянную осколку, которая может быть смертельной. (мой коллега несколько месяцев назад взял стеклянную осколку в горло и чуть не умер от того, что в противном случае было очень незначительным взрывом). Пластик для этого гораздо безопаснее.
Если он сделан из стекла, взрыв вызовет стеклянную осколку, которая может быть смертельной. (мой коллега несколько месяцев назад взял стеклянную осколку в горло и чуть не умер от того, что в противном случае было очень незначительным взрывом). Пластик для этого гораздо безопаснее.
Shadi2
2 года назад
он добавил соль, поэтому вместо водорода + кислород образует водород + газообразный хлор + гидроксид натрия. Вторая стадия превращает газообразный хлор в соляную кислоту, а гидроксид натрия нагревает воду. Поэтому во введении вода выглядит такой же желтой. За исключением питьевой воды, заливки ее на глаза или выпивки минутного количества хлорного газа, который ускользает, обращение с бритвенными лезвиями является самой опасной частью.
Как превратить воду в водород: простейший опыт
Солнечный генератор водорода / кислорода DIY – простой “электролиз” с использованием солнечного света! (превращает воду в топливо).
Соблюдайте безопасность в опытах с воспламеняющимися веществами!
Я покажу вам, как сделать простое устройство, которое превращает / расщепляет воду на водород и кислород.
Шаг 1: Посмотрите наглядное видео …
Шаг 2: Механизм генератора водорода
Простой эксперимент по «электролизу» показывает, как «расщеплять воду» на кислород / водород с помощью солнечной панели (или батареи) и воды. Графит в карандашах проводит электричество (от солнечной батареи или акб). В результате вода «расщепляется» на кислород / водород (процесс, известный как электролиз). Это видео в основном посвящено использованию солнечной панели, но также показывает батарею на 9 В в качестве источника питания, а также сравнение «нескольких напряжений» (ближе к концу видео) с использованием регулируемого источника питания постоянного тока (установленного через несколько интервалов – 3 В, 4,5 В, 6 В, 7,5 В, 9 В и 12 В).
Посмотрите, как увеличивается объем пузырьков с напряжением. Обратите внимание, что это обычный научный эксперимент в начальной школе, и он абсолютно безопасен. Можно представить, если этот мелкомасштабный эксперимент был «расширен» и усовершенствован, он мог бы стать хорошим способом хранения солнечной / ветровой энергии для последующего использования. очень «зеленая» технология в целом, если источником электричества является солнечный или ветровой (и когда используется водород (в качестве топлива и т. д.), единственным побочным продуктом является вода).
Шаг 3: Необходимые предметы …
1.) 2 карандаша
2.) стакан
3.) маленький кусочек картона
4.) пара проводов (я использовал черные / красные провода с зажимами типа «крокодил»)
5.) маленькая солнечная панель или батарея 9 В или трансформатор переменного / постоянного тока
Шаг 4: Во-первых, точить карандаши …
Заточите карандаши на обоих концах. Затем сделайте 2 маленьких отверстия в куске картона (на расстоянии около 1 дюйма) и протолкните карандаши в отверстия (см.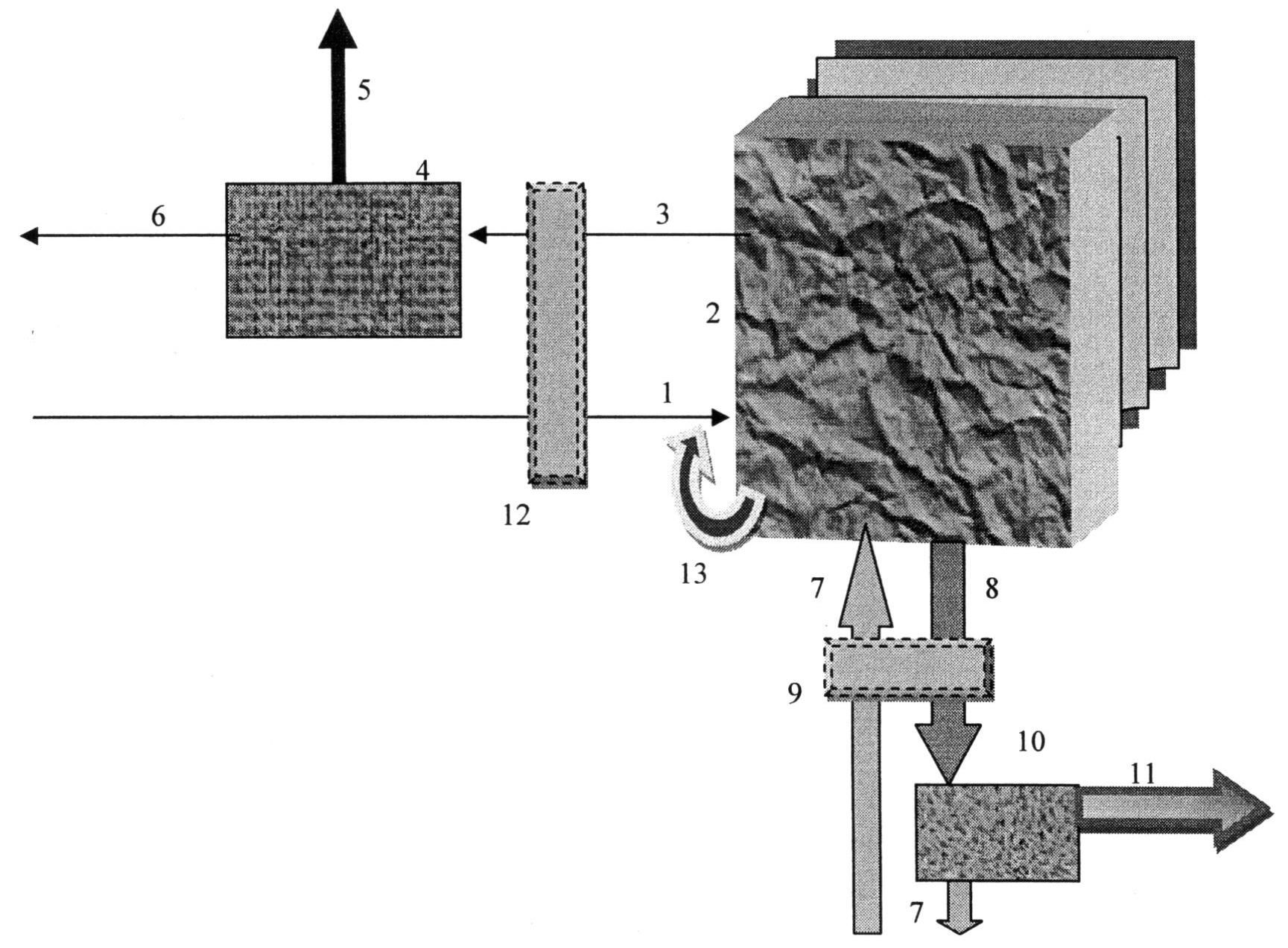 фото выше).
фото выше).
Шаг 5: добавь воды в стакан …
Долейте воды в стакан и поместите деталь (картон и карандаш) поверх стекла.
Шаг 6: Теперь подключите провода …
Теперь просто подключите провода от конца карандашей к источнику питания. Пузыри начнут формироваться немедленно. Одна интересная вещь об этом проекте – многие люди уже будут иметь все необходимое, чтобы сделать это дома. Не нужно ничего покупать (за исключением солнечной панели … но батарея 9v работает хорошо). Сделать водород и кислород дома бесплатно возможно, и все с обычными предметами домашнего обихода.
Получайте удовольствие от создания и использования! Снова посмотрите видео, чтобы увидеть, как пузыри просто стекают с карандашей. Строго соблюдайте технику безопасности!
Источник
определение производства водорода и синонимы производства водорода (английский)
Производство водорода — это семейство промышленных методов производства водорода. В настоящее время доминирующей технологией прямого производства является паровой риформинг из углеводородов. Известно много других методов, включая электролиз и термолиз.
Известно много других методов, включая электролиз и термолиз.
В 2006 году производственная мощность США оценивалась в 11 миллионов тонн водорода. 5 миллионов тонн водорода было израсходовано на месте при переработке нефти, а также при производстве аммиака (процесс Габера) и метанола (восстановление монооксида углерода).0,4 миллиона тонн были побочным продуктом хлорщелочного процесса. [1]
Паровой риформинг
Основная статья: Реформирование SteamИскопаемые виды топлива являются основным источником промышленного водорода. [2] Водород можно генерировать из природного газа с эффективностью примерно 80% или из других углеводородов с различной степенью эффективности. В частности, водород в массе обычно получают путем парового риформинга метана или природного газа [3] При высоких температурах (700–1100 ° C) пар (H 2 O) реагирует с метаном (CH 4 ), образуя выход синтез-газа.
- CH 4 + H 2 O → CO + 3 H 2 + 191,7 кДж / моль [4]
Газификация
На второй стадии дополнительный водород генерируется в результате реакции конверсии водяного газа при более низкой температуре, проводимой при температуре около 130 ° C:
- CO + H 2 O → CO 2 + H 2 -40,4 кДж / моль
По существу, атом кислорода (O) отделяется от дополнительной воды (водяного пара), чтобы окислить CO до CO 2 . Это окисление также дает энергию для поддержания реакции. Дополнительное тепло, необходимое для запуска процесса, обычно получают за счет сжигания некоторой части метана.
Это окисление также дает энергию для поддержания реакции. Дополнительное тепло, необходимое для запуска процесса, обычно получают за счет сжигания некоторой части метана.
CO 2 секвестрация
При паровом риформинге образуется диоксид углерода (CO 2 ). Поскольку производство сосредоточено на одном предприятии, можно отделить CO 2 и утилизировать его без выброса в атмосферу, например, закачив его в нефтяной или газовый резервуар (см. Улавливание углерода), хотя в настоящее время это не делается. в большинстве случаев.Норвежская компания StatoilHydro начала проект закачки углекислого газа в Северном море на месторождении Слейпнер. Это оспаривается в книге « Шумиха о водороде: факты и вымысел в гонке за сохранение климата» , книге Джозефа Дж. Ромма, опубликованной в 2004 г. издательством Island Press и обновленной в 2005 г. Ромм говорит, что прямое сжигание ископаемого топлива дает меньше CO 2 , чем производство водорода. [ требуется ссылка ]
[ требуется ссылка ]
Интегрированный паровой риформинг / когенерация — можно объединить паровой риформинг и когенерацию пара и электроэнергии в одной установке.Это может принести пользу нефтеперерабатывающему заводу, поскольку он более эффективен, чем отдельные водородные, паровые и энергетические установки. Air Products недавно построила интегрированную установку парового риформинга / когенерации в Порт-Артуре, штат Техас. [5]
Другие методы производства из ископаемого топлива
Частичное окисление
Реакция частичного окисления происходит, когда субстехиометрическая топливно-воздушная смесь частично сгорает в установке риформинга, образуя синтез-газ, обогащенный водородом.Различают парциальное термическое окисление (TPOX) и частичное каталитическое окисление (CPOX). Химическая реакция принимает общий вид:
- C n H m + n / 2 O 2 → n CO + m / 2 H 2
Идеальные примеры для топочного мазута и угля, предполагающие составы C 12 H 24 и C 24 H 12 соответственно, следующие:
- C 12 H 24 + 6 O 2 → 12 CO + 12 H 2
- C 24 H 12 + 12 O 2 → 24 CO + 6 H 2
Плазменный риформинг
Процесс Kværner или процесс Kvaerner сажи и водород (CB&H) [6] — метод плазменного риформинга, разработанный в 1980-х годах одноименной норвежской компанией для производства водорода и технического углерода из жидких углеводородов.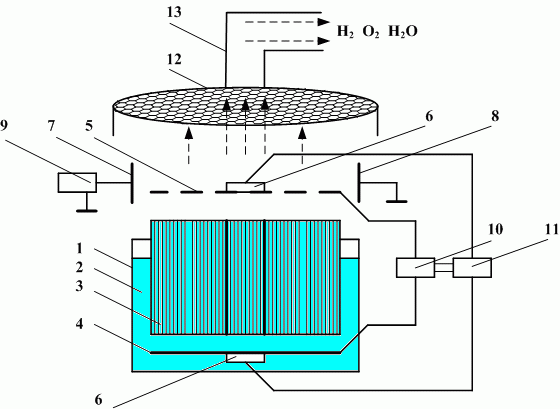 (C n H м ).Примерно 48% доступной энергии сырья содержится в водороде, 40% — в активированном угле и 10% — в перегретом паре. [7] CO 2 не производится.
(C n H м ).Примерно 48% доступной энергии сырья содержится в водороде, 40% — в активированном угле и 10% — в перегретом паре. [7] CO 2 не производится.
Вариант этого процесса представлен в 2009 году с использованием технологии утилизации отходов плазменной дуги для производства водорода, тепла и углерода из метана и природного газа в плазменном конвертере [8]
Уголь
Уголь может быть преобразован в синтез-газ и метан, также известный как городской газ, посредством газификации угля.Синтез-газ состоит из водорода и окиси углерода. [9] Другой способ конверсии — низкотемпературная и высокотемпературная карбонизация угля. [10]
Из воды
Основная статья: Разделение воды Многие технологии были исследованы, но следует отметить, что по состоянию на 2007 год «тепловые, термохимические, биохимические и фотохимические процессы пока не нашли промышленного применения». [2] Только высокотемпературный электролиз щелочных растворов находит применение.
[2] Только высокотемпературный электролиз щелочных растворов находит применение.
Электролиз
Примерно 5% промышленного водорода производится электролизом. Популярны два типа ячеек: ячейки для твердооксидного электролиза (SOEC) и ячейки для щелочного электролиза (AEC). Эти элементы оптимально работают при высоких концентрациях электролита (КОН или карбонат калия) и при высоких температурах, часто около 200 ° C. Типичными катализаторами являются стабилизированный иттрием цирконий вместе с никелем. [11] [12] На 243-м Национальном собрании и выставке Американского химического общества (ACS) в 2012 году было описано, как можно использовать тепло атомных электростанций.МАГАТЭ помогает с его Программой экономической оценки водорода (HEEP). [13]
Термолиз
Вода самопроизвольно диссоциирует при температуре около 2500 ° C, но этот термолиз происходит при температурах, слишком высоких для обычных технологических трубопроводов и оборудования. Катализаторы необходимы для снижения температуры диссоциации.
Фотобиологическое расщепление воды
Основная статья: Биологическое производство водородаБиологический водород можно производить в биореакторе для водорослей [14] .В конце 1990-х годов было обнаружено, что, если водоросли лишены серы, они переключатся с производства кислорода, то есть нормального фотосинтеза, на производство водорода. Кажется, что производство в настоящее время экономически целесообразно, если превзойти барьер энергоэффективности 7–10% (преобразование солнечного света в водород). [15] . с производительностью водорода 10-12 мл на литр культуры в час [16] .
Фотокаталитическое расщепление воды
Основная статья: Фотокаталитическое расщепление водыПреобразование солнечной энергии в водород посредством процесса разделения воды — один из наиболее интересных способов создания экологически чистых и возобновляемых источников энергии.Однако, если этому процессу способствуют фотокатализаторы, суспендированные непосредственно в воде, вместо использования фотоэлектрической и электролитической систем, реакция проходит всего за одну стадию, поэтому она может быть более эффективной. [17] [18]
Серно-йодный цикл
Серо-йодный цикл (цикл S-I) — это термохимический процесс, при котором из воды выделяется водород, но с гораздо большей эффективностью, чем при расщеплении воды. Сера и йод, используемые в процессе, восстанавливаются и повторно используются, а не потребляются в процессе.Он хорошо подходит для производства водорода высокотемпературными ядерными реакторами или путем концентрирования солнечных энергетических систем (CSP). [19]
Биоводородные маршруты
Несмотря на отсутствие промышленного значения, потоки [2] биомассы и отходов в принципе можно преобразовать в биоводород с помощью газификации биомассы, парового риформинга или биологического преобразования, такого как биокатализируемый электролиз или ферментативное производство водорода.
Производство ферментативного водорода
Основные статьи: ферментативное производство водорода и темное брожениеФерментативное производство водорода — это ферментативное преобразование органического субстрата в биоводород, проявляемое разнообразной группой бактерий с использованием мультиферментных систем, включающих три стадии, аналогичные анаэробному преобразованию.Реакции темного брожения не требуют световой энергии, поэтому они способны постоянно производить водород из органических соединений в течение дня и ночи. Фотоферментация отличается от темной ферментации тем, что она протекает только при наличии света. Например, фотоферментация с помощью Rhodobacter sphaeroides Sh3C может использоваться для превращения низкомолекулярных жирных кислот в водород. [20]
Ферментативное производство водорода может осуществляться с использованием прямого биофотолиза зелеными водорослями, непрямого биофотолиза цианобактериями, фотоферментации анаэробными фотосинтезирующими бактериями и темного брожения анаэробными ферментативными бактериями.Например, в литературе сообщается об исследованиях производства водорода с использованием H. salinarium , анаэробных фотосинтезирующих бактерий, связанных с донором гидрогеназы, таким как E. coli . [21]
Биоводород можно производить в биореакторах, в которых используется сырье, причем наиболее распространенным сырьем являются потоки отходов. В процессе участвуют бактерии, питающиеся углеводородами и выдыхающие водород и CO 2 . CO 2 можно успешно изолировать несколькими способами, оставив газообразный водород.Прототип водородного биореактора, использующего отходы в качестве сырья, работает на заводе по производству виноградного сока Велча на северо-востоке штата Пенсильвания (США).
Производство ферментативного водорода
Из-за предела Тауэра (четыре H 2 / глюкоза) для темной ферментации был разработан неприродный ферментативный путь, который может генерировать 12 моль водорода на моль единиц глюкозы полисахаридов и воды в 2007 году. [22] Стехиометрическая реакция:
- C 6 H 10 O 5 + 7 H 2 O → 12 H 2 + 6 CO 2
Ключевая технология — бесклеточная биотрансформация синтетических ферментов (SyPaB). [23] [24] Биохимик может понять это как «окисление глюкозы с использованием воды в качестве окислителя». Химик может описать это как «расщепление воды энергией на углеводы». Ученый-термодинамик может описать это как первую энтропийную химическую реакцию, которая может производить водород за счет поглощения отходящего тепла. В 2009 году целлюлозные материалы были впервые использованы для получения водорода с высоким выходом. [25] Кроме того, было предложено использование углевода в качестве носителя водорода с высокой плотностью, чтобы устранить наибольшее препятствие на пути к экономии водорода и предложить концепцию транспортных средств на сахарных топливных элементах. [26]
Синтетическая биология [27] [28] [29]
Биокатализируемый электролиз
Ячейка для микробного электролиза
Основные статьи: электрогидрогенез и микробный топливный элементПомимо темного брожения, другой возможностью является электрогидрогенез (электролиз с использованием микробов). Используя микробные топливные элементы, сточные воды или растения могут использоваться для выработки энергии. Биокатализируемый электролиз не следует путать с биологическим производством водорода, поскольку последний использует только водоросли, а с последним водоросли сами генерируют водород мгновенно, тогда как при биокатализируемом электролизе это происходит после прохождения микробного топливного элемента и множества водных растений. [30] Можно использовать .К ним относятся тростник сладкая трава, кордграсс, рис, помидоры, люпин, водоросли [31]
Возобновляемый водород
В настоящее время существует несколько практических способов производства водорода в возобновляемом промышленном процессе. Один из них — использовать свалочный газ для производства водорода в установке парового риформинга, а другой — использовать возобновляемые источники энергии для производства водорода в результате электролиза. Водородное топливо, производимое из возобновляемых источников энергии, таких как энергия ветра или солнца, является возобновляемым топливом. [32]
Использование водорода
Водород в основном используется для преобразования тяжелых нефтяных фракций в более легкие посредством процесса гидрокрекинга и других нефтяных фракций (дегидроциклизация и процесс ароматизации).Он также необходим для очистки ископаемого топлива путем гидрообессеривания.
Водород в основном используется для производства аммиака по методу Габера. В этом случае водород производится на месте. Аммиак — основной компонент большинства удобрений.
Раньше было принято сбрасывать излишки водорода, в настоящее время технологические системы уравновешиваются водородом для сбора водорода для дальнейшего использования.
Водород также производится как побочный продукт промышленного производства хлора путем электролиза. Национальная лаборатория возобновляемых источников энергии Обзор исследований за 2003 год: «Новые горизонты для водорода».
Внешние ссылки
Производство, очистка, хранение, применение и безопасность Луис М. Гандиа
Водород — идеальное топливо будущего; он может внести значительный вклад в решение двух больших проблем, с которыми сталкивается современное общество: безопасность энергоснабжения, а также воздействие на окружающую среду и глобальное потепление, вызванное загрязнителями, выделяемыми при использовании ископаемого топлива.Однако для того, чтобы водород стал реальным решением, его необходимо получать экологически рациональными способами, то есть из возобновляемых источников энергии. В этой книге основное внимание уделяется последним технологическим достижениям в области производства водорода из воды, а также из обработки биомассы, которые являются основными способами перехода к экологически безопасному водороду. Области, охватываемые темой водородной энергетики, быстро выросли, и теперь она стала явно междисциплинарной. Таким образом, помимо производства, очистка водорода и особенно его хранение являются ключевыми проблемами, которые могут ограничить использование водородного топлива.В этой книге рассматривается очистка водорода с помощью мембранной технологии и его хранение в «твердой» форме с использованием новых гидридов и углеродных материалов. Другие новинки этого тома включают кондиционирование энергии водяных электролизеров, интеграцию в электрическую сеть возобновляемых водородных систем, будущую роль микрореакторов и микропроцессов в водородной технологии, а также потенциал вычислительной гидродинамики для проектирования водородного оборудования и оценка вопросов безопасности.И, наконец, учитывая, что транспорт, вероятно, станет первым коммерческим применением водородного топлива, две главы посвящены последним достижениям в области водородных топливных элементов и двигателей внутреннего сгорания, работающих на водороде, для транспортных средств.
Рассмотрены водород из воды и биомассы
Целостный подход к теме производства возобновляемого водорода
Рассмотрены кондиционирование воды в электролизерах и интеграция систем возобновляемой водородной энергетики
Предметы, не включенные в предыдущие книги по водородной энергии
Рассмотрены микропроцессорные технологии
Предмет, не включенный в предыдущие книги по водородной энергии
Рассмотрены приложения CFD
Предмет, не включенный в предыдущие книги по водородной энергии
Фундаментальные аспекты не будут подробно обсуждаться сознательно, поскольку они надлежащим образом рассмотрены в предыдущих книгах
Выделение о технологических достижениях
Главы, написанные признанными экспертами
Актуальный подход к предметам и соответствующие библиографические ссылки
Hydrogen View — Держите вас в авангарде приложений и технологий водородной энергетики
Загрузка…
Загрузка …- Дом
- Дом
- О нас
- Объявление
- Карьера
- Связаться
- Новости
- Все новости
- Северная Америка
- Южная Америка
- Европа
- Ближний Восток
- Азиатско-Тихоокеанский регион
- Африка
- Просмотры
- Интервью
- Колумнисты
- Мобильность
- Мощность
- Технологии
- Вебинары
- Водород: управляемый, не уменьшенный
- Вебинар Shell Hydrogen
- Рекламные возможности
- Подкасты
- Журнал
- Выпуски
- Медиа-пакет
Что такое водородная вода и стоит ли ее пить?
К настоящему времени наука ясна: самый полезный напиток, который вы можете пить, — это вода.Он не содержит сахара, соли и химикатов, которые могут повредить клетки и вызвать их старение, если он правильно фильтруется.
Если h3O так полезен для вас, то повышение содержания водорода должно сделать его еще более здоровым, верно? Именно на это делают ставку все больше и больше компаний, производящих напитки. Так называемая «водородная вода» — вода, в которой растворен газообразный водород — становится все более популярной. Несколько компаний сейчас продают бутылки этого вещества по 3 доллара, в то время как другие предлагают таблетки, которые можно растворить в воде, чтобы повысить содержание водорода.Гораздо больше людей продают машины стоимостью более 1000 долларов для людей, которые хотят заправить свои собственные домашние версии. Это все, что касается воды, которая, скорее всего, не будет иметь вкуса и внешнего вида, чем то, что выходит из-под крана.
Некоторые из этих компаний заявляют, что добавление большего количества водорода в воду увеличивает энергию, улучшает восстановление после тренировки и уменьшает воспаление, из-за чего обычная вода выглядит совершенно неуспевающей.
Но наука, стоящая за этими утверждениями, слаба, она подкреплена лишь несколькими обнадеживающими исследованиями на крысах и мышах и еще меньшим — и меньшим — испытаниями на людях.
БОЛЬШЕ: Почему ваша вода в бутылках содержит четыре разных ингредиента
Доктор Николас Перриконе, который продает то, что он называет природным антиоксидантным «напитком для восстановления энергии» под названием Dr. Perricone Hydrogen Water по цене около 3 долларов за банку, признает, что это не так. пока точно известно, как водород, добавленный в воду, потенциально действует на организм.Исследования на животных и несколько исследований на людях, проведенных, в основном, в Японии, показывают, что он может действовать как антиоксидант и уменьшать воспаление. Окислительный стресс от солнца, нормальные процессы в организме и воздействие загрязнителей могут повредить клетки и привести к преждевременному старению и таким заболеваниям, как рак. Воспаление также способствует возникновению многих хронических заболеваний, от диабета 2 типа до сердечных заболеваний и заболеваний мозга. Водород снижает и то, и другое. Это означает, по крайней мере теоретически, что водородная вода может помочь уменьшить все, от диабета до затвердевания сердечных сосудов до болезни Альцгеймера и рака.Однако исследований, чтобы доказать, так ли это, не проводилось.
Даже без этого подтверждения водородная вода — это следующая важная вещь в области оздоровления в Японии. Министерство здравоохранения недавно одобрило внутривенные инъекции водородного солевого раствора для помощи людям, выздоравливающим после инфекций и других состояний, а купание в водородной воде становится популярным спа-лечением для борьбы с морщинами и повреждениями кожи.
В США водородное помешательство в основном ограничивается водой, и заявления о нем распространены повсюду.Перриконе сосредотачивает свое внимание на влиянии водорода на энергию, которое основано на его собственном небольшом исследовании с участием 20 человек. Он измерил изменения энергии в клетках кожи после того, как люди выпили 16 унций водородной воды Dr. Perricone, и обнаружил, что у людей, которые пили ее, по-видимому, повышалась активность ферментов, ответственных за выработку энергии в клетках.
Этого было достаточно, чтобы убедить его изучить водородную воду на предмет ее способности улучшать энергию, которая, по его словам, может влиять не только на мышцы, но и на мозг.«Я не вижу недостатков в питье водородной воды», — говорит он. «Это нетоксично, это не дорого». Он также рассматривает его как альтернативу энергетическим напиткам.
БОЛЬШЕ: Имеет ли розовая гималайская соль какие-либо преимущества для здоровья?
Все-таки почему бы и нет? — недостаточно веская причина для покупки напитка, который заявляет о своей пользе для здоровья. Во-первых, неясно, сколько водорода необходимо для терапевтического эффекта и сколько воды нужно выпить, чтобы получить потенциальные выгоды.«Мы ничего не знаем о дозировке или частоте употребления водородной воды для получения пользы для здоровья», — говорит Робин Фороутан, диетолог и представитель Академии питания и диетологии. Количество водорода в различных продуктах, которые в настоящее время продаются на полках, сильно различается, и нет никаких правил для стандартизации формул — в основном потому, что нет прочной научной базы, чтобы определить, сколько нужно, чтобы повлиять на различные условия.

