Электролиз воды. Как происходит процесс и для чего он нужен
Электролизом называется особый физико-химический процесс, при котором жидкость или, иначе говоря, электролит, распадается на положительные и отрицательные ионы. Происходит это под воздействием электрического тока. Каким же образом протекает данный процесс?
Электролиз воды происходит из-за того, что электрический ток, проходя через электролит, вызывает реакцию на электродах, на которых и оседают положительные и отрицательные ионы. На отрицательно заряженном электроде (катоде) оседают катионы, соответственно, на положительном (аноде) – анионы. Электролит может состоять из воды, в которую добавлена кислота или же представляет собой раствор солей. Распад солей на металл и кислотный остаток возникает после того, как через электролит пропускается электрический ток. Заряженный положительным электричеством металл подходит к катоду (отрицательно заряженному электроду), именно этот металл и называется катионом. Кислотный остаток, отрицательно заряженный, стремится к аноду (положительно заряженному электроду), и называется анионом. Электролиз дает возможность получения из солей хорошо очищенных элементов, благодаря чему находит широкое применение в разнообразных отраслях современной промышленности.
Электролиз дает возможность получения из солей хорошо очищенных элементов, благодаря чему находит широкое применение в разнообразных отраслях современной промышленности.
Электролиз воды жизненно необходим сегодня, когда тысячи предприятий применяют воду для отдельных этапов своего производства. Объясняется это тем, что после большинства процессов, которые выполняются на предприятиях, вода после использования превращается в опасную для людей и живой природы жидкость. Электролиз воды служит для очистки сточных вод, которые не должны попадать в землю или же в источники чистой воды. Эти сточные воды необходимо очищать для того, чтобы не допустить экологическую катастрофу, риск которой и так уже достаточно высокий во многих регионах России.
Сегодня существует несколько методов электролиза воды. К ним относится электроэкстракция, электрокоагуляция и электрофлотация. Электролиз воды, применяемый для очистки сточных вод, производится в электролизерах. Это специальные сооружения, в которых органические вещества разлагаются на металлы, кислоты и другие вещества, относящиеся к категории неорганического происхождения. Особенно важно проводить очистку сточных вод на вредных производствах, таких как предприятия химической промышленности, там, где ведутся работы с медью и свинцом, а также на комбинатах, выпускающих краски, лаки, эмали. Безусловно, это далеко не дешевый способ очистки воды при помощи электролиза, но затраты, связанные с очисткой воды, не идут ни в какие сравнения со здоровьем человека и заботой об окружающей среде.
Особенно важно проводить очистку сточных вод на вредных производствах, таких как предприятия химической промышленности, там, где ведутся работы с медью и свинцом, а также на комбинатах, выпускающих краски, лаки, эмали. Безусловно, это далеко не дешевый способ очистки воды при помощи электролиза, но затраты, связанные с очисткой воды, не идут ни в какие сравнения со здоровьем человека и заботой об окружающей среде.
Интересный факт, но можно осуществить электролиз воды в домашних условиях. Этот процесс не займет много времени и средств и даст возможность для получения кислорода и водорода. В емкость с водой, в которой предварительно растворена соль, (соли необходимо взять не менее ¼ объема воды), опускаются два электрода. Их можно сделать из любого металла. Электроды подключаются к источнику питания с силой тока не менее 0,5 А. На одном из электродов образуются пузыри, что и говорит о том, что электролиз воды в домашних условиях проходит успешно. Данным способом можно получить едкий натрий, хлор и другие химические элементы, в зависимости от того, из чего состоит электролит.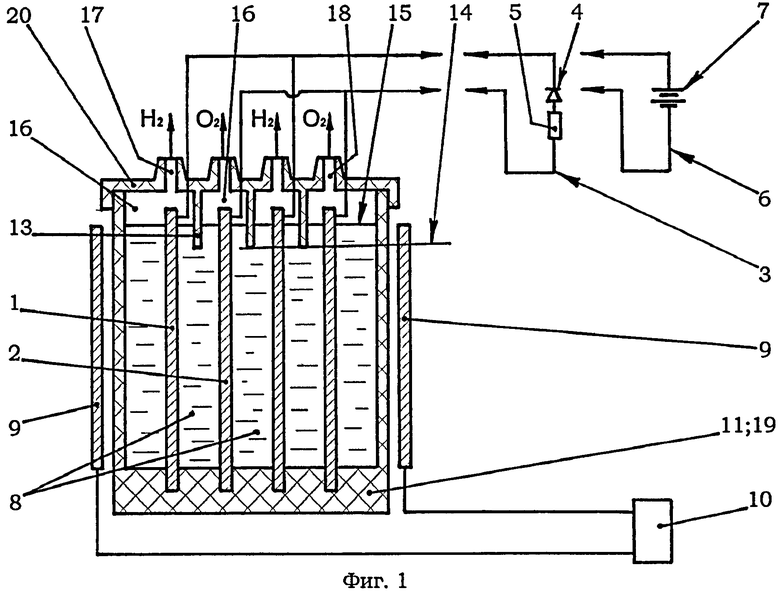 Плазменный электролиз воды применяют в плазмотеплолизерах. Это новейшее современное устройство, работающее в режимах плазменного электролиза воды и ее непосредственного нагрева до определенных температур. Плазменный электролиз воды дает возможность для получения новых видов энергии, в которой с каждым днем все больше нуждается человечество. Энергия, которую можно будет получать из воды, даст возможность для создания новых, безопасных и эффективных видов источников энергии. Явления плазменного электролиза воды еще не изучены до конца, но они имеют огромные перспективы и поэтому интенсивно изучаются современными учеными.
Плазменный электролиз воды применяют в плазмотеплолизерах. Это новейшее современное устройство, работающее в режимах плазменного электролиза воды и ее непосредственного нагрева до определенных температур. Плазменный электролиз воды дает возможность для получения новых видов энергии, в которой с каждым днем все больше нуждается человечество. Энергия, которую можно будет получать из воды, даст возможность для создания новых, безопасных и эффективных видов источников энергии. Явления плазменного электролиза воды еще не изучены до конца, но они имеют огромные перспективы и поэтому интенсивно изучаются современными учеными.
Будущее и настоящее водородной энергетики — Энергетика и промышленность России — № 14 (106) июль 2008 года — WWW.EPRUSSIA.RU
Газета «Энергетика и промышленность России» | № 14 (106) июль 2008 года
Водородная энергетика сформировалась как одно из направлений развития научно-технического прогресса в середине 1970‑х. По мере того, как расширялась область исследований, связанных с получением, хранением, транспортом и использованием водорода, становились все более очевидными экологические преимущества водородных технологий.
Успехи в развитии ряда водородных технологий (таких, как топливные элементы, транспортные системы на водороде, металлогидридные и многие другие) продемонстрировали, что использование водорода приводит к качественно новым показателям в работе систем или агрегатов.
Топливные элементы
В настоящее время в США и Канаде основные НИОКР проводятся по созданию топливных элементов (ТЭ) двух типов: с твердополимерным электролитом (PEM FC) и высокотемпературных с твердоокисным (SOFC). Только эти два направления, как наиболее перспективные, финансируются за счет средств федерального бюджета. Высокотемпературные ТЭ с расплавнокарбонатным электролитом (MCFC) продолжают изучаться в рамках программ фундаментальных исследований.
Твердополимерные ТЭ по их техническому уровню находятся на пороге коммерциализации. Однако в настоящее время их высокая стоимость (энергоустановка – примерно 110 долларов / кВт) в значительной степени сдерживает этот процесс. Для массового применения PEM FC в автотранспорте их стоимость должна быть снижена до 50‑100 долл / кВт (при современной стоимости бензина и отсутствии финансовых механизмов, учитывающих качество выхлопных газов). В недалекой перспективе в результате ужесточения стандартов на выбросы, повышения стоимости бензина и снижения стоимости ТЭ ожидается изменение конъюнктуры в пользу автомобилей и автономных энергоустановок мощностью до 100‑300 кВт с PEM FC. В этих направлениях НИОКР развиваются с возрастающей активностью.
В недалекой перспективе в результате ужесточения стандартов на выбросы, повышения стоимости бензина и снижения стоимости ТЭ ожидается изменение конъюнктуры в пользу автомобилей и автономных энергоустановок мощностью до 100‑300 кВт с PEM FC. В этих направлениях НИОКР развиваются с возрастающей активностью.
К настоящему времени созданы и успешно проходят испытания энергетическая установка на базе твердоокисных ТЭ мощностью 100 кВт с КПД по электричеству – 46 процентов и 80‑85 процентов при утилизации тепла (ресурс работы свыше 20 тысяч в час) и установка комбинированного типа мощностью 200 кВт. Однако инвестиционные расходы на строительство указанных установок еще велики – свыше 10 тысяч долларов США за кВт установленной мощности. В связи с этим основные усилия разработчиков направлены на снижение стоимости установок.
Водород для энергетики
Основные направления работ – системы водородного аккумулирования электроэнергии, автономные энергоустановки мощностью до 200 кВт с использованием ДВС, микротурбин и топливных элементов, мощные водородосжигающие энергоустановки паротурбинного цикла с водородными парогенераторами, энергоустановки на базе возобновляемых энергоресурсов с производством водорода электролизом воды (ветро‑солнечно-водородные) мощностью до нескольких мегаватт.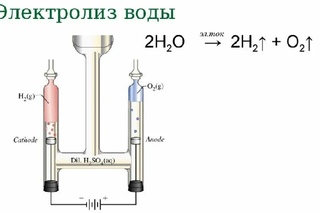
Характерная особенность работ последних лет – переход от создания ключевых элементов энергоустановок к созданию универсальных систем, полностью обеспечивающих потребителей энергией. Например, компания «Стюарт Энерджи Систем» наряду с продолжением производства электролизеров Стюарта создала производство интегрированных систем обеспечения потребителей сжатым водородом и электроэнергией. Это дает возможность расширить рынок сбыта продукции.
Новые технологии хранения
В этом направлении разработки главным образом направлены на создание бортовых систем хранения – суперлегких баллонов, компактных криогенных баков и металлогидридных систем. В настоящее время разработаны суперлегкие баллоны на давления до 450 атмосфер и выше с весовым содержанием водорода до 13 процентов, а также криогенные баки для автомобилей с экранно-вакуумной изоляцией и сроком автономного хранения более 15 суток (потери на испарение жидкого водорода
В последние 2‑3 года активизировались НИОКР по разработке систем хранения водорода в наноструктурах: фуллеренах и нанотрубках. Результаты фундаментальных исследований указывают на возможность создания таких сред хранения с емкостью по водороду до 7‑8 весовых процентов.
Результаты фундаментальных исследований указывают на возможность создания таких сред хранения с емкостью по водороду до 7‑8 весовых процентов.
Опыт производства
В этой области исследования и разработки относятся главным образом к плазмохимическим методам, новым типам электролизеров, процессам переработки угля, биоконверсии и компактным реформерам углеводородных топлив.
Сегодня реализован КПД электролизера, приблизительно равный 70‑80 процентам, в том числе для электролиза под давлением. Японскими исследователями разработаны экспериментальные мембранно-электродные блоки с твердополимерным электролитом, обеспечивающие электролиз воды с КПД > 90 процентов при плотностях тока до 3 А / см2.
Работы по новым плазмохимическим методам производства водорода вслед за пионерскими работами Института водородной энергетики и плазменных технологий (ИВЭПТ) Российского научного центра «Курчатовский институт» активно развиваются в США, Канаде, Франции и других странах. Реализация этих разработок позволит получать достаточно дешевый водород из нетрадиционного сырья и природных углеводородных топлив. Сегодня Россия в этой области лидирует, однако зарубежные работы финансируются в более крупных масштабах.
Реализация этих разработок позволит получать достаточно дешевый водород из нетрадиционного сырья и природных углеводородных топлив. Сегодня Россия в этой области лидирует, однако зарубежные работы финансируются в более крупных масштабах.
Металлогидридные разработки
Среди водородных технологий, разрабатывающихся в последние годы, металлогидридные – одни из первых, успешно выходящих на рынок. Достаточно упомянуть о NiMeHy батареях и аккумуляторах, в короткий срок занявших существенный сектор рынка компактных источников тока. В настоящее время во многих странах выпускаются компактные безопасные системы хранения водорода на основе металлогидридов, разрабатываются металлогидридные системы для автотранспорта, подводных лодок, малотоннажных судов и т. д., а также создаются новые сплавы–накопители водорода.
К сожалению, государственное финансирование отечественных работ в области водородной энергетики несопоставимо с финансированием этих работ в других странах. В сегодняшней ситуации это означает, что Россия сможет сохранить передовые позиции в НИОКР лишь по двум-трем проектам на весьма короткое время.
В сегодняшней ситуации это означает, что Россия сможет сохранить передовые позиции в НИОКР лишь по двум-трем проектам на весьма короткое время.
Вместе с тем межотраслевой и междисциплинарный характер проблемы требует комплексного подхода к ее решению и развитию разработок по более широкому кругу задач, чем это делается сейчас. В условиях нарастания темпов проведения и реализации зарубежных НИОКР и реальных перспектив ужесточения национальных и международных правовых норм в области защиты окружающей среды опоздание с развитием работ в области водородной энергетики и технологии может привести к существенным экономическим потерям.
Водородная Энергетика
Водородная Энергетика
Метод бесконтактного электролиза был запатентован еще в 1888 году Д.А. Лачиновым. Усовершенствование этого метода сулит населению земли океаны дешевенького водорода и появление сверхэффективного источника энергии, работающего по замкнутому циклу. Главной сложностью способа Лачинова являлась неувязка газовой пленки, покрывавшей с течением времени электрод и прекращавшей реакцию. Горячев И.А. предлагал биться с пленкой с помощью пульсирующего электрического поля. Фролов А.В. предложил способ повышения эффективности электролиза за счет вращения. Возникающая центробежная сила скорее отрывает пузырьки газа с поверхности электродов. Издержки мощности на преодоление сил трения в конструкции и на создание потенциального электрического поля незначительны, если сопоставить их с выходной мощностью. Другими словами эффективность системы может быть намного больше 100%. Описана и экспериментальная установка для получения водорода (и кислорода) из воды с подачей на электроды не неизменного, а модулированного напряжения. Частота модуляции связывается с своей частотой колебания молекул воды и с их пространственной структурой. Нуждается в исследовании вероятная эффективность электролиза воды в искровом разряде, удаляющем примесь кислорода, либо при облучении электромагнитными волнами светового спектра. Научноисследовательский центр «Икар» докладывает, что более вероятным источником дешевенького водорода готов стать плазменный электролиз.
Горячев И.А. предлагал биться с пленкой с помощью пульсирующего электрического поля. Фролов А.В. предложил способ повышения эффективности электролиза за счет вращения. Возникающая центробежная сила скорее отрывает пузырьки газа с поверхности электродов. Издержки мощности на преодоление сил трения в конструкции и на создание потенциального электрического поля незначительны, если сопоставить их с выходной мощностью. Другими словами эффективность системы может быть намного больше 100%. Описана и экспериментальная установка для получения водорода (и кислорода) из воды с подачей на электроды не неизменного, а модулированного напряжения. Частота модуляции связывается с своей частотой колебания молекул воды и с их пространственной структурой. Нуждается в исследовании вероятная эффективность электролиза воды в искровом разряде, удаляющем примесь кислорода, либо при облучении электромагнитными волнами светового спектра. Научноисследовательский центр «Икар» докладывает, что более вероятным источником дешевенького водорода готов стать плазменный электролиз. Авторское свидетельство на 1ый плазмоэлектролитический реактор получила группа ученых РФ в 1987 г. Так как реактор был разработан на предприятии Военнопромышленного комплекса, то авторское свидетельство было выдано с грифом «Для служебного использования» и его содержание не публиковалось в открытой печати. В описании свидетельства приведена схема конструкции реактора и результаты очистки и обеззараживания воды при помощи плазмы. Никаких сведений о генерировании плазмой доборной энергии и получении водорода в описании авторского свидетельства не приводится.
Авторское свидетельство на 1ый плазмоэлектролитический реактор получила группа ученых РФ в 1987 г. Так как реактор был разработан на предприятии Военнопромышленного комплекса, то авторское свидетельство было выдано с грифом «Для служебного использования» и его содержание не публиковалось в открытой печати. В описании свидетельства приведена схема конструкции реактора и результаты очистки и обеззараживания воды при помощи плазмы. Никаких сведений о генерировании плазмой доборной энергии и получении водорода в описании авторского свидетельства не приводится.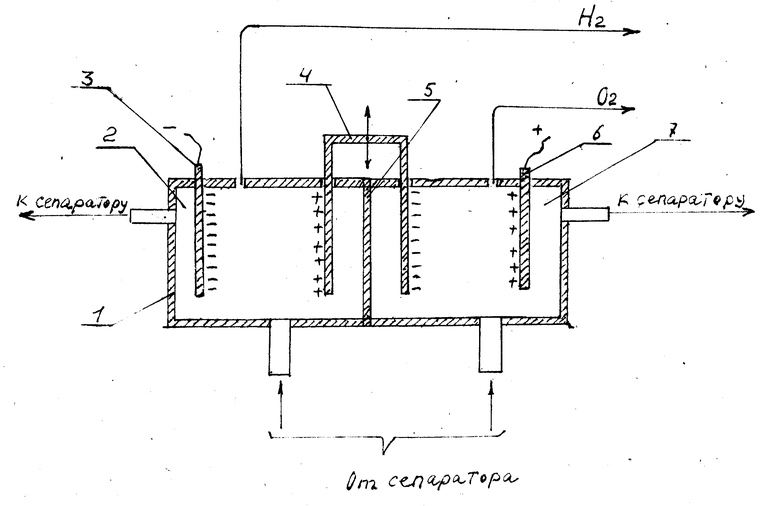
В 1998 г возникают новейшие экспериментальные данные о наличии доборной энергии в плазмоэлектролитическом процессе. Заказать промышленная тара по лучшей цене в компании Полимерная Тара.
<< В начало < Предыдущая 1 2 3 4 5 6 Следующая > В конец >>
7.4.2. ЭЛЕКТРОЛИТИЧЕСКОЕ РАЗЛОЖЕНИЕ (ЭЛЕКТРОЛИЗ) ВОДЫ. История электротехники
Читайте также
Установка распылителя воды
Установка распылителя воды Уже не раз было сказано, что современный рынок представляет широкий выбор различных сантехнических устройств как отечественных, так и зарубежных производителей. Выбрать какое-нибудь кухонное устройство нетрудно, и помощь от него в работе
Происхождение воды
Происхождение воды Источники получения питьевой воды в зависимости от водозабора подразделяют на две основные группы – подземные воды и поверхностные
Подземные воды
Подземные воды Артезианские воды
Речь идет о водах, которые с помощью насоса поднимаются на поверхность из подземного пространства. Они могут залегать под землей в несколько слоев или так называемых ярусов, которые изолированы друг от друга и отделены хотя бы одним
Они могут залегать под землей в несколько слоев или так называемых ярусов, которые изолированы друг от друга и отделены хотя бы одним
Артезианские воды
Артезианские воды Речь идет о водах, которые с помощью насоса поднимаются на поверхность из подземного пространства. Они могут залегать под землей в несколько слоев или так называемых ярусов, которые изолированы друг от друга и отделены хотя бы одним водонепроницаемым
Подрусловые воды
Подрусловые воды Эта вода добывается насосами из скважин, глубина которых соответствует отметкам дна ручья, реки или озера. Качество такой воды в значительной степени определяется поверхностной водой в самом водотоке, т. е. вода, добытая при помощи инфильтрационного
Поверхностные воды
Поверхностные воды Речная вода
Речная вода сильнее всего подвергается загрязнению, поэтому в последнюю очередь пригодна для целей питьевого водоснабжения. Она загрязняется продуктами жизнедеятельности людей и животных. В еще большей степени загрязнение речных вод
Она загрязняется продуктами жизнедеятельности людей и животных. В еще большей степени загрязнение речных вод
Умягчение воды
Умягчение воды С жесткой водой сталкивается каждый, достаточно вспомнить о накипи в чайнике.Жесткость пресных природных водоемов меняется в течение года, имея минимум в период паводка. Например, в Москве, которую обслуживают четыре станции водоочистки, забор воды
Картриджи для горячей воды
Картриджи для горячей воды Картриджи к фильтрам для горячей воды изготавливаются из материалов, учитывающих высокую температуру и свойства горячей воды.Производительность фильтров для горячей воды различна и определяется их габаритами, проходным сечением, а также
Многоступенчатые системы подготовки воды
Многоступенчатые системы подготовки воды
Сегодня на рынке водоочистного оборудования присутствует множество моделей и типов фильтров, предназначенных для многоступенчатой доочистки питьевой воды. Конструктивно – это соединенные между собой картриджные фильтры
Конструктивно – это соединенные между собой картриджные фильтры
Обеззараживание воды
Обеззараживание воды Микробиологические загрязнения воды занимают первое место по степени риска для здоровья человека. Сегодня доказано, что опасность заболеваний от присутствующих в воде болезнетворных микроорганизмов в тысячи раз выше, чем при загрязнении воды
Обеззараживание воды ультрафиолетовым излучением
Обеззараживание воды ультрафиолетовым излучением Ультрафиолетовым называется электромагнитное излучение в пределах длин волн от 100 до 400 нм. Для обеззараживания используется «ближняя область»: 200–400 нм (длина волн природного ультрафиолетового излучения у поверхности
4.
 Обработка воды сильными окислителями
Обработка воды сильными окислителями
4. Обработка воды сильными окислителями Обеззараживание воды реагентными методами осуществляется добавлением в воду различных химических дезинфицирующих средств или проведением специальных мероприятий. Применение химических веществ в обработке воды обычно приводит
4.3. Другие галогены для обеззараживания воды
4.3. Другие галогены для обеззараживания воды 4.3.1. Йодирование Йод – химический элемент из группы галогенов, «родственниками» которого являются фтор, хлор и бром, обозначается символом I (от греч. iodes – фиолетовый; лат Iodum), имеет порядковый номер 53, атомный – 126,90, плотность
7.4.5. ЭЛЕКТРОЛИТИЧЕСКОЕ ПОЛУЧЕНИЕ И РАФИНИРОВАНИЕ МЕТАЛЛОВ
7. 4.5. ЭЛЕКТРОЛИТИЧЕСКОЕ ПОЛУЧЕНИЕ И РАФИНИРОВАНИЕ МЕТАЛЛОВ
Электроосаждение металла на катоде лежит в основе электрохимического получения металлов из растворов (гидроэлектрометаллургия) или из расплавов, а также рафинирования (очистки) металлов.Металлы, имеющие
4.5. ЭЛЕКТРОЛИТИЧЕСКОЕ ПОЛУЧЕНИЕ И РАФИНИРОВАНИЕ МЕТАЛЛОВ
Электроосаждение металла на катоде лежит в основе электрохимического получения металлов из растворов (гидроэлектрометаллургия) или из расплавов, а также рафинирования (очистки) металлов.Металлы, имеющие
Из-под воды – под воду
Из-под воды – под воду Ракета 83Р комплекса РПК-6 «Водопад»В декабре 1969 года вышло постановление Совета Министров о создании противолодочного ракетного комплекса РПК-6 «Водопад» с ракетами 83Р (МГТ в качестве боевой части) и 84Р (с ядерной БЧ) для оснащения подводных лодок.
Роль российского природного газа в развитии водородной энергетики
Олег АКСЮТИНЗаместитель председателя правления – начальник департамента № 623 ПАО «Газпром», член-корреспондент РАН, д.
 т. н.
т. н.e-mail: [email protected]Александр ИШКОВ
Заместитель начальника департамента – начальник управления ПАО «Газпром», профессор кафедры ЮНЕСКО «Зеленая химия для устойчивого развития» РХТУ им. Д.И. Менделеева, д. х. н.
e-mail: [email protected]Константин РОМАНОВ
Ответственный секретарь координационного комитета «Газпром» по вопросам рационального природопользования, начальник отдела ПАО «Газпром», к. э. н.
e-mail: [email protected]Роман ТЕТЕРЕВЛЕВ
Заместитель начальника
отдела ПАО «Газпром»
e-mail: [email protected]
Аннотация. В условиях набирающего силу тренда на декарбонизацию мировой экономики возможность энергетического применения водорода связана с отсутствием прямых выбросов в атмосферу загрязняющих веществ и диоксида углерода. В статье рассмотрены преимущества развития водородной энергетики на основе природного газа, включая перспективные технологии (термокаталитический, плазменный пиролиз метана), и оптимальные решения по экспорту энергоносителя.
Ключевые слова: водородная энергетика, пиролиз метана, углеродный след, углерод, метано-водородная смесь.
Abstract. Under over-growing trend of decarbonization of the world economy, the possibility of hydrogen energy is linked to absence of direct toxic and greenhouse gases emissions. The article considers the advantages of developing hydrogen energy based on natural gas, including perspective technologies (thermos-catalytic pyrolysis, plasma pyrolysis), and optimal solutions for energy supplies.
Keywords: hydrogen energy, methane pyrolysis, carbon footprint, carbon black, methane-hydrogen mixture.
Мировой спрос на водород: настоящее и будущее
Сегодня спрос на водород в чистом виде составляет около 70 млн тонн в год. Основным сырьем его производства является природный газ, который используется в процессе паровой конверсии метана (steam methane reforming – SMR) – основного способа получения водорода в мире на нефтеперерабатывающих заводах, при производстве аммиака и метанола. Вклад природного газа в мировое производство водорода оценивается в 205 млрд кубометров в год [1].
Вклад природного газа в мировое производство водорода оценивается в 205 млрд кубометров в год [1].
На текущий момент более 95 % мирового потребления водорода приходится на традиционные отрасли, в основном самостоятельно обеспечивающие потребности в этом газе за счет его производства на специализированных установках непосредственно в месте потребления. Таким образом, несмотря на рост спроса на водород в мире, глобального рынка этого продукта на данный момент не существует. Водород сейчас является сырьем или реагентом в отраслях промышленности, при этом рядом стран мира водород начинает рассматриваться в качестве энергоносителя для решения климатических задач, получения, накопления, хранения и доставки энергии. Следует учитывать, что водород является вторичным энергоносителем, то есть требуется дополнительная энергия для его производства, что всегда будет отражаться на себестоимости (природный газ в отличие от водорода является первичным источником энергии).
К перспективным областям использования водорода относят энергетический комплекс, промышленность, транспортный сектор, а также бытовое применение в жилищно-коммунальном хозяйстве [2].
Будущий рынок водорода оценивается в очень широких пределах. По разным оценкам, к 2050 году доля водорода в мировом энергетическом балансе может составить от 7 % (IRENA) до 24 % (Bloomberg NEF) при реализации различных сценариев декарбонизации мировой экономики. Необходимо отметить, что целесообразность использования водородных энергоносителей в той или иной области определяется условиями каждой отдельной национальной экономики.
Водородная стратегия Европейского союза
8 июля 2020 года Европейская комиссия опубликовала Стратегию в области водорода (Building a hydrogen economy for a climate-neutral Europe) [3]. В этот же день было официально объявлено о начале работы Альянса по развитию «чистого» водорода (Сlean Hydrogen Alliance). В Стратегии впервые приводится подробная классификация различных видов этого газа в зависимости от источника происхождения и способа производства (рис. 1).
Рис. 1. Классификация водорода в Европейском союзеВ ЕС установлены исключительно кратко- и среднесрочные показатели для возобновляемого водорода:
– на первом этапе (2020–2024 гг. ) – производство 1 млн т возобновляемого водорода и установка электролизеров общей мощностью не менее 6 ГВт;
) – производство 1 млн т возобновляемого водорода и установка электролизеров общей мощностью не менее 6 ГВт;
– на втором этапе (2025–2030 гг.) – производство 10 млн т возобновляемого водорода и установка мощностей по его производству в объеме не менее 40 ГВт.
При этом ожидается, что доля водородного топлива (все виды) в энергобалансе ЕС вырастет с текущих менее 2 % до 13–14 % к 2050 году [3].
В соответствии с немецкой водородной стратегией спрос на водород в среднесрочной перспективе (до 2030 года) удвоится до 90–110 ТВт·ч Н2. Существующие и перспективные мощности возобновляемой энергетики Германии будут способны обеспечить производство порядка 14 ТВт·ч Н2 (примерно 0,4 млн т) «зеленого» водорода электролизом воды. Оставшуюся часть спроса на водород (76–96 ТВт·ч Н2) предполагается покрыть за счет использования других низкоуглеродных технологий производства водорода, в том числе из природного газа, или импорта.
Драйвером развития германского водородного сектора выступает металлургическая отрасль с объемом спроса на водород 10 ТВт·ч Н2 в 2030 году и 80 ТВт·ч Н2 в 2050 году [4]. В январе 2021 года компания thyssenkrupp Steel Europe объявила об успешном окончании этапа предпроектной работы по техническому обоснованию возможности обеспечения одной из сталелитейных установок в г. Дуйсбург низкоуглеродным водородом, получаемым из природного газа с использованием технологии улавливания и захоронения СО2. При этом хранить СО2 предполагается с использованием мощностей проектов Northern Light (Норвегия) и Porthos (Нидерланды). По информации thyssenkrupp Steel Europe полная производственно-сбытовая цепочка может быть организована к 2027 году. Согласно экономическим расчетам, полученным в ходе предпроектного исследования, цена на «голубой» водород составит около 2,1 евро/кг (58 евро/МВт·ч) при прогнозируемой в долгосрочной перспективе цене на природный газ 23 евро/МВт·ч [5].
В январе 2021 года компания thyssenkrupp Steel Europe объявила об успешном окончании этапа предпроектной работы по техническому обоснованию возможности обеспечения одной из сталелитейных установок в г. Дуйсбург низкоуглеродным водородом, получаемым из природного газа с использованием технологии улавливания и захоронения СО2. При этом хранить СО2 предполагается с использованием мощностей проектов Northern Light (Норвегия) и Porthos (Нидерланды). По информации thyssenkrupp Steel Europe полная производственно-сбытовая цепочка может быть организована к 2027 году. Согласно экономическим расчетам, полученным в ходе предпроектного исследования, цена на «голубой» водород составит около 2,1 евро/кг (58 евро/МВт·ч) при прогнозируемой в долгосрочной перспективе цене на природный газ 23 евро/МВт·ч [5].
Особенности развития водородной энергетики в России
В июне 2020 года направление «Водородная энергетика» впервые было включено в состав Энергетической стратегии Российской Федерации на период до 2035 года. Стратегия включает положения в области производства, транспортировки и хранения водорода, нормативно-правовой базы, интенсификации международного сотрудничества. Согласно данному документу, Россия планирует экспортировать к 2024 году 0,2 млн тонн водорода, а к 2035 году – 2 млн тонн водорода, при этом целевые показатели для внутреннего рынка не предусмотрены [6].
Промышленное хранение водородаИсточник: etanker.com
В экономических условиях России основными областями развития внутреннего рынка энергетического водорода будут являться премиальный транспорт, а также реальный сектор экономики, поставляющий продукцию на экспорт и заинтересованный в сокращении ее «углеродного следа». Вместе с тем представляется целесообразным сформировать направления всестороннего, но локального применения водородной энергетики. Так, в регионах могут быть созданы отдельные небольшие водородные энергосистемы в виде водородных кластеров или автономных энергосистем. По мировому опыту такие системы имеют скорее демонстрационно-репутационный характер, поэтому не смогут сформировать полноценный рынок водородных энергоносителей в России в просматриваемой перспективе, однако они могут стимулировать создание отечественного водородного энергетического оборудования, водородных технологий и решений для поставок на экспорт, а также технологическую базу. Примером такого подхода может являться создание технопарков с обеспечением возможности свободной реализации водородных инновационных проектов и отработки товарно-логистических цепочек.
Кроме того, в целях апробации и комплексного внедрения водородных технологий целесообразно создание опытных полигонов, например, в областях:
– применения нативных источников холода в производстве и транспорте водорода;
– получения водорода из природного газа с улавливанием и захоронением (использованием) углерода в виде углекислого газа;
– получения водорода из природного газа с улавливанием углерода в твердой форме;
– производства аммиака из низкоуглеродного водорода с ограниченными прямыми выбросами углекислого газа для транспортировки водорода, в том числе на азиатский рынок;
– хранения и транспортировки водорода в химически связанном виде.
В качестве основных критериев для создания водородных кластеров, автономных энергосистем, полигонов являются наличие сырьевой базы, геологических формаций (в случае захоронения СО2), а также близость к потенциальным рынкам сбыта.
Для развития технологий производства водорода из природного газа представляется возможным создание технологических экспериментально-демонстрационных комплексов на базе существующих научных организаций и объединений, на котором в дальнейшем будет проводиться экспериментально-демонстрационная отработка и развитие технологий и технологических установок, разрабатываемых или планируемых к разработке в рамках НИОКР.
Таким образом, учитывая, что в России до конца не исчерпан потенциал природного газа для низкоуглеродного развития национальной экономики, водородная энергетика в кратко- и среднесрочной перспективе будет сфокусирована на экспортном направлении и реализации ряда пилотных проектов в соответствии с Планом мероприятий «Развитие водородной энергетики в Российской Федерации до 2024 года».
Экспортно-ориентированное производство водорода
Для формирования экспортно-ориентированного производства водорода из природного газа требуется анализ емкости и ценовых параметров целевых рынков потребления водорода (спроса на водород) и, что очень важно, способов транспортировки водородной продукции.
По азиатскому направлению целесообразно рассмотрение возможностей поставок водорода в различном виде на экспорт авто-, морским и железнодорожным транспортом, для чего необходимо создание соответствующей законодательной базы (в части налогообложения и таможенного регулирования), а также развитие технологий транспортировки. В частности, особый интерес представляет возможность производства водорода на территории Дальнего Востока России методом парового риформинга метана с обеспечением улавливания и захоронения диоксида углерода и последующим экспортом Н2 в страны-потребители (Япония, Южная Корея, Китай). Соответственно, в рамках двустороннего сотрудничества с азиатскими партнерами в краткосрочной перспективе целесообразно развивать обмен технологиями транспортировки водорода, а также улавливания, хранения и использования СО2. В средне- и долгосрочной перспективе возможна проработка поставок водорода на экспорт при условии коммерческого спроса на него в странах – потенциальных импортерах.
Если рассматривать европейский рынок, то перспективными являются исследования оптимальных маршрутов транспортировки водорода. В основе таких решений может лежать использование различных жидких и твердых органических и неорганических соединений для транспортировки водорода в химически и/или физически обратимо связанном состоянии на экспорт. Транспортировка водорода в жидком состоянии требует применения сложного технологического оборудования для сжижения водорода до температуры –253 °C (для сравнения СПГ: –161,5 °C), систем регазификации, а также специальных сосудов для его транспортировки, что повлияет на стоимость водорода и его конкурентоспособность на зарубежных рынках. Возможным вариантом является поставка водорода в необратимо связанном состоянии, например, в виде аммиака, метанола, этанола и др.
Технология транспортировки водорода в виде метано-водородной смеси по существующей системе газопроводов обусловлена рисками технического, юридического и регуляторного характера.
Во-первых, добавление водорода в существующую газотранспортную сеть приведет к изменению состава, качества и цены экспортируемого газа, что будет являться нарушением экспортных контрактных обязательств, а также потребует отдельной специальной сертификации магистрального газопровода.
Во-вторых, открытыми остаются вопросы целостности технологического оборудования вследствие насыщения металла водородом (водородное охрупчивание), обеспечения промышленной безопасности и возможных потерь из-за сверхвысокой проницаемости водорода. Применяемое при транспортировке оборудование имеет ограничения по качеству и составу газа, связанные с обеспечением безопасности работ и сохранению долгосрочной работоспособности единой системы газоснабжения. Для гарантии безопасной транспортировки метано-водородной смеси по магистральному газопроводу требуется проведение полномасштабных натурных циклических испытаний в условиях, приближенных к реальной перекачке, что в настоящее время не реализовано.
В-третьих, отсутствуют единое нормативно-техническое регулирование трубопроводной транспортировки метано-водородных смесей как в России, так и в европейских странах. В настоящее время правила смешивания водорода и природного газа в европейской сети регулируются нормативными актами каждого государства-члена ЕС с учетом технических особенностей местной инфраструктуры. Для отдельных видов газового оборудования и газовых сетей европейские стандарты допускают достаточно широкий диапазон концентраций водорода в природном газе (от 0,02 до 10 % об.), однако единые требования по допустимому содержанию водорода в газотранспортной сети, также как единые технические регламенты, отсутствуют, что не позволяет осуществлять экспортные поставки метано-водородных смесей по трубопроводам без разработки и принятия указанного регулирования на уровне ЕС, а также его гармонизации с российским законодательством (рис. 2) [7].
Экономическая несостоятельность транспортировки водорода в виде метано-водородной смеси по «Северному потоку» отмечена зарубежными аналитиками IHS Markit. Результаты анализа показывают, что использование существующей экспортной газопроводной инфраструктуры и производство низкоуглеродного водорода из российского природного газа в ЕС (1,1–1,5 долл. США/кг h3) – наиболее экономически эффективно в сравнении с транспортировкой водорода из России по газопроводу (1,9–2,1 долл. США/кг h3) [8].
Учитывая развитую единую систему газоснабжения и реализацию новых международных газотранспортных проектов, в том числе в ЕС, производство водорода или метано-водородного топлива из природного газа рядом с крупными зарубежными потребителями, например, сталелитейными промышленными предприятиями, электрогенерирующими объектами и др. – самое оптимальное решение.
Реализация данной концепции в рамках Зеленого курса ЕС (с акцентом на водородную энергетику) открывает дополнительные возможности для российской газовой отрасли. Если краткосрочный потенциал природного газа для низкоуглеродного развития ЕС заключается в быстром сокращении выбросов СО2 при замещении угольной генерации, то долгосрочный – в возможности производства из метана водорода без выбросов CO2. Это будет иметь жизненно важное значение для ЕС при реализации эффективной политики по декарбонизации экономики, поскольку ряд европейских экспертных мнений показывает, что «зеленый» водород будет значительно дороже, чем водород с низкими или нулевыми выбросами диоксида углерода, произведенный из природного газа, до 2050 года и, вероятно, дальше. Это связано с тем, что электролиз воды – очень энергоемкий процесс, требующий от 48 до 78 кВт∙ч дорогой возобновляемой электрической энергии на 1 кг полученного водорода [9] (в разы больше, чем энергопотребление процессов получения водорода из природного газа).
В соответствии с оценкой IHS Markit дополнительный спрос на природный газ в Европе как сырье для производства водорода может составить 80 млн т н. э. (или 84 млрд кубометров) к 2050 году.
Пиролиз метана – процесс получения водорода
без выбросов СО2
Один килограмм водорода, получаемого с помощью парового риформинга природного газа, сопровождается образованием порядка 9 кг СО2экв. («well-to-gate» охват) [3]. Однако предлагаемый ЕС целевой показатель углеродоемкости процессов получения водорода (в соответствии с инициативой CertifHy) составляет половину от этого значения. Следовательно, продолжение использования обычного парового риформинга метана потребует масштабного применения технологий улавливания, использования и захоронения диоксида углерода (CCUS), что несомненно отразится на себестоимости получаемого водорода, так как инвестиции в создание дополнительной производственной структуры возрастают в среднем на 16 % [9].
Существующий технологический задел, имеющийся в мире, способен обеспечить низкоуглеродное производство водорода из природного газа методом пиролиза. Пиролиз метана – это процесс разложения природного газа (органического сырья). Пиролиз метана является альтернативным подходом к получению водорода из природного газа без образования CO2 в ходе реакции: Ch5 → C↓ + 2h3↑.
При пиролизе метана образуется водород, который может быть использован в энергетике, транспортном секторе, в промышленных / химических процессах и т. д. для снижения выбросов загрязняющих веществ и парниковых газов, а также углерод в твердой форме.
Пиролиз метана относится к целому ряду процессов (по аналогии с конверсией метана), которые могут быть разделены на несколько больших классов – термический пиролиз, каталитический пиролиз, плазменный пиролиз, а также отдельно может быть выделен пиролиз в жидких средах, например, расплавах металлов.
В настоящее время пиролизом метана на промышленном уровне получают, например, технический углерод, с побочным образованием водородсодержащего газа. Процессы целенаправленного получения низкоуглеродного водорода пиролизом метана – предмет научных исследований. В то время, как компании BASF, Thyssenkrupp и Linde сосредоточились на процессе термического пиролиза, американская компания Monolith занимается плазменным пиролизом. Другой подход применяют IASS и KIT – использование жидкого металла в качестве теплоносителя. Напротив, австралийский процесс HAZER® компании Hazer Group основан на каталитическом пиролизе метана. Степень готовности технологий находится в интервале TRL4–7 [10].
Для термического разложения метана необходимы высокие температуры (выше 1000 °C). Использование катализатора помогает увеличить скорость реакции и, таким образом, снижает температуру, требуемую для конверсии природного газа. Технологической особенностью такого процесса является периодическое восстановление катализатора, что сопровождается выбросами диоксида углерода и, таким образом, повышается «углеродный след» получения водорода. Поиск дешевых катализаторов для исключения этапа восстановления – актуальное направление исследований, результаты которых уже существуют. Примером такого катализатора служит железная руда (The Hazer Process). Потребность процесса в тепловой и электрической энергии может частично покрываться за счет получаемого водорода.
Плазменный пиролиз – это способ разложения метана в плазме (например, сверхвысокочастотного разряда). В этом случае в качестве источника энергии используется электроэнергия (сетевая или возобновляемая) и, соответственно, процесс не сопровождается «прямыми» выбросами диоксида углерода.
Существенным преимуществом пиролиза метана является меньший удельный расход электроэнергии (оценивается менее 20 кВт·ч на килограмм водорода) в сравнении, например, с электролизом воды (от 48 до 78 кВт∙ч) [9].
«Углеродный след» получения водорода в ЕС
В технологиях пиролиза метана не образуются «прямые» выбросы диоксида углерода (рис. 3), а «косвенные» выбросы зависят от «углеродного следа» поставок природного газа и электроэнергии (сетевой или возобновляемой), используемых в процессе.
При этом технологически обусловленные минимальные фугитивные выбросы метана при добыче и транспортировке природного газа, могут быть потенциально компенсированы с помощью специальных мер (например, лесовосстановления), а использование возобновляемого электричества позволит значительно снизить «углеродный след» получения водорода методом пиролиза метана.
Производство оборудования, транспортировка, а также эксплуатация и восстановление катализаторов играют второстепенную роль.
По экспертной оценке, выполненной Техническим университетом Мюнхена (TUM), пиролиз метана демонстрирует «углеродный след» в диапазоне 2,1–5,2 кг CO2экв. на 1 кг полученного водорода с учетом усредненного для ЕС «углеродного следа» поставок природного газа (рис. 4).
При использовании сетевого электричества в качестве источника энергии пиролиз метана имеет преимущества в части «углеродного следа» по сравнению с электролизом воды из-за низкого потребления электрической энергии. При этом удельные выбросы углекислого газа при электролизе воды и плазменном пиролизе с использованием возобновляемого электричества (фотовольтаики) сопоставимы.
В зависимости от способов (сжиженный природный газ, трубопроводный газ) и маршрутов «углеродный след» поставок природного газа в ЕС может достигать значения 25 г СО2экв. /МДжLHV. Для российских трубопроводных проектов «Северный поток», «Северный поток‑2», «Турецкий поток» «углеродный след» поставок газа оценивается в пределах 6,3–7,3 г СО2экв. /МДжLHV – это одни из самых минимальных значений для возможных маршрутов поставок природного газа до границы с ЕС [11].
низкоуглеродного водорода из российского природного газа
С учетом транспортировки газа по новым российским газопроводам и использования возобновляемых источников энергии (ветра и солнца) «углеродный след» получения водорода, например, плазменным пиролизом метана, в районе точки выхода газопровода «Северный поток» оценивается всего в 1,2–1,6 кг СО2экв. на 1 кг водорода 2.
Таким образом, водород, получаемый пиролизом метана, по критерию углеродоемкости соответствует низкоуглеродному водороду согласно опубликованной водородной стратегии ЕС, а также проектным параметрам для устойчивых инвестиций [12] и является одним из эффективных решений для достижения краткосрочных и долгосрочных климатических целей ЕС.
Побочный углерод в твердой форме – ценный продукт
При пиролизе метана технологический процесс обеспечивает производство углерода в твердой форме – так называемого технического углерода. На один килограмм водорода, как правило, образуется около 3‑х килограммов углерода, при этом существует возможность получения ценных продуктов, например, синтетического графита, графена, фуллеренов, углеродных нанотрубок, использование которых имеет перспективы в электротехнике, электронике, строительстве, машиностроении и др. В отличие от диоксида углерода в газообразной форме, твердый углерод легко хранить. Отдельным перспективным направлением углеродных материалов выступает адсорбционное хранение газов. Таким образом, производство твердого углерода позволяет не только снизить прямые выбросы диоксида углерода, но и создать новые рыночные возможности [10].
Если водород, производимый сегодня в мире, получать пиролизом метана, то образование твердого углерода составило бы порядка 200 миллионов тонн в год. При этом были бы исключены «прямые» выбросы диоксида углерода при производстве водорода, а сокращение выбросов парниковых газов с учетом «углеродного следа» составило бы 700–900 миллионов тонн СО2экв в год . Кроме того, использование углеродного материала вместо традиционного угля позволило бы предотвратить выбросы парниковых газов угольной отрасли при добыче и транспортировке. Указанные преимущества могут оказаться актуальными для сталелитейной промышленности. По данным [14], три тонны твердого углерода, получаемого в качестве побочного продукта при пиролизе метана, могут заместить 3,7 тонны коксующегося угля. Другие доступные рынки углерода в мире и приблизительные их объемы представлены на рис. 6.
Прогнозируемый темп роста рынка графена оценивается в 38,7 % в год. Ожидается, что к 2027 году мировой рынок графена достигнет 1,08 млрд долларов США [15].
Пиролиз метана имеет преимущества с экономической точки зрения. При оценочных затратах на производство 1 килограмма водорода 1,36–1,79 $ (в зависимости от типа процесса) с учетом коммерческой реализации углерода, пиролиз метана конкурирует с электролизом (4,61–14,87 $ / кг h3) и паровым риформингом (1,03–2,16 $ / кг h3) [16]. Водород, производимый пиролизом метана, отличается наименьшей стоимостью среди низкоуглеродного и возобновляемого водорода и может стать важной частью будущей «циркулярной экономики» ЕС.
Вызовы водородной экономики
В истории человечества уже были случаи, когда химические вещества (соединения), которые выбрасывались в атмосферу в результате хозяйственной деятельности, в будущем приводили к неожиданным экологическим проблемам.
Транспортный сектор и местное загрязнение воздуха, производство галокарбонов (например, хлорфторуглерода) и глобальное разрушение озонового слоя – серьезность этих проблем стала понятна только после того, как были внедрены промышленные технологии. Учитывая растущий интерес к водородной экономике, сейчас самое время корректно оценить ее экологические последствия, для предотвращения возможных экологических проблем.
Атмосфера Земли содержит в общей сложности ~175 тераграмм водорода (175 млн тонн) или 0,5 ppm, который влияет на глобальную химию атмосферы – поглощает один радикал OH и высвобождает один радикал HO2 (плюс водяной пар). Учитывая, что радикал OH является первичным поглотителем метана, сокращение его (радикала ОН) содержания в атмосфере будет способствовать увеличению содержания в атмосфере метана [17]. Таким образом, водород является косвенным парниковым газом.
По оценкам [17], учитывая время жизни водорода в атмосфере равное ~2 годам, утечки водорода в размере ~100 млн тонн в год увеличат содержание его в атмосфере на ~200 млн тонн, что, в свою очередь, будет способствовать увеличению глобального среднего содержания метана в атмосфере на 4 %. Такое повышение концентрации метана в атмосфере соответствует климатическому воздействию, вызванному выбросами CO2 современной авиацией.
Еще одним экологическим вызовом водородной экономики является возможное нарушение круговорота воды и снижение устойчивости биосферы. При масштабном применении электролиза воды для производства возобновляемого водорода потребуются огромные объемы специально подготовленной воды. По данным IRENA [18] для обеспечения декарбонизации глобальное потребление возобновляемого водорода должно быть на уровне 160 млн тонн к 2050 году, что потребует 7500 ТВт∙ч электрической энергии и около 3 миллиардов тонн воды . Использование воды в процессах электролиза в одних регионах (производителях водорода) и выбросы воды (водяного пара) при использовании этого водорода в других (потребителях водорода), может негативным образом отразиться на экологической обстановке этих регионов.
Заключение
В свете вышеприведенных фактов при развитии водородной энергетики важно соблюдать принцип технологической нейтральности, исходить не из геополитических предпочтений и модных трендов, а из экономической целесообразности. Внедрение дискриминационных механизмов, направленных против водорода, получаемого из природного газа в соответствии с требованиями углеродоемкости процессов, может привести к экономически неэффективной политике декарбонизации экономики, а также увеличению выбросов парниковых газов.
Необходимо в первоочередном порядке качественно и в полной мере оценить возможные риски перехода к водородной экономике в целях недопущения в будущем негативных экологических последствий, снижения уровня жизни населения, угроз здоровью.
При трансформации энергетических моделей необходимо учитывать, что в настоящее время в большинстве случаев не исчерпан потенциал природного газа для устойчивого, в том числе низкоуглеродного развития экономики.
Использованные источники
- IEA. The Future of Hydrogen. Report prepared by the IEA for the G20, Japan. – URL: https://www.iea.org/reports/the-future-of-hydrogen
- Аксютин О.Е. и др. Метан, водород, углерод: новые рынки, новые возможности. Нефтегазовая вертикаль, №1-2/2021.
- European Commission. Communication from the Commission to the European Parliament, the Council, the European economic and social committee and the committee of the regions. A hydrogen strategy for a climate-neutral Europe. Brussels, 8.7.2020. COM(2020) 301 final. – URL: https://ec.europa.eu/energy/sites/ener/files/hydrogen_strategy.pdf
- Bundesministerium für Wirtschaft und Energie (BMWi). Die Nationale Wasserstoffstrategie. – URL: https://www.bmwi.de/Redaktion/DE/Publikationen/Energie/die-nationale-wasserstoffstrategie.html
- Информационные бюллетени по материалам представительства ПАО «Газпром» в Королевстве Бельгия в г. Брюсселе.
- Энергетическая стратегия Российской Федерации на период до 2035 года.
- European Clean Hydrogen Monitor 2020, Hydrogen Europe.
- Energy Briefing «Gas, Power, Renewables and Energy Futures». Session VI: Europe`s Emerging Hydrogen Ambitions: What does it mean for Russia, IHS Markit.
- Hydrogen and hydrogen-derived fuels through methane decomposition of natural gas – GHG emissions and costs. Sebastian Timmerberg, Martin Kaltschmitt, Matthias Finkbeiner. Energy Conversion and Management: X 7 (2020) 100043.
- Ishkov A., Romanov K., Teterevlev R., Kuhn M. Cost-effective and clean ways of producing hydrogen from natural gas. International Gas Union. International Gas, 10-2020, Industry expected to rebound in 2021.
- Life Cycle Emissions of Natural Gas Transported via TurkStream. Final Report. © thinkstep, a Sphera Company.
- Guidehouse. Hydrogen generation in Europe: overview of costs and key benefits. – URL: https://op.europa.eu/en/publication-detail/-/publication/7e4afa7d-d077-11ea-adf7-01aa75ed71a1/language-en?WT.mc_id=Searchresult&WT.ria_c=37085&WT.ria_f=3608&WT.ria_ev=search
- Life Cycle Assessment and Water Footprint of Hydrogen Production Methods: From Conventional to Emerging Technologies. Andi Mehmeti, Athanasios Angelis-Dimakis, George Arampatzis, Stephen J. McPhail, Sergio Ulgiati. Environments 2018, 5, 24; doi:10.3390/environments5020024.
- Hydrogen production using methane: Techno-economics of decarbonizing fuels and chemicals. Brett Parkinson, Mojgan Tabatabaei, David C. Upham, Benjamin Ballinger, Chris Greig, Simon Smart, Eric McFarland. International Journal of Hydrogen Energy. Volume 43, Issue 5, 1 February 2018, Pages 2540-2555.
- URL: https://www.grandviewresearch.com/press-release/global-graphene-market
- Parkinson B., Balcombe P., Speirs J. F., Hawkes A. D., Hellgardt K. Levelized cost of CO2 mitigation from hydrogen production routes. Energy & Environmental Science 12 (2019), Nr. 1, S. 19–40 – Überprüfungsdatum 2019-08-22.
- An Environmental Experiment with h3? Michael J. Prather. www.sciencemag.org SCIENCE VOL 302.
- IRENA (2020), Global Renewables Outlook: Energy transformation 2050.
Плазма выделила аммиак из смеси воды и азота на радость «зеленым» химикам. Апробированный учеными метод не требует ни нагрева, ни повышенного давления — нужны только вода и электрический разряд над ее поверхностью — Наука
Аммиак можно назвать одним из важнейших для человечества веществ: он является основой для производства азотных удобрений. Использование азотных удобрений позволило повысить урожайность растений в несколько раз по сравнению с началом XX века; кроме того, аммиак нужен при производстве массы иных веществ, от соды до взрывчатки, и выступает в качестве теплоносителя для промышленных холодильников. Столь массовое использование этого вещества стало возможным благодаря открытию в начале XX столетия синтеза аммиака из водорода и азота — процесса Габера.
Процесс Габера, заключающийся в нагреве смеси газов под давлением и в присутствии катализатора из железа, используется по сей день, поскольку он достаточно дешев и прост. Первый завод по производству аммиака этим методом запустили в Германии еще до начала Первой мировой войны. Но чем больше требуется аммиака, тем выше суммарные затраты на его производство и тем больший эффект может дать оптимизация — например, отказ от необходимости греть смесь до высокой температуры или возможность обойтись без повышенного давления.
Химический реактор, построенный для синтеза аммиака в 1921 году. После окончания работы установлен как памятник в университете Карлсруэ; стенки реактора рассчитаны на давление в сто атмосфер. Drahkrub / wikimedia commons / CC BY-SA 3.0
Работы в этом направлении ведутся разными группами химиков и технологов по всему миру, и исследователи из университета Кейс-Вестерн в США представили в журнале Science Advances один из возможных подходов. Они описали способ, который не требует ни нагрева всей емкости до сотен градусов Цельсия, ни создания повышенного давления — требуется только вода и электрический разряд над ее поверхностью.
Электрический разряд создает плазму, в которой ионизированный азот и водород из подвергаемой электролизу воды создают молекулы аммиака. Протекающий ток при этом сравнительно невелик, а самое главное, отпадает нужда в катализаторе. Впрочем, наряду с достоинствами потенциальный новый метод имеет и ряд недостатков: пока что он выдает очень мало газа и потребляет очень много электричества.
В экспериментах, которые провели химики, количество полученного газа исчислялось считанными миллиграммами. Этого, безусловно, мало для промышленного применения, но сами авторы и не ставили цели сразу представить прототип химического реактора для массового производства. Они указывают, что их данные показывают на принципиальную возможность реакции, протекающей в компактной установке и дающей достаточно чистый продукт. «Требуются дополнительные исследования для оптимизации процесса. Но сопоставление нашего метода с другими аналогичными разработками указывает на то, что возможна разработка технологии распределенного и экологически чистого производства аммиака», — пишут ученые в завершающей части своей работы.
Вторая большая проблема, с которой столкнулись исследователи, в том, что переход от стандартного процесса Габера к электроплазменной технологии сам по себе должен привести к увеличению затрат энергии на синтез аммиака. Сейчас на килограмм аммиака в процессе Габера тратится около десяти киловатт-часов, а собранная учеными установка потребовала бы (с учетом масштабирования) более 2 000 КВт × час, что очень много, даже с учетом возможной оптимизации.
Однако для промышленного применения аммиак мало синтезировать. Его необходимо как-то доставить в нужное место, а это не только затраты, но и риски: аммиак — это ядовитый газ, поэтому его нельзя перекачивать или возить в цистернах с той же легкостью, что и жидкие нефть или бензин. Трубопроводов для аммиака в мире насчитывается гораздо меньше, чем нефте- или газопроводов, в том числе из-за жестких требований безопасности. Например, по российским правилам, все живущие ближе 2,5 километра от аммиакопровода должны быть проинструктированы на случай утечек (которые, кстати, случались в минувшие годы и приводили к эвакуации целых сел).
Самый длинный в мире аммиакопровод проходит из российского Тольятти в украинскую Одессу, где аммиак перегружают на специальные суда. На нем дважды с момента запуска в 1981 году происходили небольшие утечки, хотя обе обошлись без значительных последствий. Антон Оболенский / wikimedia commons / CC BY-SA 2.5
Возможность получать аммиак рядом с местом его использования может, как считают исследователи, сделать химическое производство проще, безопаснее и дешевле за счет отказа от сложных и небезопасных систем для транспортировки и хранения. В пресс-релизе университета авторы сообщают, что им удалось преодолеть другую проблему, которая долгое время преследовала химиков, работающих над нестандартными методами синтеза аммиака: их реактор давал практически чистый аммиак без примеси водорода. А что касается высокого энергопотребления, то «учитывая растущую доступность возобновляемой энергии, это может вовсе не быть принципиальным ограничением», добавляет Мохан Санкаран, один из соавторов новой публикации.
Получение водорода с СВЧ и ВЧ разрядах
Как ранее было указано, электрохимическая реакция присоединения электрона к иону водорода требует некоторой энергии активации, т. е. для того, чтобы процесс разряда ионов водорода шел на электроде с определенной скоростью, необходимо сообщить ему некоторый избыточный (против равновесного) потенциал, который определяется величиной перенапряжения водорода. Потенциал разряда водородных ионов с определенной скоростью к равен сумме равновесного потенциала водородного электрода и величины перенапряжения водорода, обозначаемой г]. Под величиной перенапряжения водорода понимают сдвиг потенциала катода при данной плотности тока 1п в отрицательную сторону по сравнению с потенциалом водородного электрода в том же растворе, в тех же условиях, но при отсутствии тока в системе. Поэтому расход электрической энергии на получение водорода электролизом больше, чем это определяется термодинамическими подсчетами. [c.42]Атомы водорода, полученные при разряде в молекулярном водороде, смешивали с избытком кислорода в потоке инертного газа при O33 К- При этом протекали реакции по уравнениям [30J [c.39]
Плазмохимические методы. Получение водорода методом СВЧ- и ВЧ-разрядов [c.420]
В противоположность прямому термическому разложению водяного пара при температуре примерно 3000 К разложение воды в низкотемпературной плазме протекает за счет термически неравновесного взаимодей- ствия электронов плазмы с молекулами воды или при разложении диоксида углерода на оксид углерода и кислород с молекулами диоксида углерода. Получение водорода в плазме (в СВЧ- и ВЧ-разрядах) представляет интерес в первую очередь по той причине, что удельная производительность химических процессов в разряде чрезвычайно велика. [c.421]
Перспективны методы получения водорода в ВЧ- и СБЧ-разрядах (низкотемпературная плазма), интенсивно разрабатываемых советскими исследователями. [c.422]
Многообразие и надежность современных методов изучения особенностей протекания электрохимических реакций дали возможность установить механизм и кинетические характеристики наиболее важных электродных процессов, связанных с получением водорода, кислорода, других газо образных продуктов, с протеканием электрохимического синтеза ряда соединении, катодного выделения и анодного окисления металлов, совместным разрядом ионов, а также с явлениями самопроизвольного растворения металлов (коррозионные процессы). [c.139]
Табл. 45, несмотря на ее неполноту, правильно отражает содержание основных представлений о возможных стадиях реакции электрохимического выделения кислорода. По I варианту образование молекулярного кислорода совершается рекомбинацией его атомов, полученных после разряда одновалентных ионов кислорода О , а по варианту II — в результате распада высшего неустойчивого окисла МОж+ь возникшего из низшего устойчивого окисла МО после разряда на нем ионов О». Вариант III исключает участие в электродном процессе каких бы то ни было заряженных частиц, кроме ионов гидроксила. Выделение кислорода происходит здесь через промежуточные стадии образования и распада гидратов окислов и окислов металла. В IV варианте непосредственным источником кислорода являются его молекулярные ионы Oj», образовавшиеся из гидратированных ионов 0 -Н20 после отнятия от них воды. Эти гидратированные ионы кислорода можно рассматривать так же, как отрицательно заряженные молекулы перекиси водорода [c.387]
Основным продуктом электролиза на аноде является хлор, получающийся при разряде ионов хлора. Катодный процесс различается в зависимости от материала катода если применяется твердый (обычно железный) катод, тогда на нем выделяется молекулярный водород, оставшиеся ионы гидроксила дают около катода щелочь если применяется жидкий ртутный катод, на котором разряд ионов водорода затруднен, идет разряд ионов щелочного металла с образованием соответствующей амальгамы, которая потом, в другом аппарате, может использоваться для разложения воды с получением водорода и щелочи, или для других целей. [c.49]
Активные частицы, получающиеся в газофазных реакциях, могут быть выморожены на охлажденных поверхностях с целью накопления и детального изучения их спектров ЭПР. Таким образом удалось получить фенильный радикал [16] при реакции атомов водорода, полученных при разряде, с бензолом [c.13]
Полученные результаты, наряду с данными по кинетическому анализу рассмотренных выше реакций, протекающих в разрядах, можно использовать также при получении в разряде соединений, меченных редкими изотопами водорода, углерода, азота и кислорода. [c.79]
Из данных по изучению объемной рекомбинации атомов водорода, полученных в разряде, следует ( ), что [c.174]
Разложение метана в искровом разряде. Свойство метана разлагаться на элементы при действии высокой температуры используется в промышленности для получения водорода и чистого углерода (сажи) из природных газов. Для демонстрационного опыта разложения метана удобно воспользоваться искровым электрическим разрядом. [c.71]
Ацетилен может быть получен воздействием разряда не только на газообразные углеводороды, но и на жидкие. При разложении жидких углеводородов газообразные продукты разложения очень мало времени находятся в горячей зоне, что способствует сохранению образующегося ацетилена без его дальнейшего разложения на водород и сажу. Таким образом, условия реакции разложения ацетилена, характерные для [c.89]
По формуле (19) из опытных данных по измерению р1 [47] можно вычислить относительные значения величины е для разных материалов при данной температуре. Оказывается, что полученные таким образом результаты совпадают с данными по измерению эффективности этих же поверхностей по отношению к рекомбинации атомов водорода, полученных 1в разряде. Это можно считать еще одним подтверждением положения о том, что основным активным промежуточным веществом при горении водорода являются именно атомы водорода. [c.51]
Понятие перенапряжение связано с избыточным напряжением, которое необходимо приложить сверх электродвижущей силы системы в равновесных условиях для проведения процесса электролиза с определенной скоростью. Расход электрической энергии на получение водорода поэтому больше, чем это определяется термодинамическими подсчетами. Это добавочное напряжение обеспечивает в данных условиях определенную скорость разряда водородных ионов с последующим образованием и выделением пузырьков водорода. [c.37]
Кальций, как и другие щелочные и щелочноземельные металлы, не может быть получен из водных растворов, так как потенциал выделения водорода выше потенциала выделения кальция, и ионы водорода разрядятся раньше, [c.385]
Эти общие заключения о природе перенапряжения на разных металлах подтверждаются в общих чертах соответствием между наиболее важными следствиями из теории перенапряжения водорода и данными, полученными при экспериментальном изучении кинетики выделения водорода. Так, на поверхности ртути в области потенциалов катодного выделения водорода ни одним из методов не удается обнаружить заметных следов адсорбированного атомарного водорода. Следовательно, стадия его удаления не является лимитирующей. Предлогарифмический коэффициент Ь на ртути близок к 0,12. При учете ничтожно малого заполнения поверхности ртутного катода адсорбированным атомарным водородом такое значение величины Ь не может быть получено из теории замедленной рекомбинации. Экспериментальные данные по влиянию состава раствора и pH на перенапряжение при выделении водорода на ртути также лучше всего согласуются с предположением о замедленности разряда на свободных участках катода. [c.413]
Для получения струи плазмы в целях резки используется газоразрядное устройство, называемое плазмотроном, где рабочий газ (водород, азот, аргон, гелий или их смеси) превращается в плазму в дуговом разряде между электродами [ 36 ]. [c.117]
Химические реакции в тлеющем разряде. Получение атомного водорода и других свободных радикалов [c.241]
Показано, что атомарный водород, полученный в электрическом разряде, полностью восстанавливает уголь и даже коронен до смеси метана, этилена и ацетилена. Парафины, фенантрен и пирен образуют также высокомолекулярные остатки, богатые гидроароматическими соединениями. В присутствии воды процесс ускоряется, образуются окислы углерода Изучены массонеренос при размешивании пасты и влияние размешивания на процесс гидрогенизации угля. На размешивание не влияет отношение водород [c.23]
Содержание дейтерия в природном водороде составляет 0,02%. Впервые он был получен в значительных количествах в виде тяжелой воды ОгО путем электролиза природной воды. При электролизе воды разряд Н+ происходит значительно быстрее, чем 0+, [c.464]
Атомарный водород образуется а) при получении водорода in statu nas endi (в момент выделения) б) при термической диссоциации молекулярного водорода в) под действием электрических разрядов г) в вольтовой дуге при прохождении молекулярного водорода между электродами дуги д) при облучении светом, [c.19]
Интересно сопоставигь результаты наших вычислений с данными Смита ( ), изучавшего рекомбинацию атомарного водорода, полученного в разряде, на различных поверхно-дс7о данным этого автора, гн на чистом пирексе при 457 равно 8 10 . Поскольку указания об особом проплавлении материала Смит не дает, то, полагая, что он работал с обычным сосудом, можно объяснить расхождение с нашими данными, тем более, что, как мы указывали выше, даже в одинаковых сосудах из проплавленного пирекса значение p может отличаться в несколько раз. Более интересно поэтому сравнить данные, относящиеся к стеклу, обработанному солями, хотя при этом остается некоторая неопределенность в характере обработки. Так, для пирекса, обработанного раствором ка, Смит дает значение гн =2-10- (при 477°), что находится в согласии с приведенным выше значением. [c.52]
Высокая энергонапряженность неравновесных плазмохимических систем и большая скорость газовых потоков через разряд определяют большую удельную производительность и, следовательно, низкую металлоемкость и оптимальные мессогаба-ритные характеристики плазмохимических реакторов. В этом отношв11ии в рамках атомно-водородной энергетики ллазмохимические методы получения водорода особенно интересны. По энергетической эффективности они близки к другим электри- [c.65]
Несмотря на особую важность ллазмохимических методов получения водорода в решении ряда прикладных задач, экспериментальные исследования этого вопроса сравнительно малочисленны. До последнего времени они были главным образом связаны с разложением углеводородов в тлеющем разряде и характеризовались чрезвычайно низкой энергетической эффективностью. Более высокая эффективность была достигнута в экспериментах по прямому разложению Н2О в тлеющем и СВЧ-разрядах (см. ниже). [c.66]
Рассмотрим далее энергетическую эффективность описанного процесса разложения воды и получения водорода. Полный КПД процесса (Т ) определяется потерями энергии в разряде r gy на непроизводительные каналы возбуждения, эффективностью хим связанной с потерями в прямых экзоэргических и обратных реакциях, и, наконец, эффективностью Т] /т реакции по отношению к колебательной релаксации. [c.67]
Наряду с проведенным кратким сравнительным анализом различных разрядных схем следует заметить, что пока еще нельзя выделить конкретный тип разряда, в котором оптимальные условия протекания плазмохимических реакций реализуются наиболее просто. Тот факт, что наилучшие показатели по энергетической эффективности достигнуты в СВЧ-разрядах умеренного давления, еще не доказывает их исключительность, в особенности если речь идет о мощностях, превышающих 100 кВт. Возможно даже, что для каждого конкретного плазмохимического процесса придется создавать индивидуальные газоразрядные системы с оптимальными именно для этого процесса характеристиками. Тем не менее уже сейчас можно предположить, что организация в неравновесной плазме химических процессов, стимулируемых колебательным возбуждением реагентов электронами плазмы, позволяет при энергетической эффективности до 80% достигать производительности до 10 м /ч газа-продукта с 1 см активного объема плазмы. Такие характеристики эндоэргических процессов (в первую очередь получения водорода и окиси углерода), особенно по удельной производительности, намного превышают показатели альтернативных методов и позволяют решать с помощью нёравновес-ной плазмохимии ряд важных задач атомно-водородной энергетики и металлургии. [c.84]
При электроанализе определяют массу осадка, образовавшегося на электроде в результате протекания количества электричества, достаточного для полного, илн практически полного, выделения данного вещества. Образование осадка может происходить ири этом на катоде (разряд металлических ионов с выделением металла) илн на аноде (разряд анионов с образованием соответствующих солей или оксидов). Если химический состав осадка известен, нетрудно по его массе рассчитать содержание определяемого вещества в исходном растворе. Так как количество электричества, пошедшее на получение осадка, не входит в последующие расчеты, то при электроанализе выход по току определяемого вещества необязательно должен равняться 100%. Част(. тока может пойти на другие электродные реакции при том условии, что они пе изменят состава осадка и не нарушат его компактности и прочности сцепленит с электродом. С этой точки зрения можно допустить расход некоторой доли тока на выделение водорода или кислорода. Необходимо, однако, иметь в виду, что чем меньиге выход по току определяемого вещества, тем больше придется затратить времени на анализ. [c.284]
Присоединение адсорбированных атомов водорода как стадия, определяющая кинетику электровосстановления. По дру- ому варианту скорость процесса лсктровосстановления определяется ирисоединением адсорбироЕ.анных атомов водорода к восстанавливаемым частицам. Первой стадией в этом случае является разряд водородных ионов с получением адсорбированных атомов водорода [c.438]
В тлеющем разряде также могут протекать разнообразные химические реакции. В 1920 г. американский физик Р. Вуд получил с помощью тлеющего разряда водород. В тлеющем разряде можно синтезировать различные вещества (Н2О2, О3, N0). Предложено использовать тлеющий разряд для получения напыленных полимерных мембран [8]. Плазменной полимеризации подвергаются различные органические соединения. Используется как электродная, так и безэлектродная форма разряда (разряд, протекающий в стеклянной трубке, помещенной внутри соленоида, питаемого от ВЧ-генератора). Образующийся полимер осаждается на пористой подложке в зоне тлеющего разряда. [c.175]
То же относится и к химическим процессам. Взаимодействие водорода и кислорода с образованием воды может происходить самопроизвольно, и осуществление этой реакции дает возможность получать соответствующее количессво работы. Но, затрачивая работу, можно осуществить и обратную реакцию — разложения воды на водород и кислород, — например, путем электролиза. И другие химические реакции, которые по своим термодинамическим параметрам не могут в данных условиях совершаться самопроизвольно, можно проводить, затрачивая работу извне. Большей частью это осуществляют или путем электролиза, или при электрическом разряде в газах, или действием света, или же путем повышения давления (причем одновременно изменяются и условия проведения реакции). Из хорошо известных процессов такого рода можно назвать фотосинтез в растениях, получение натрия и хлора путем электролиза расплавленного хлористого натрия, получение металлического алюминия из бокситов путем электролиза, синтез аммиака при высоком давлении и др. [c.209]
Один из наиболее употребительных методов получения атомов Н — это метод электроразряда. Как было показано Вудом [596], в тлеющем разряде в водороде при даилении 0,1 — 1 тор получается высокий процент атомарного водорода. Метод Вуда в настоящее время широко применяется для получения атомных газов. [c.31]
Для получения алифатических радикалов иногда применяется следующий вариант электроразрядного метода непосредственно в электрическом разряде (в водороде) получаются атомы Н. Так как при комнатной температуре взаимодействие атомов Н с олефинами сводится практически исключительно к процессу Н + С Н2 = h3 +i, т. е. к образованию алифатического радикала, то н присутствии олефина можно получить соответствующий радикал. Свободвые радикалы могут быи. получены также фотохимическим путем. [c.35]
К Электрокрекинг, предназначенный, главным образом, для получения ацетилена и лишь частично этилена и других олефинов, впервые подробно изучен и разработан советскими учеными, показавшими его большие практические возможности. Процессы крекинга в электрической дуге не получили широкого промышленного распространения, несмотря на то, что несколько установок были построены и испытаны давно. Так, для производства ацетилена в Германии на заводе в г. Хюлье во время второй мировой войны была сооружена промышленная установка электро-крекинга метана, работавшая при температуре 1600° С и весьма ограниченном времени реакции (10 с). Мощность установки составляла 200 т ацетилена в сутки. Получаемый газ содержал 13,3% по объему ацетилена, 46 — водорода, 8,9 — азота, 2,9 — окиси углерода, 27,8% — парафинов, а также диацетилен, метилацетилен и винилацети-лен. Позднее по результатам исследований, проведенных в Техасском университете, была построена другая установка электрокрекинга в тихом разряде мощностью 7500 т ацетилена в год. В конце пятидесятых годов в Румынии была сооружена установка электрокрекинга метана, на которой выполнено большое число экспериментов. Но из-за сильного сажеобразования эксплуатация этой полузаводской установки затруднена. [c.25]
Газофазное химическое осаждение (ГФХО) является одним из наиболее эффективных методов получения различных углеродных материалов. Фазовый состав, структурные характеристики и другие свойства ГФХО пленок огтределяются условиями активации газовой смеси. В данной работе представлены результаты исследования состава газовой смеси водорода и метана, активированной разрядом постоянного тока. [c.99]
(PDF) Выделение водорода при плазменном электролизе в водном растворе
Выделение водорода при плазменном электролизе в водном растворе
Tadahiko MIZUNO
, Tadashi AKIMOTO, Kazuhisa AZUMIO
HIOR20003000, Tadayoshi, квантовой энергетики, Высшая школа инженерии, Университет Хоккайдо, Кита 13 Ниси 8, Кита-ку, Саппоро 060-8628, Япония1 Отделение молекулярных наук, Высшая школа инженерии, Университет Хоккайдо, Кита 13 Ниси 8, Кита ku, Саппоро 060-8628, Япония
2 Исследовательский центр катализа, Университет Хоккайдо, Кита 11 Ниси 10, Кита-ку, Саппоро 060, Япония
3Центр перспективных исследований энергетических технологий Университета Хоккайдо, Кита 13 Ниси 8, Кита ku, Саппоро 060-8628, Япония
4 Кафедра ядерной инженерии, Высшая инженерная школа, Университет Осаки, 2-1 Ямадаока, Суита, Осака 565-0871, Джапа №
(Поступила 26.01.2004; принято 4 октября 2004 г .; опубликовано 11 января 2005 г.)
В последнее время водород привлекает внимание как возможное решение экологических и энергетических проблем.Если водород должен быть
,считается средством хранения энергии, а не природным ресурсом. Однако свободного водорода на Земле не существует. Было предложено множество способов получения водорода
. Его можно переформулировать из обычного углеводородного топлива или
, полученного непосредственно из воды путем электролиза или высокотемпературного пиролиза с использованием источника тепла, такого как ядерный реактор.
Однако эффективность этих методов невысока. Непосредственный нагрев воды до достаточно высоких температур для поддержания пиролиза
очень труден.Пиролиз происходит, когда температура превышает 4000C. Таким образом, плазменный электролиз может быть лучшей альтернативой
, его не только легче достичь, чем прямое нагревание, но он также дает больше водорода, чем обычный электролиз
, как предсказывается законами Фарадея, что является косвенным свидетельством того, что он дает очень высокую температуры. Мы также наблюдали
большого количества свободного кислорода, образовавшегося на катоде, что является дополнительным свидетельством прямого разложения, а не электролитического разложения
.Для достижения непрерывного производства водорода с эффективностью, превышающей эффективность Фарадея,
, необходимо контролировать состояние поверхности электрода, температуру плазменного электролиза, плотность тока и входное напряжение
. Минимальное входное напряжение, необходимое для индукции состояния плазмы, зависит от плотности и температуры раствора,
в данном исследовании было оценено как 120 В. Самая низкая температура электролита, при которой образуется плазма, составляет -75 ° C. У нас есть
, наблюдается в 80 раз больше водорода, генерируемого при плазменном электролизе, чем при обычном электролизе при
300 В.[DOI: 10.1143 / JJAP.44.396]
КЛЮЧЕВЫЕ СЛОВА: плазменный электролиз, генерация водорода, эффективность тока, пиролиз
1. Введение
Количество водорода и кислорода, образующихся при электролизе
, предсказывается законом Фарадея. При стандартных условиях
при 298 К, 1: 013 105 Па, 0,116 см3CÀ1
водорода и 0,0581 см3CÀ1 кислорода. Если температура
превышает 4000 ° C, может произойти пиролиз, и количество образующегося водорода
превысит количество
, предсказанное законом Фарадея.
1,2)
Реакция тлеющего разряда возникает при электролизе
в растворе при высоком входном напряжении (100 В или на
больше).
3–9)
Плазма образуется на поверхности электрода.
Слой смешанного водорода, кислорода и пара образуется на
поверхности катода. Если температура и плотность тока
верны, может наблюдаться генерация водорода сверх того, что предсказывается законом Фарадея
.Однако даже при соблюдении этих условий
регулирование количества образующегося водорода
все еще очень сложно.
Разработан метод получения эффективного водорода
. Сообщалось об аномальном образовании водорода
и продуктах плазменного электролиза. Когда напряжение
выше 140 В подавалось на межэлектроды в электролите
при высоких температурах, легко достигалось плазменное состояние
.Многие исследователи подтвердили образование
различных химикатов с помощью плазменного электролиза.
10,11)
Там было
обширное обсуждение механизма генерации
продуктов.
12,13)
Сообщалось, что температура
достигает 9000 К, а давление достигает 4000 атм, когда
плазма образуется при нескольких сотнях вольт.
14)
Для определения текущей эффективности производства водорода
необходимо оценить тепловой баланс.Однако на входе
напряжение и ток значительно колеблются, и
сложно измерить выходной тепловой баланс во время плазменного электролиза. Измерение потерь тепла из ячейки и температуры жидкости
относительно просто, но измерение энтальпии отходящего газа
, который представляет собой смесь водорода, кислорода и пара
, очень сложно. Точное измерение
до сих пор не проводилось. Измерение
усложняется тем фактом, что количество образующегося газа не может быть оценено на основе входного тока
(как это может быть при обычном электролизе
), потому что должна быть включена порция, произведенная пиролизом
.Для определения энтальпии необходимо, чтобы
точно измерили фактическое количество водорода, смешанного с
потоком газа.
2. Эксперимент
2.1 Электролизная ячейка
На рисунке 1 показана схема ячейки и измерительной системы
. Ячейка изготовлена из стекла Pyrex, имеет диаметр
10 см, высоту 17 см и емкость 1 литр. Крышка ячейки
изготовлена из Te fl на резине, диаметром 7 см и несколькими отверстиями
.Самое большое отверстие находится в центре, куда вставляется стеклянная воронка
, закрывающая катод. Также имеется вентиляционное отверстие для отходящего газа
из анода, входные и выходные отверстия для трубки
Tygon, по которой охлаждающая жидкость проходит через ячейку, отверстие
для ввода анодного подводящего провода и три других отверстия для
.платиновых резистивных датчика температуры (RTD). ТДС
измеряют температуру электролита. Они размещаются на расстоянии
3 см от стенки ячейки, достигая глубины 3, 6 и 9 см, чтобы
измеряли температуру в разных точках раствора.
Непрерывно измеряли температуру на трех глубинах.
Никакой значительной разницы температур между тремя точками
не наблюдалось, потому что раствор хорошо перемешивается
во время электролиза с использованием магнитной мешалки.
Адрес электронной почты: [email protected]
Японский журнал прикладной физики
Vol. 44, No. 1A, 2005, pp. 396–401
# 2005 Японское общество прикладной физики
396
Произошла ошибка при настройке пользовательского файла cookie
Этот сайт использует файлы cookie для повышения производительности.Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка вашего браузера для приема файлов cookie
Существует множество причин, по которым cookie не может быть установлен правильно. Ниже приведены наиболее частые причины:
- В вашем браузере отключены файлы cookie. Вам необходимо сбросить настройки своего браузера, чтобы он принимал файлы cookie, или чтобы спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает вас, хотите ли вы принимать файлы cookie, и вы отказались.Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файлы cookie.
- Ваш браузер не поддерживает файлы cookie. Если вы подозреваете это, попробуйте другой браузер.
- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г., браузер автоматически забудет файл cookie. Чтобы исправить это, установите правильное время и дату на своем компьютере.
- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie.Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу. Чтобы предоставить доступ без файлов cookie потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в cookie; никакая другая информация не фиксируется.
Как правило, в файлах cookie может храниться только информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта. Например, сайт не может определить ваше имя электронной почты, пока вы не введете его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступа к остальной части вашего компьютера, и только сайт, который создал файл cookie, может его прочитать.
Производство богатого водородом синтез-газа импульсной атмосферной плазмой, погруженной в смесь воды с этанолом
Фотография импульсного разряда постоянного тока в смеси воды с этанолом представлена на рис.2.
Рис. 2Импульсный разряд постоянного тока в смеси этанол – вода
Было обнаружено, что производство газа начинается и прекращается практически мгновенно при включении и выключении плазмы. Кратковременная задержка (около 1 мин) в производстве водорода на графике представлена временем, необходимым для повышения давления и вытеснения окружающего воздуха над раствором газообразным продуктом конверсии. Производство газа контролировалось ротаметром и независимо проверялось путем зажигания стабильного пламени на выходном сопле.Возрастающее содержание водорода, измеренное детектором водорода в добываемом газе, как функция времени процесса, показано на рис. 3 вместе с соответствующими значениями температуры в электролите. Видно, что образование большого количества водорода начинается быстрее, чем рост температуры. Изображение пламени с содержанием водорода 50% показано на вставке на рис. 3. Значения объема водорода, полученные HY-Alerta, были подтверждены независимыми измерениями на образцах, транспортируемых мешками для отбора проб газа Tedlar ® в хранилище. газовый хроматограф.Максимальное содержание насыщенного водорода, полученное в описанных выше экспериментальных условиях, составляло 60%. Соответствующие данные, полученные с помощью газового хроматографа: 60% H 2 , 22,5% CO, 4,6% CO 2 и 2,5% метана.
Рис. 3Объем водорода в полученном газе и соответствующая температура электролита в зависимости от времени. На вставке показано пламя с 50% водорода в потоке добываемого газа 250 куб. Наружный диаметр сопла с пламенем 3 мм
В оптическом излучении разряда наблюдались и контролировались следующие линии и полосы: атомные линии водорода H α (переход 2–3, λ = 656.3 нм), H β (переход 2–4, λ = 486,1 нм) и H γ (переход 2–5, λ = 434 нм), линии атомарного кислорода (407,7, 615,7, триплет 777 нм, 821,2, 844,6 и 926 нм) и системы Ангстрема CO [(0,2), λ = 519,8 нм]. Полосы ОН в спектрах с этанолом не наблюдались. Однако следует отметить, что полосы ОН наблюдались в разряде в чистой воде.
Диссоциация молекул воды в разряде является основным образованием атомов водорода по реакции
$$ {\ text {H}} _ {2} {\ text {O}} + {\ text {e} } \ to {\ text {H}} + {\ text {OH}} + {\ text {e}} $$
(1)
Обратите внимание, что уравнение.(1) представляет собой интенсивно изучаемый процесс плазменного электролиза как более эффективную альтернативу традиционному электролизу [2, 20]. Радикалы H и OH из молекулы воды могут реагировать с этанолом — реакция с атомом водорода, т.е. образование молекулярного водорода, стимулируемое присутствием воды
$$ {\ text {CH}} _ {3} {\ text {CH} } _ {2} {\ text {OH}} + {\ text {H}} \ to {\ text {CH}} _ {3} {\ text {CH}} _ {2} {\ text {O} } + {\ text {H}} _ {2} $$
(2)
и реакция
$$ {\ text {CH}} _ {3} {\ text {CH}} _ {2} {\ text {OH}} + {\ text {OH}} \ to {\ text {CH}} _ {3} {\ text {CH}} _ {2} {\ text {O}} + {\ text {H}} _ {2} {\ text {O}}.$$
(3)
За ними может следовать
$$ {\ text {CH}} _ {3} {\ text {CH}} _ {2} {\ text {O}} + {\ text {e}} \ to {\ text {C}} _ {2} {\ text {H}} _ {5} + {\ text {O}} + {\ text {e}} $$
(4)
и
$$ {\ text {CH}} _ {3} {\ text {CH}} _ {2} {\ text {O}} + {\ text {e}} \ to {\ text { CH}} _ {3} {\ text {CHO}} + {\ text {H}} + {\ text {e}}, $$
(5)
с образованием ацетальдегида CH 3 CHO [21].Реакции и электронно-молекулярные реакции этилгруппы C 2 H 5 и ацетальдегида CH 3 CHO приводят к образованию метилена CH 2 , этилена C 2 H 4 , метильной группы CH 3 , ацетильная группа CH 3 CO и метан CH 4 . Эти соединения могут вступать в реакции, снова образуя CH 3 , винильный радикал C 2 H 3 , альдегидную группу HCO, CH 2 , OH, H 2 , радикал CH, H, CH 4 , этан C 2 H 6 , CO, O и впоследствии ацетилен C 2 H 2 , C 2 H 4 , CH 4 , CO, CO 2 , OH, H, HCO и O [21].Некоторые продукты снова входят в реакцию, а некоторые видны на выходе из реактора, например, H 2 , CO, CO 2 и CH 4 . Как сообщается, в выходящем газе могут быть небольшие количества C 2 H 4 и C 2 H 6 , например в [22], но они не были зарегистрированы методом газовой хроматографии. CO и радикалы H и O обнаруживаются в плазме с помощью оптической эмиссионной спектроскопии (OES).
Спектры оптического излучения процесса для двух частот повторения импульсов 12 и 15 кГц показаны на рис.4. Оба спектра имеют схожий характер. Чем выше частота повторения, тем выше средняя мощность, передаваемая процессу. Соотношение эмиссий двух водородных линий (здесь от 2–4 до 2–3 переходов) в неравновесной плазме экспоненциально зависит от температуры электронов [23]. Таким образом, различные отношения интенсивностей излучения H β / H α , 0,081 для 12 кГц и 0,090 для 15 кГц, соответственно, отражают увеличение температуры электронов в плазме с увеличением мощности.Помимо сильных линий водорода, в спектрах присутствует полоса системы Ангстрема СО (0,2), слабая полоса молекулярного водорода и интенсивные линии атомарного кислорода.
Рис. 4Спектры оптического излучения из погруженной плазмы в воде, смешанной с 26% этанолом, на двух частотах следования импульсной мощности
Мы полагаем, что причина, по которой радикал ОН не наблюдается в спектрах оптического излучения, заключается в его расходе в реакциях с радикалом C 2 H 5 O в соответствии с формулой.(3.) и / или диссоциация на атомы O и H после
$$ {\ text {OH}} + {\ text {e}} \ to {\ text {O}} + {\ text {H}} + {\ text {e}} \ quad [21]. $$
(6)
Измерения электропроводности и плотности электролита в ходе более длинной серии экспериментов по конверсии показаны на рис. 5. Электропроводность смеси воды с этанолом монотонно увеличивается со временем от начального значения 1 мкСм / см, что соответствует деионизированная вода, смешанная с непроводящим чистым этанолом.При этом снижается плотность смеси, что свидетельствует о снижении концентрации этанола в воде. Этот результат указывает на то, что для стабильного производства водорода в реакторе необходимо постоянно измерять содержание этанола и компенсировать его до исходного уровня. Значения pH также меняются со временем. В течение 1 ч после включения плазмы значение pH снижается с 5,7 (свежая смесь) до 4,74.
Рис. 5Временная функция проводимости и содержания этанола в смеси деионизированной воды с 99.Этанол чистотой 5% в экспериментах с погруженной плазмой
Повышенная эффективность производства водорода из метанола с использованием методологии плазмы диэлектрического барьерного разряда и проводимости морской воды в качестве электрода
Heliyon. 2020 сен; 6 (9): e04717.
Нихар Ранджан Панда
a Школа фундаментальных наук, Индийский технологический институт Бхубанешвар, Одиша, Индия
Доджалиса Саху
b Школа прикладных наук, Университет технологии и управления Центурион, Одиша,
, Индия a Школа фундаментальных наук, Индийский технологический институт Бхубанешвар, Одиша, Индияb Школа прикладных наук, Университет технологии и управления Центурион, Одиша, Индия
Поступила в редакцию 28 марта 2019 г .; Пересмотрено 30 августа 2019 г .; Принята в печать 11 августа 2020 г.
Это статья в открытом доступе под лицензией CC BY-NC-ND (http://creativecommons.org/licenses/by-nc-nd/4.0/).
Abstract
В данной работе обсуждается метод разложения метанола для получения газообразного водорода с применением плазмы. Для этого был разработан плазменный реактор простого диэлектрического барьерного разряда (ДБР) с двумя типами электродов. Плазменный реактор DBD был испытан путем замены одного из металлических электродов слабопроводящей морской водой, что дало лучшую эффективность при производстве газообразного водорода.Экспериментальные параметры, такие как; напряжение и время разряда варьировались, поддерживая разрядный промежуток 1,5 мм, и изучались разрядные характеристики плазмы. Обнаружено формирование микроразрядов нитевидного типа, которые наблюдались в виде многочисленных стримерных кластеров на осциллограмме тока. Газохроматографическое исследование подтвердило образование газообразного водорода со временем пребывания около 3,6 мин. Хотя концентрация (%) H 2 была высокой (98,1%) и соответствовала узлу медного электрода, скорость образования и концентрация оказались самыми высокими (98.7%) для водяного электрода при удельном разрядном напряжении. Энергетическая эффективность составила 0,5 моль H 2 / кВтч и 1,2 моль H 2 / кВтч для металлических (Cu) и водяных электродов соответственно. Материал электрода существенно влияет на состояние плазмы и, следовательно, на скорость образования водорода. Анализ состава воды, использованной в качестве электрода, показал минимальное изменение состава даже после завершения эксперимента по сравнению с неочищенной водой. Исследование разложения метанола показывает присутствие необработанного метанола в остатке плазменного реактора, что подтверждается спектрами поглощения.
Ключевые слова: Энергетика, Химическая инженерия, Физика плазмы, Возобновляемые источники энергии, Диэлектрический барьерный разряд, Водородная энергия, Метанол, Плазма, Водный электрод
1. Введение
Обычная энергия, вырабатываемая из ископаемого топлива, ограничена и является вспомогательной для нескольких экологические проблемы [1, 2, 3, 4, 5]. Итак, поиск альтернативных и возобновляемых источников энергии был инициирован для долгосрочного решения этой проблемы. Среди источников неисчерпаемой и устойчивой энергии солнечные, ветровые и биомассовые источники энергии в основном зависят от конкретного места, непостоянны и не обладают стабильностью [6, 7].Водород является многообещающим вариантом для энергоснабжения и считается чистым топливом, имеющим высокую энергию на единицу массы [8, 9, 10]. При сгорании он может производить высокую тепловую энергию, которая в три раза выше, чем у бензина [11]. В настоящее время это идеальный энергоноситель для использования в нефтехимической, автомобильной и химической промышленности [12]. Будущий рынок топливных элементов также будет полностью зависеть от водорода как основного источника топлива [3, 4, 5]. Он может быть образован из различных источников сырья, таких как высшие углеводороды, парниковые газы, нефтеперерабатывающие газы и возобновляемые материалы, такие как древесина, твердые органические отходы, сточные воды и спирты, полученные из биомассы [1, 2, 3, 4, 5, 6 , 7, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24].Из них метанол широко используется в качестве жидкого топлива для производства водорода с помощью различных технологий конверсии из-за высокого содержания H 2 , низкой стоимости, простоты хранения и удобной транспортировки [16, 25, 26, 27, 28 , 29, 30]. В последнее время было внедрено множество методов производства водорода, таких как поточный риформинг метанола и природного газа [20, 21, 27], частичное окисление метанола [31, 32, 33, 34], газификация угля [22], и электролиз метанол-вода [23].Выход водорода 20 мол.% Был достигнут Gondal et al. лазерным воздействием метанола в течение 90 мин [25]. Аналогичным образом Take et al. [24] сообщили о получении водорода (95–97 мол.%) Электролизом водно-метанольного раствора.
Плазменные технологии использовались для ряда приложений, таких как спектрохимия плазмы, резка, распыление, сварка, травление или осаждение тонких слоев, катализ, производство озона, очистка топливного газа и разрушение летучих органических соединений и т. Д.[35, 36, 37, 38, 39, 40, 41]. Среди различных нетепловых плазменных процессов, таких как диэлектрический барьерный разряд (DBD), коронный разряд, тлеющий разряд и скользящая дуга, плазменный процесс DBD является более стабильным и однородным и имеет множество потенциальных промышленных применений [42, 43, 44]. Исследователи в этом направлении предприняли несколько попыток для конверсии метана, этанола и метанола с помощью плазменной технологии DBD для эффективного получения газообразного водорода. Используя аналогичный метод, Wang et al.[27] сообщили о производстве водорода и обсудили это с использованием внутреннего электрода из нержавеющей стали; более длинная разрядная зона и больший разрядный промежуток были бы полезны для реакции. Исследование разложения метанола, проведенное Sarmient et al. [45] выявили влияние таких параметров, как напряжение, частота (1–6 кГц), шероховатость электрода, скорость потока и т. Д., И обнаружили усиленное разложение метанола при скорости потока менее 50 см 3 / с. Имеются сообщения о разложении метанола на водород с помощью DBD [20, 46, 47].Такие плазменные установки DBD для конверсии метанола проще в эксплуатации по сравнению с другими каталитическими процессами и широко используются.
Производительность реактора DBD существенно зависит от материалов электродов (внутреннего и внешнего). Выбор внутреннего электрода влияет на конверсию метанола и селективность продукта [27]. Сообщалось, что конверсия метанола наиболее высока для электрода из нержавеющей стали и постепенно снижается для латуни и алюминия [27]. Превращение метана в соответствии с селективностью материала электродов было изучено Xu et al.[48]. Он показывает изменение порядка; нержавеющая сталь> красная медь> латунь> алюминий. Эти отчеты свидетельствуют о значении каталитического эффекта внутренних электродов для преобразования метанола / метана с образованием H 2 . Внутренний электрод остается в непосредственном контакте с химически активным материалом, температура которого достигает 200 ° C, вызывая реакцию разложения. Материал внешнего электрода также способствует производству H 2 согласно имеющемуся отчету [48].Вышеупомянутое исследование показывает, что использование алюминиевой фольги в качестве электрода показывает превосходство по селективности H 2 (%) над железной сеткой [48].
В данной статье представлено исследование генерации высокочистого газообразного водорода с использованием простой и отечественной плазменной установки DBD, основанной как на твердой, так и на жидкой форме электродов. Была сделана попытка создать экономичный плазменный реактор DBD лабораторного масштаба и изучить характеристики разряда при производстве водорода из метанола.В основном морская вода использовалась в качестве внешнего электрода вместо металлического электрода в плазменном реакторе для изучения его эффективности в производстве водорода.
2. Экспериментальная часть
В настоящей работе был разработан коаксиальный плазменный реактор DBD с использованием различных электродных материалов, дающих две разные конфигурации. В первой конфигурации плазменный реактор состоял из медного стержня диаметром 2 мм в качестве высоковольтного электрода (внутреннего электрода), который был покрыт кварцевой трубкой толщиной 1 мм.Другая полая стеклянная трубка помещалась снаружи кварцевой трубки с разрядным промежутком 1,5 мм. Эта внешняя трубка была намотана какой-то медной металлической сеткой в качестве заземленного электрода (внешнего электрода). Во второй конфигурации слабопроводящая соленая вода с проводимостью 730 мкСм / см была помещена в стеклянную трубку в качестве внешнего электрода вместе с тем же медным стержнем в качестве внутреннего электрода. В этом случае медно-металлический беспорядок был заменен проводящей водой, собранной из Бенгальского залива недалеко от морского пляжа Пури, Одиша, Индия.Здесь к реактору присоединялась внешняя вертикальная стеклянная трубка для помещения проводящей воды в установку. Принципиальная схема указанного реактора показана на рис. Соленая морская вода действует как прозрачный заземленный электрод с погруженным в воду металлическим кольцом, обеспечивающим электрическое соединение с ним. Ghomi et al. сообщается о плазменном реакторе аналогичной конфигурации на основе диэлектрического барьерного разряда [49]. Экспериментальные параметры, поддерживаемые для вышеупомянутого эксперимента, суммированы в.
Принципиальная схема экспериментальной установки плазменного реактора DBD.
Таблица 1
Экспериментальные параметры реактора DBD.
| Напряжение (кВ) | от 1,9 до 2,4 |
| Мощность (Вт) | от 0,4 до 0,61 |
| Частота (кГц) | 9 |
| 3 9025 мм 3 | 0,744 |
| Объем метанола (мл) | 8 |
| Время (мин) | 5 |
| Объем использованного метанола | 15 мл |
| Время обработки min |
Использовался источник высокого напряжения (Модель-CTP2000K), способный обеспечивать выход биполярной синусоидальной волны с напряжением 0–30 кВ (размах) и максимальной частотой переменного тока до 20 кГц.В этом случае напряжение изменялось от 1,9 кВ до 2,9 кВ, поддерживая частоту 9 кГц. Вольт-амперные осциллограммы плазменного разряда были получены при варьировании мощности разряда. Для этого использовался цифровой осциллограф (марки Tektronix) с высоковольтным пробником. Реактор имел возможность пропускать в зону разряда как жидкости, так и газы. Для этой цели использовали метанол аналитической чистоты (M / s Merck-67-56-1). Сначала в реактор загружали метанол, а затем подавали напряжение.Предусмотрена возможность сбора газов и жидкостей после разряда.
Продуктовый газ, образующийся в процессе, собирали путем вытеснения воды вниз. Собранный газообразный водород анализировали с помощью газовой хроматографии (GC-17A, Shimadzu) с использованием колонки с молекулярным ситом 5 Å и детектора теплопроводности (TCD) для обнаружения водорода, монооксида углерода и т.д. В качестве газа-носителя использовали аргон. Высокочистый (чистота 99,9%) водород, окись углерода, пары метанола использовались для проверки чистоты продукта путем картирования площади в ГХ-анализе.Исследование разложения метанола проводили при различных напряжениях, сохраняя постоянное время пребывания, и определяли выход и чистоту водорода. Также сравнивались разрядные характеристики, полученные для обеих конфигураций электродов. Состав морской воды, используемой в качестве внешнего электрода, также проводился до и после эксперимента. УФ-видимый спектрометр (Shimadzu UV-1700) использовали для записи спектров УФ-поглощения метанола перед плазменной обработкой.Тот же эксперимент был проведен для записи спектров остатка, полученного из реактора.
3. Результаты и обсуждение
Обычно реактор DBD работает в гомогенном и нитевидном режимах при атмосферном давлении [50, 51]. В нитевидном режиме между двумя электродами случайным образом формируется большое количество микроразрядов, тогда как в однородном разряде равномерная плазма покрывает поверхность электрода. Плазменный разряд ДБР протекает в три фазы, а именно: (1) стадия пробоя (2) квазиравновесная стадия и (3) неравновесная стадия [43].Последний является наиболее эффективным для инициирования химической реакции из-за наличия электронов высокой энергии, которые могут производить возбужденные молекулы и радикалы. Когда нетепловой электрический разряд происходит между электродами в среде воздуха или кислорода, УФ-свет, ударные волны и многие химически активные вещества, такие как ионы, свободные радикалы, высокореактивные молекулы и электроны, образуются в результате диссоциации, возбуждения и ионизации молекул и молекул газа. на поверхности жидкости [53]. Сильные окислители из этих частиц, такие как ионы гидроксила и озон, образующиеся на границе раздела газ-жидкость, могут легко диффундировать в эту поверхность, что приводит к диссоциации рабочего газа / жидкости [52, 53, 54, 55].
Разложение органического соединения, такого как метанол, также представляет собой сложный физико-химический процесс при плазменной обработке. Параметры разряда и химические реакции с химически активными частицами, образующимися в разряде, в значительной степени влияют на этот процесс разложения [55]. В воздушной плазме возможны три возможных пути разложения метанола, как указано ниже (уравнения (1), (2) и (3)) [55].
CH 3 OH → · CH 2 OH + · H
(2)
CH 3 OH → · CH 3 O + · H
(3)
Как сообщалось, Энергии диссоциации C – O, C – H и O – H составляют примерно 351 кДж / моль, 414 кДж / моль и 460 кДж / моль соответственно [55].Таким образом, связь C – O сначала диссоциирует за счет реактивных частиц, образующихся плазменными струями. Затем вышеуказанные промежуточные продукты превращаются в H 2 , HCHO, HCOOH и HCOOCH 3 вместе с другими частицами плазменными струями в соответствии со следующими реакциями (уравнения (4), (5), (6), (7), (8), (9), (10), (11), (12), (13) и (14)) [56, 57, 58, 59]. Но в нашем эксперименте мы не обнаружили таких видов, как HCHO, HCOOH и CO 2 .
CH 3 OH + · OH → H 2 O + CH 2 OH ·
(7)
· CH 2 OH + · H → H 2 + HCHO
(8 )
· CH 2 OH + · OH → H 2 O + HCHO
(9)
CH 3 OH + · H → · CH 2 OH + H 2
( 10)
· CH 3 O + · H → H 2 + HCHO
(11)
H 2 + · OH → H 2 O + H ·
(14)
Эксперимент проводился путем подачи метанола в качестве рабочей жидкости в плазменный реактор DBD, подключенный к источнику высокого напряжения.Осциллограммы напряжения и тока разряда регистрировались для различных приложенных напряжений (1,9–2,9 кВ) для двух типов конфигурации электродов. Но частота и разрядный промежуток были зафиксированы на 9 кГц и 1,5 мм соответственно. а показаны формы сигналов напряжения, записанные для приложенного напряжения 2,4 кВ. Когда электрическое поле в разрядном промежутке достаточно велико, чтобы вызвать пробой, наблюдается большое количество микроразрядов. В этом случае применяемое давление воздуха составляет порядка 10 5 Па.Этот диапазон давления идеален для генерации озона, образования эксимеров, а также для обработки дымовых газов. Разряд происходит либо нитевидным, либо однородным образом по поверхности диэлектрика. В нашем случае наблюдались микроразряды нитевидного типа, которые можно увидеть в виде многочисленных стримерных кластеров на осциллограммах тока. Это изображено на b, где показана форма волны тока, записанная для приложенного напряжения 2,6 кВ для обоих типов электродов. Одиночный стримерный кластер состоит из нескольких стримеров / шипов, типичное время жизни которых составляет 50 нс [60].Они случайным образом распределены во времени и пространстве по поверхности диэлектрика и проходят в разрядном промежутке [60]. Эти стримеры или импульсы очень важны и эффективны для индукции химической реакции с повышенной скоростью реакции [61]. Паттерн Лиссажу содержит важную информацию о разряде и, соответственно, зафиксирован нами [43]. Это было показано на (а и б) для реакторов DBD на основе медных и водных электродов при приложенном напряжении 2,6 кВ. Для большинства приложений DBD эта фигура очень похожа на идеальный параллелограмм, что можно определить из [43].В этом случае напряжение достаточно высокое, чтобы вызвать пробой газа внутри реактора. В результате заряд сдвигается по фазе относительно напряжения из-за резистивных потерь в разряде, что приводит к такому типу структуры [62]. Из этого рисунка можно узнать напряжение разряда и эффективные емкости разрядного промежутка и диэлектриков [43]. Линии (a – b) и (c – d) на изображении представляют собой емкостные переходы, а линии (b – c) и (d – a) — переходы разряда [62].Наклоны линий, представляющих емкостные переходы, дают общую емкость разрядного реактора, которая обозначается как C — . Наклоны линий, отображающих переходы разряда, равны C diel , которая представляет собой емкость диэлектрика [62]. Энергия, рассеиваемая в разряде за один период напряжения, может быть рассчитана путем измерения площади паттерна Лиссажу [43, 62, 63]. Если умножить частоту на эту площадь, то можно получить среднюю мощность (Вт), рассеиваемую в разряде [63, 64, 65, 66, 67].Мощность разряда также можно рассчитать, используя значения тока и напряжения разряда, которые в нашем случае изменяются от 0,40 до 0,61 Вт.
(a) Формы сигналов напряжения и (b) формы сигналов тока, демонстрирующие микроразряды нитевидного типа, зарегистрированные для плазменного реактора DBD с использованием конфигураций медного и водяного электродов.
Картины Лиссажу (Q – V), полученные для плазмы разряда с использованием конфигураций медного (а) и водяного (б) электродов.
Изучена скорость реакции разложения метанола при различной входной мощности.Возьмем C 0 и C t в качестве начальной и конечной концентрации раствора метанола во время реакции t соответственно. Теперь C t / C 0 был рассчитан и нанесен на график в зависимости от времени обработки для различных входных мощностей. Это было изображено в. Это показывает, что графики деградации следуют кинетике первого порядка со следующим выражением (уравнение 15).
Разложение метанола (Ct / C 0 ) со временем для различных входных мощностей, показывающее кинетику первого порядка.
В приведенном выше уравнении k обозначает константу скорости (с -1 ) . Из анализа был сделан вывод, что с увеличением мощности разложение метанола будет более эффективным.
Продукт, полученный из реактора, был проанализирован с помощью газовой хроматографии (ГХ), и полученные данные представлены для медных и водяных электродов соответственно. Один набор таких хроматограмм, полученных со спектрометра для продуктовых газов, генерируемых из плазменного реактора с приложенным напряжением 2.9 кВ и мощность 0,61 Вт показаны на (a и b) для медных и водяных электродов. Можно заметить, что на обеих хроматограммах наблюдался один главный пик со временем удерживания около 3 мин. Этот пик был приписан газу H 2 [68]. Для медного электрода концентрация газообразного водорода варьировалась от 79,2 до 98,1% при изменении мощности разряда от 0,40 до 0,61 Вт. Но для проведения воды в качестве электрода концентрация H 2 меньше для начальной мощности до 0.46 Вт. После этого концентрация увеличивается и достигает максимума (98,7%) со временем удерживания 3,681 мин при максимальной мощности разряда 0,61 Вт. Это значение выше, чем концентрация, полученная для медного электрода. Таким образом, из всех наблюдений наибольшая концентрация H 2 с высочайшей чистотой наблюдается для водного электродного узла. Но концентрация более стабильна для установки с медным электродом. Изменение концентрации водорода, производимого для различных входных напряжений и электродов, показано на.
Таблица 2
Данные газовой хроматографии при разном напряжении и входной мощности для медного электрода.
| Sl. № | Напряжение (кВ) | Время пребывания (мин) | Площадь на хроматограмме (кв. Ед.) | Концентрация H 2 (%) | ||||
|---|---|---|---|---|---|---|---|---|
| 1 | 1,9 | 3,6975566 | 94,0 | |||||
| 2 | 2,2 | 3,701 | 87613 | 96.3 | ||||
| 3 | 2,4 | 3,681 | 535282 | 98,1 | ||||
| 4 | 2,6 | 3,490 | 106425 | 4 93,8 | 106425 | 4 93,8 | 4,8 | 97,4 |
| 6 | 2,9 | 3,642 | 105293 | 79,2 |
Таблица 3
Данные газовой хроматографии при различных напряжениях и входной мощности для водяного электрода.
| Sl. № | Напряжение (кВ) | Время пребывания (мин) | Площадь на хроматограмме (кв. Ед.) | Концентрация H 2 (%) | ||||
|---|---|---|---|---|---|---|---|---|
| 1 | 1.9 | 3,631 | 13830 | 29,6 | ||||
| 2 | 2,2 | 3,627 | 16421 | 37,0 | ||||
| 3 | 2,4 | 3,681 | 394628 | |||||
| 4 | 2,6 | 3,685 | 555202 | 75,7 | ||||
| 5 | 2,8 | 3,693 | 501858 | 4 904 904 | 501858 | 4 98,4 | 4 98,4 | 98,7 |
Газовые хроматографы, записанные для газообразного продукта из реактора DBD с использованием (а) медных и (б) водяных электродов.
H 2 концентрация (%) для различных напряжений разряда реактора DBD с использованием (а) медных и (б) водяных электродов.
Из вышеупомянутого эксперимента также было замечено, что скорость образования (мол.%) Водорода увеличивается с увеличением мощности разряда. Молярный процент H 2 напрямую зависит от разложения метанола [27, 28]. При фиксированном объеме и концентрации метанола разложение будет зависеть от приложенной энергии, генерируемой плазмой, которая инициирует химическую реакцию. Эта энергия подается от электрического генератора в реактор, чтобы активировать молекулу метанола до более высоких уровней энергии и генерировать более энергичные электроны и радикалы.Вследствие этого происходит инициирование разрыва связей C – H и O – H в метаноле, приводящее к разложению [27]. Это приводит к увеличению мол.% Водорода с увеличением мощности разряда, что показано на фиг. Выход водорода (%) рассчитывается с использованием значений количества продукта (мол.%) И количества (мол.%) Метанола [60]. Поддерживая постоянную мощность разряда на уровне 0,61 Вт, исследования разложения метанола проводили в течение 35 мин и определяли выход (%) водорода.Изменение значения доходности (%) относительно время было показано в. Когда мы подаем измеренное количество метанола в реактор, все молекулы, распределенные по всему объему, могут не найти равного воздействия на основную зону разряда, чтобы получить достаточно энергии для начала разложения. Таким образом, часть метанола разлагается с образованием водорода, что вначале приводит к более низкому выходу (%). Но с течением времени все больше и больше молекул метанола возбуждаются, что приводит к увеличению выхода водорода.Скорость столкновения молекул метанола с другими ионными частицами, такими как электроны или радикалы, увеличивается, что приводит к увеличению превращения метанола в водород и другие продукты [27]. Он достигает максимума, а затем уменьшается, так как концентрация метанола также уменьшается со временем. В нашем случае то же самое наблюдалось, и через 35 мин мы наблюдали снижение выхода H 2 . С увеличением времени разряда выход водорода увеличивается и достигает максимального значения 12.4% для медного электрода и 24,3% для водяного электрода. Вначале скорость образования водорода увеличивается до 15 мин, а затем скорость уменьшается. Конверсия метанола увеличивается с 67% до 88% при увеличении времени с 5 до 35 минут. Установлено, что энергоэффективность составляет 0,5 моль H 2 / кВтч и 1,2 моль H 2 / кВтч для медных и водяных электродов соответственно. Зона разряда также играет важную роль в конверсии метанола и производстве водорода для того же диэлектрического материала при постоянной входной мощности [11, 42, 60, 69, 70, 71].В настоящем исследовании разряд характеризуется множественным током и серией микроразрядов за полупериод приложенного напряжения. Разгрузка осуществляется непрерывно по всей зоне, и непрерывное выделение газа наблюдается в течение 20 мин. Наблюдается, что через 20 мин скорость производства водорода замедляется, а затем увеличивается с дальнейшим увеличением мощности. Однако выход водорода зависит от количества концентрации метанола. Если концентрация метанола уменьшается, скорость производства водорода также уменьшается.Нельзя не учитывать влияние материала внешнего электрода на выход водорода. Эти электроды не контактируют с химически активным материалом, то есть с метанолом, и подключены как заземленный электрод. Таким образом, можно утверждать, что нет каталитического влияния этого электрода на деградацию метанола [48]. Но в нашем случае мы наблюдали самую высокую концентрацию и лучший выход водорода в% для водяного электрода по сравнению с медной сеткой. Таким образом, можно утверждать, что однородное и стабильное электрическое поле создается водным электродом, индуцирующим превращение метанола и показывающим лучший выход.Этого не добиться с помощью медной сетки, которая имеет меньшую площадь поверхности и пористую структуру [48]. Неповрежденность поверхности также является важным параметром для рассеивания энергии и генерации плазмы, что больше в случае водяного электрода. Это может быть еще одной причиной того, что в случае водяного электрода имеет место лучший нитевидный разряд, чего не обеспечивает пористая медная сетка.
Изменение скорости (моль) образования водорода при различной мощности разряда в течение времени разряда 5 мин.
Изменение выхода водорода (%) во времени (мощность разряда: 0,5 Вт).
Во время разряда можно предположить разложение промежуточных соединений метанола типа OH, O, CO и CH 3 O [72, 73]. Однако газохроматографическое исследование указывает на образование только H 2 , что подтверждено значением времени пребывания при постоянной скорости потока. На электродах не обнаружено нагара. Образование гидроксильных радикалов (обнаруживаемое с помощью гидрофильного теста полиэтиленом) предотвращает образование углеродистых частиц.Когда вода используется в качестве дополнительного реагента вместе с метанолом в реакторе DBD, такие вещества, как H 2 , CO, CO 2 , HCHO, этиленгликоль, также образуются в качестве побочных продуктов [74, 75, 76]. Плазменные реакторы DBD с различными конфигурациями с различными типами диэлектрических материалов, таких как оксид алюминия и титанат бария, обсуждались с точки зрения энергоэффективности [77]. Но в нашем случае слабопроводящая морская вода, используемая в качестве внешнего электрода, показала лучшую энергоэффективность, чем медный электрод.Концентрация и объем побочных продуктов также очень меньше по данным газохроматографического исследования. Входной ток также меньше для плазменного разряда в случае водяного электрода по сравнению с медным внешним электродом. Анализ состава воды, используемой в качестве внешнего электрода для плазменного реактора, также проводился до и после процесса разряда. Это было выполнено для изучения влияния плазменного процесса на материал электрода. Данные представлены в формате. Можно отметить, что значение pH воды немного меняется от 7.76-7,62 после плазменной обработки, как и другие параметры, приведенные в таблице. Значение химической потребности в кислороде (ХПК) изменяется до 1146–1923 мг / л с 1235–2506 мг / л после завершения эксперимента. Это может быть связано с влиянием плазменного процесса. Таким образом, можно констатировать минимальное изменение состава воды после эксперимента. Также было проведено исследование разложения метанола для проверки наличия каких-либо вредных материалов в виде остатков после завершения процесса плазменной резки.Спектры поглощения раствора метанола в УФ-видимой области до начала эксперимента и для остатка, полученного после обработки, также были записаны, которые показаны на рис. Спектр поглощения необработанного метанола показывает пик около 270 нм, который, по-видимому, остается таким же для остаточных продуктов, полученных из реактора после завершения эксперимента для различных приложенных напряжений. Метанол показывает пик поглощения (λ max ) около 220–280 нм в УФ-области [78].Таким образом, можно понять, что остаток также содержит необработанный метанол в качестве основной части, которая не подверглась разложению. Согласно недавно опубликованному отчету, Dey et al. сообщили о производстве H 2 с использованием плазменной технологии DBD со встроенным медным электродом [79]. Эль-Шафи и др. исследовали образование водорода при разложении водяного пара с использованием плазмы в качестве источника энергии [80, 81]. Насколько нам известно, исследований по производству водорода с использованием плазменного реактора DBD с водой в качестве электрода не сообщалось.Итак, наш метод — это инновационный подход в производстве возобновляемой водородной энергии.
Таблица 4
Состав воды, используемой в качестве электрода до и после плазменного процесса.
| Параметр | До лечения | После лечения |
|---|---|---|
| pH | 7,76 | 7,62 |
| Общая жесткость (мг / л) | (мг / л)3088 | 3075 |
| Электропроводность (мкСм / см) | 730 | 734 |
| DO (мг / л) | 12 | 10.5 |
| ХПК (мг / л) | 1235–2506 | 1146–1923 |
Спектры оптического поглощения остатка, полученного из плазменного реактора DBD вместе с необработанным метанолом.
4. Заключение
Настоящее исследование основано на конструкции плазменного реактора DBD и получении газообразного водорода путем разложения метанола в указанном выше реакторе. Характеристики плазменного разряда были изучены с использованием двух типов внешних электродов, таких как медь, и проводящей морской воды, при этом внутренний электрод оставался неподвижным как медный.Нитевидные типы микроразряда наблюдались в форме волны тока при приложении напряжения, которое увеличивается со временем. Характеристики разряда контролировались, обращая внимание на такие важные факторы, как: входная мощность, время разряда и типы электродов, которые имеют доминирующее влияние на характеристики реакции. Проведены электрические характеристики для определения оптимальной входной мощности реактора DBD. Было обнаружено, что выход конверсии метанола выше для водяного электрода по сравнению с металлическим при более высокой мощности разряда.Было обнаружено, что реактор демонстрирует лучшую энергоэффективность (1,2 моль H 2 / кВт · ч) для узла водяного электрода. Таким образом, можно использовать слабопроводящую морскую воду в качестве электрода в плазменной установке DBD, которая показала лучшую энергоэффективность. Водный электрод создает однородное и стабильное электрическое поле в плазменном реакторе, вызывая более быстрое преобразование метанола, что приводит к более высокому выходу водорода (%). Анализ состава воды, используемой в качестве электрода, показывает минимальные изменения после плазменной обработки без каких-либо других вредных остатков из реактора, кроме необработанного метанола.Считается, что это исследование будет полезно для моделирования и применения разрядной плазмы экономически эффективным способом для генерации водорода.
Заявления
Заявление автора о вкладе
Н. Р. Панда, Д. Саху: задумал и спроектировал эксперименты; Проведены эксперименты; Проанализировал и интерпретировал данные; Предоставленные реагенты, материалы, инструменты анализа или данные; Написал газету.
Отчет о финансировании
Это исследование не получало какого-либо специального гранта от финансирующих агентств в государственном, коммерческом или некоммерческом секторах.
Заявление о конкурирующих интересах
Авторы заявляют об отсутствии конфликта интересов.
Дополнительная информация
Дополнительная информация по данной статье недоступна.
Благодарности
Авторы искренне благодарят уважаемых рецензентов за конструктивные предложения по импровизации рукописи. Один из авторов (DS) очень благодарен профессору Суприя Паттанаяк, вице-канцлеру CUTM за постоянную поддержку в проведении этой работы.
Ссылки
1. Ло Й., Тан Л., Хан У., Ю К., Ченг Х.-М., Цзоу Х., Лю Б. Морфология и химия поверхности инженерии к универсальным pH-катализаторам для выделения водорода при высокая плотность тока. Nat. Commun. 2019; 10 (269): 1–9. [Бесплатная статья PMC] [PubMed] [Google Scholar] 2. Кумар П., Деви П., Джайн Р., Шивапрасад С.М., Синха Р.К., Чжоу Г., Нотцель Р. Квантовая точка активировала нитрид индия-галлия на кремнии в качестве фотоанода для генерации солнечного водорода. Communications Chem. 2019; 2 (4): 1–7.[Google Scholar] 3. Zhang H., Ding Q., He D., Liu H., Liu W., Li Z., Yang B., Zhang X., Lei L., Jin S. A p-Si / NiCoSe x core / оболочка наностолбикового фотокатода для улучшенного фотоэлектрохимического производства водорода. Energy Environ. Sci. 2016; 9: 3113–3119. [Google Scholar] 4. Карраро П.М., Сапаг К., Олива М.И., Эймер Г.А. Сравнительное исследование накопления водорода на мезопористых материалах, легированных металлами. Chem. Phys. Lett. 2018; 701: 93–97. [Google Scholar] 5. Кумар А., Прасад Р., Шарма Ю.С. Исследование парового риформинга этанола на катализаторе ZSM-5 на основе кобальта по сравнению с никелевым для производства возобновляемого водорода.Подбородок. J. Chem. Англ. 2019; 27 (3): 677–684. [Google Scholar] 6. Ли С.-Л., Сюй К. Металлоорганические каркасы как платформы для чистой энергии. Energy Environ. Sci. 2013; 6: 1656–1683. [Google Scholar] 7. Чу С., Маджумдар А. Возможности и проблемы для устойчивого энергетического будущего. Природа. 2012; 488: 294–303. [PubMed] [Google Scholar] 8. Тернер Дж. А. Устойчивое производство водорода. Наука. 2004; 305: 972–974. [PubMed] [Google Scholar] 9. Гольцов В.А., Везироглу Т.Н., Гольцова Л.Ф. Водородная цивилизация будущего — новая концепция ИАГЭ.Int. J. Водородная энергия. 2006; 31: 153–159. [Google Scholar] 10. Ni M., Leung D.Y.C., Leung M.K.H., Sumathy K. Обзор производства водорода из биомассы. Топливный процесс. Technol. 2006; 87: 461–472. [Google Scholar] 11. Ван Б., Лу Ю., Чжан Х., Ху С. Генерация водорода при паровом риформинге этанола в диэлектрическом барьерном разряде. J. Nat. Gas Chem. 2011; 20: 151–154. [Google Scholar] 12. Зюттель А., Боргшульте А., Шлапбах Л. Верлаг ГмбХ и Ко. KGaA; Weinheim: 2008. Водород как будущий носитель энергии, WILEY-VCH.[Google Scholar] 13. Румпель С., Зибель Дж. Ф., Фарес К., Дуан Дж., Рейджерс Э., Хаппе Т., Любиц В., Винклер М. Повышение производства водорода микроводорослями путем перенаправления электронов из фотосистемы I на гидрогеназу. Energy Environ. Sci. 2014; 7: 3296–3301. [Google Scholar] 14. Крузе О., Ханкамер Б. Производство водорода из микроводорослей — обзор. Curr. Opin. Biotechnol. 2010. 21 (3): 238–243. [PubMed] [Google Scholar] 15. Джэ Х., Хван А., Кабра Н., Ким Дж. Р., Чон Б.-Х. Производство водорода из фотогетеротрофных микроводорослей с использованием сточных вод, богатых ацетатом и бутиратом.Энергия. 2014; 78: 887–894. [Google Scholar] 16. Ли X.S., Чжу А.М., Ван К.Дж., Сюй Ю., Сун З.М. Конверсия метана в углеводороды C 2 и водород в атмосферной нетепловой плазме, генерируемой различными методами электрического разряда. Катал. Сегодня. 2004. 98: 617–624. [Google Scholar] 17. Индарто А. Производство водорода из метана в диэлектрическом барьерном разряде с использованием оксида цинка и хрома в качестве катализатора. J. Chin. Inst. Chem. Англ. 2008; 39: 23–28. [Google Scholar] 18. Са С., Сильва Х., Суза Дж.М., Мендес А. Производство водорода паровым риформингом метанола в мембранном реакторе: палладиевые и углеродные мембраны молекулярных сит. J. Membr. Sci. 2009. 339 (1–2): 160–170. [Google Scholar] 19. Zong C.Y., Chen L., Wang H.L. Генерация водорода при электролизе метанольных растворов плазмой тлеющего разряда. Int. J. Водородная энергия. 2009. 34 (1): 48–55. [Google Scholar] 20. Чанг Ф.В., Розелин Л.С., Оу Т.С. Получение водорода частичным окислением метанола на биметаллических катализаторах Au – Ru / Fe 2 O 3 .Прил. Катал. A Gen.2008; 334 (1-2): 147–155. [Google Scholar] 21. Индарто А., Ян Д. Р., Палгунади Дж., Чой Дж. У., Ли Х., Сон Х. К. Частичное окисление метана на катализаторе Cu – Zn – Al в диэлектрическом барьерном разряде. Chem. Англ. Процесс. 2008. 47 (5): 780–786. [Google Scholar] 22. Безансон Б.М., Хасанов В., Имбо-Ластапис Р., Бенешб Р., Баррио М., Мольнвикч М.Дж. Качество водорода от декарбонизированного ископаемого топлива до топливных элементов. Int. J. Водородная энергия. 2009. 34 (5): 2350–2360. [Google Scholar] 23. Дас Д., Везироглу Т.N. Производство водорода биологическими процессами: обзор литературы. Int. J. Водородная энергия. 2001. 26 (1): 13–28. [Google Scholar] 24. Возьмите Т., Цурутани К., Умеда М. Получение водорода электролизом водного раствора метанола. J. Источники энергии. 2007. 164 (1): 9–16. [Google Scholar] 25. Гондал М.А., Хамид А., Ямани З.Х. Получение водорода путем лазерного преобразования метанола с использованием полупроводникового катализатора n-типа WO 3 . J. Mol. Катал. Chem. 2004. 222 (1–2): 259–264. [Google Scholar] 26. Мединский М.А., Дорман Д.С. Последние разработки в области токсичности метанола. Toxicol. Lett. 1995. 82–83: 707–711. [PubMed] [Google Scholar] 27. Ван Б., Чжан Х., Бай Х., Лу Ю., Ху С. Производство водорода из метанола с помощью диэлектрического барьерного разряда. Передний. Chem. Sci. Англ. 2011; 5 (2): 209–214. [Google Scholar] 28. Wang Y.-F., You Y.-S., Tsai C.-H., Wang L.-C. Производство водорода путем разложения метанола с использованием скользящего дугового газового разряда. Int. J. Водородная энергия. 2010; 35: 9637–9640. [Google Scholar] 29. Дурка Т., Стефанидис Г.Д., Гервен Т.В., Станкевич А.И. Активируемый микроволнами паровой риформинг метанола для производства водорода. Int. J. Водородная энергия. 2011; 36: 12843–12852. [Google Scholar] 30. Янь З.С., Ли К., Ли В.Х. Получение водорода плазменным электролизом метанольных растворов тлеющим разрядом. Int. J. Водородная энергия. 2009; 34: 48–55. [Google Scholar] 31. Гасемзаде К., Тилебон С.М.С., Базиль А. Реакции риформинга и частичного окисления метанола для производства водорода. В: Базиль А., Далена Ф., редакторы. Метанол; Наука и техника.Эльзевир; 2018. С. 239–278. [Google Scholar] 32. Ван Х.-С., Хуанг К.-Й., Хуан Ю.-Дж., Су Я.-К., Цзэн Ф.-Г. Низкотемпературная установка микрореформинга метанола с частичным окислением с высокой степенью конверсии топлива и выходом производства водорода. Прил. Энергия. 2015; 138: 21–30. [Google Scholar] 33. Толедо М., Гонсалес Ф., Эллзи Дж. Производство водорода из метанола и частичного окисления этанола. Энергетическое топливо. 2014. 28 (5): 3453–3459. [Google Scholar] 34. Chen W.-H., Shen C.-T., Lin B.-J., Liu S.-C. Производство водорода путем частичного окисления метанола на катализаторе Pt / Al 2 O 3 с низким содержанием Pt.Энергия. 2015; 88: 399–407. [Google Scholar] 35. Мейяппан М. Плазменные нанотехнологии: прошлое, настоящее и будущее. J. Phys. D Прил. Phys. 2011; 44: 174002. [Google Scholar] 36. Кен Остриков К., Квелбар У., Мерфи А. Плазменная нанонаука: определение направлений, решение грандиозных проблем. J. Phys. D Прил. Phys. 2011; 44: 174001. [Google Scholar] 37. Богертс А., Нейтс Э., Гиджбельс Р., Spectrochim J. Плазма газового разряда и ее применение. Acta, Часть B. 2002; 57: 609–658. [Google Scholar] 38. Ма М., Ян Л., Оуян Л., Шао Х., Чжу М. Содействие получению водорода при гидролизе Mg-графитовых композитов с помощью плазменного измельчения. Энергия. 2019; 167: 1205–1211. [Google Scholar] 39. Ян З., Чен Л., Ван Х. Экспериментальное исследование плазменного поджидкостного электролиза при генерации водорода. Подбородок. J. Proc. Англ. 2006. 6 (3): 398–401. [Google Scholar] 40. Поляков О.В., Бадалян А.М., Бахтурова Л.Ф. Выход разложения воды и пространственное распределение первичных радикалов в приразрядном объеме электролитического катода.High Energy Chem. 2002. 36 (5): 280–284. [Google Scholar] 41. Rico V.J., Hueso J.L., Cotrino J., Gonzalez-Elipe A.R. Оценка различных конфигураций плазмы диэлектрического барьерного разряда в качестве альтернативной технологии для зеленой химии C 1 при конверсии метана с диоксидом углерода и прямом разложении метанола. J. Phys. Chem. 2010. 114 (11): 4009–4016. [PubMed] [Google Scholar] 42. Чироков А., Гуцол А., Фридман А. Плазма атмосферного давления диэлектрических барьерных разрядов.Pure Appl. Chem. 2005. 77 (2): 487–495. [Google Scholar] 43. Когельшац У. Разряды с диэлектрическим барьером: их история, физика разряда и промышленное применение. Plasma Chem. Плазменный процесс. 2003. 23 (1): 1–46. [Google Scholar] 44. Giorgi M.G.D., Ficarella A., Sciolti A., Pescini E., Campilongo S., Lecce G.D. Повышение устойчивости обедненного пламени обратного диффузионного пламени метан / воздух за счет использования коаксиальных диэлектрических исполнительных механизмов плазменного разряда. Энергия. 2017; 126: 689–706. [Google Scholar] 45. Сармиент Б., Брей Дж.Дж., Виера И.Г., Гонсалес-Элипе А.Р. Производство водорода путем риформинга углеводородов и спиртов в диэлектрическом барьерном разряде. J. Источники энергии. 2007. 169: 140–143. [Google Scholar] 46. Танабэ С., Мацугума Х., Окицу К., Мацумото Х. Получение водорода из метанола в разрядно-плазменной системе с диэлектрическим барьером. Chem. Lett. 2000. 29 (10): 1116–1117. [Google Scholar] 47. Ван Л., Лю С.Ю., Сюй С., Ту X. Прямое преобразование метанола в n-C 4 H 10 и H 2 в разрядном реакторе с диэлектрическим барьером.Green Chem. 2016; 18: 5658–5666. [Google Scholar] 48. Чжан X., Ван Б., Лю Ю., Сюй Г. Конверсия метана путем парового риформинга с использованием разряда с диэлектрическим барьером. Подбородок. J. Chem. Англ. 2009. 17 (4): 625–629. [Google Scholar] 49. Гоми Х., Сафа Н.Н., Гасеми С. Исследование плазменного реактора DBD. IEEE Trans. Plasma Sci. 2011. 39 (11): 2104–2105. [Google Scholar] 50. Индарто А. Обзор прямого превращения метана в метанол с помощью диэлектрического барьерного разряда. IEEE Trans. Dielectr. Электр. Insul. 2008. 15 (4): 1038–1043.[Google Scholar] 51. Сюэ Дж., Чен Л., Ван Х. Л. Механизм разложения ализаринового красного в плазме гибридного газожидкостного диэлектрического барьерного разряда: экспериментальное и теоретическое рассмотрение. Chem. Англ. J. 2008. 138 (1–3): 120–127. [Google Scholar] 52. Вагнер Х. Э., Бранденбург Р., Козлов К. В., Зонненфельд А., Мишель П., Бенке Дж. Ф. Барьерный разряд: основные свойства и применения для обработки поверхностей. Вакуум. 2003. 71 (3): 417–436. [Google Scholar] 53. Сан Б., Сато М., Харано А., Клементс Дж. С. Образование радикалов в дистиллированной воде при неоднородном импульсном разряде.J. Electrost. 1998. 43 (20): 115–126. [Google Scholar] 54. Ма Ю., Чен Дж., Ян Б., Ю. К. Деградация метанола высокой концентрации в водном растворе с помощью диэлектрического барьерного разряда. Труды IEEE по плазменным наукам. 2013. 41 (7): 1716–1724. [Google Scholar] 55. Ци З., Лин Х., Чжао Ю., Ню Дж., Лю Д., Дин З., Ся Й., Цзи Л., Чжао З., Ян Л. Взаимодействие плазменной струи с метанолом как фундаментальные процессы в растворе . IEEE Trans. Plasma Sci. 2019; 47 (11): 4802–4810. [Google Scholar] 56. Кабашима Х., Эйнага Х., Футамура С. Генерация водорода из воды, метана и метанола с нетепловой плазмой. IEEE Trans. Ind. Appl. 2003. 39 (2): 340–345. [Google Scholar] 57. Бундалеска Н., Цыганов Д., Сааведра Р., Татарова Е., Диас Ф. М., Феррейра К. М. Получение водорода в результате риформинга метанола в плазме типа «торнадо» СВЧ. Int. J. Водородная энергия. 2013. 38 (22): 9145–9157. [Google Scholar] 58. Футамура С., Кабашима Х. Влияние типа реактора и вольт-фарадных свойств на риформинг метанола с нетепловой плазмой.IEEE Trans. Ind. Appl. 2004. 40 (6): 1459–1466. [Google Scholar] 59. Zhang H., Zhu F., Li X., Cen K., Du C., Tu X. Повышенное производство водорода путем разложения метанола с использованием новой вращающейся плазмы скользящего дугового разряда. RSC Adv. 2016; 6 (16): 12770–12781. [Google Scholar] 60. Чао X., Синь Т. Конверсия метана с помощью плазмы в реакторе с диэлектрическим барьерным разрядом атмосферного давления. J. Energy Chem. 2013. 22: 420–425. [Google Scholar] 61. Яо С., Накаяма А., Судзуки Э. Конверсия метана с использованием высокочастотной импульсной плазмы: особенности разряда.Айше Дж. 2001; 47: 419–426. [Google Scholar] 62. Магуряну М., Мандаче Н. Б., Парвулеску В. И., Субраманьям Ч., Ренкен А., Киви-Минскер Л. Повышение производительности нетеплового плазменного реактора при разложении трихлорэтилена: оптимизация геометрии реактора и введение каталитического электрода. Прил. Катал. B Environ. 2007. 74: 270–277. [Google Scholar] 63. Краусс М., Элиассон Б., Когельшатц У., Вокаун А. CO 2 риформинг метана путем сочетания разрядов с диэлектрическим барьером и катализа.Phys. Chem. Chem. Phys. 2001; 3: 294–300. [Google Scholar] 64. Шибата Т., Нишияма Х. Обработка воды разрядной трубкой с диэлектрическим барьером с потоком пара. Int. J. Plasma Environ. Sci. Technol. 2017; 11 (1): 112–117. [Google Scholar] 65. Фалькенштейн З., Куган Дж. Дж. Поведение микроразряда при бесшумном разряде смесей азота с кислородом и водой с воздухом. J. Phys. D Прил. Phys. 1997. 30: 817–825. [Google Scholar] 66. Zou J.-J., Zhang Y.-P., Liu U.-J. Производство водорода путем частичного окисления диметилового эфира с использованием плазмы коронного разряда.Int. J. Водородная энергия. 2007. 32: 958–964. [Google Scholar] 67. Накаяма Ю.С., Судзуки А.Э. Конверсия метана с использованием высокочастотной импульсной плазмы: особенности разряда. Айше Дж. 2001; 47: 419–426. [Google Scholar] 68. Лэмб А., Ларсон К.А., Толлефсон Э.Л. Газохроматографический метод анализа выхлопных газов. J. Загрязнение воздуха. Contr. Доц. 1973; 23 (3): 200–202. [PubMed] [Google Scholar] 69. Хадир Н., Ходжа К., Беласри А. Конверсия метана с использованием реактора с диэлектрическим барьерным разрядом при атмосферном давлении для производства водорода.Plasma Sci. Technol. 2017; 19: 95502. [Google Scholar] 70. Ван К., Ян Б.-Х., Цзинь Ю., Ченг Ю. Исследование сухого риформинга метана в реакторе с диэлектрическим барьерным разрядом. Plasma Chem. Плазменный процесс. 2009. 29: 217–228. [Google Scholar] 71. Саху Д. Деградация промышленных фенольных сточных вод с использованием метода плазмы диэлектрического барьерного разряда. Русь. J. Appl. Chem. 2020; 93: 905–915. [Google Scholar] 72. Ван В., Чжу С., Цао Ю. Исследование DFT путей парового риформинга этанола в условиях холодной плазмы для генерации водорода.Int. J. Водородная энергия. 2010; 35: 1951–1956. [Google Scholar] 73. Ван В.Дж., Ван Ю.К. Сухой риформинг этанола для производства водорода: термодинамическое исследование. Int. J. Водородная энергия. 2009. 34: 5382–5389. [Google Scholar] 74. Обри О., Мет К., Хацеф А., Кормье Дж. М. Об использовании нетеплового плазменного реактора для парового риформинга этанола. Chem. Англ. J. 2005; 106: 241–247. [Google Scholar] 75. Янгуас Хил А., Уэсо Дж. Л., Котрино Дж., Кабальеро А., Гонсалес Элипе А. Р. Риформинг этанола в плазменном СВЧ-разряде поверхностных волн.Прил. Phys. Lett. 2004. 85: 4004–4006. [Google Scholar] 76. Янь З.С., Ли К., Линь В.Х. Получение водорода плазменным электролизом метанольных растворов тлеющим разрядом. Int. J. Водородная энергия. 2009; 34: 48–55. [Google Scholar] 78. Уоррен К.Р. Быстрое измерение хлорофиллов с помощью считывающего устройства для микропланшетов. J. Plant Nutr. 2008. 31: 1321–1332. [Google Scholar] 79. Дей Г.Р., Зоде С.Д., Намбоудири В. Применение плазмы для эффективного производства H 2 : реализм медного электрода в разрядном реакторе с одним диэлектрическим барьером.Phys. Плазма. 2018; 25: 103508. [Google Scholar] 80. Эль-Шафи М., Камбара С., Хаякава Ю. Оценка производительности промышленной абсорбционной системы. Energy Rep. 2020; 6: 45–51. [Google Scholar] 81. Эль-Шафи М., Камбара С., Хаякава Ю., Миура Т. Исследование влияния температуры реактора на производство h3 из парового разложения с использованием плазмы DBD. Int. J. Водородная энергия. 2019; 44: 20239–20248. [Google Scholar](224b) Производство водорода с помощью плазменного электролиза газовой смеси h3O / SO2
Мы продемонстрировали, что реакция между водой и диоксидом серы (SO2) может катализироваться плазмохимически, а продукты реакции могут быть удалены электрохимически в виде молекул водорода (h3) с помощью палладиевого биполярного электрода.Основным побочным продуктом реакции смеси h3O / SO2 в плазменном реакторе является серная кислота (h3SO4), которую можно разложить обратно до газообразного SO2 с использованием источника тепловой энергии, такого как ядерное тепло.
Наиболее известным методом разложения воды является электролиз. Термодинамическое напряжение при электролизе воды составляет 1,23 вольта, но добавляя к воде некоторые химические вещества, такие как Ti3 +, Sb, Re, SO2, Sb, As, Re и Bi, или органические топлива, такие как метанол, термодинамическое напряжение можно значительно снизить.Например, на аноде электролизера смесь воды и SO2 окисляется с образованием иона водорода (протона) и h3SO4 при 0,18 В. Однако газ SO2 часто переходит на катод, противоположный электрод, отравляя его и электролиз. смеси является кинетически вялой, требующей высокого перенапряжения даже при использовании катализаторов семейства платины. Для решения этих проблем мы разработали новую схему, в которой обычная электролизная ячейка была заменена электрохимическим водородным насосом, контактирующим с плазменным реактором.Эти два блока, плазменный реактор и электрохимический насос, имеют общий электрод, сделанный из металла, поглощающего водород. Микроплазма может заменить дорогой катализатор Pt. Реагирующий газ, контактирующий с анодом, катализируется нетепловыми электронами, генерируемыми в плазменном реакторе. Атомы водорода, продукты плазменной реакции, растворяются в металле, поглощающем водород, таком как палладий (Pd). Металл, поглощающий водород, препятствует переносу SO2. Растворенные атомы водорода окисляются на границе раздела между Pd, теперь анодом насоса, и протонопроводящей мембраной, электролитом насоса, и восстанавливаются в газ h3 на катоде насоса.Для работы при низких температурах ниже 180 ° C в качестве электролита насоса использовалась полимерная мембрана, такая как Nafion, в то время как для работы при высоких температурах между 600 и 850 ° C твердооксидная мембрана, такая как оксид BaCe0,8Y0,2O3-К, использовалась в качестве протонпроводящего электролита.
Скорость производства газообразного водорода из насоса для низкотемпературной работы составляла около 0,5 мл в минуту, когда напряжение и ток регулировались на 0,1 В и 60 мА ∙ см-2, соответственно. Энергоэффективность, определяемая как объем водорода, произведенного на общую потребляемую электрическую энергию, составляла 6 мл на 100 Дж для низкотемпературного режима, в то время как эффективность подскочила до 16 мл на 100 Дж для высокотемпературного режима.Эффективность дополнительно увеличивалась, когда вместо источника постоянного тока использовался источник энергии, генерирующий импульсы, для экономии электроэнергии для генерации плазмы. Эффективность составляла около 50 мл на 100 Дж потребляемой электроэнергии. Для сравнения, эффективность обычного электролизера, использующего газовую смесь h3O / SO2, составляет около 25 мл на 100 Дж подводимой электроэнергии.
Процесс травления увеличивает извлечение водорода при электролизе воды
компании KeAi Communications Co., ООО
Принципиальная схема процесса травления электрокатализаторов на основе фосфидов металлов. Предоставлено: авторы.Извлечение водорода из воды посредством электролиза предлагает многообещающий путь увеличения производства водорода, чистого и экологически чистого топлива. Но одной из основных проблем электролиза воды является вялотекущая реакция кислорода на аноде, известная как реакция выделения кислорода (OER).
Сотрудничество между исследователями из Университета Хунань и Университета Шэньчжэня в Китае привело к открытию, которое обещает улучшить процесс ООР. В своей недавней статье, опубликованной в журнале KeAi Green Energy & Environment , они сообщают, что травление — или, другими словами, химическое удаление — оксидных покрытий, которые образуются на поверхности электрокатализаторов на основе фосфидов металлов, регулярно используемых в электролизе, может повысить эффективность OER.
Профессор Шуанъинь Ван из государственной ключевой лаборатории химии / био-зондирования и хемометрики Хунаньского университета возглавил исследование. Он объясняет: «Хотя фосфиды металлов часто используются в качестве катализаторов из-за их уникальных физико-химических свойств, таких как высокая проводимость, обильные запасы земли и отличные характеристики, общим, но часто игнорируемым фактом является то, что они быстро подвергаются атмосферному окислению, когда они подвержены воздействию воздуха. Это заставляет их образовывать оксидные слои на своей поверхности, что может изменить процесс реконструкции поверхности и запутать взаимосвязь между структурой и характеристиками.«
Чтобы решить эту проблему, профессор Ван и его коллеги решили удалить эти оксидные слои, используя технику плазмы диэлектрического барьерного разряда. И они обнаружили, что процесс травления не только ускоряет процесс восстановления поверхности, но и значительно усиливает образование гидроксидов металлов и активность OER.
Профессор Ван говорит: «Эти открытия полезны для понимания взаимосвязи между структурой и характеристиками фосфидов металлов в реакции электроокисления.И мы подозреваем, что тот же процесс травления может быть использован для других чувствительных к кислороду соединений металлов, таких как халькогениды, нитриды и карбиды.
«Мы надеемся, что наше исследование поможет в рациональном проектировании и разработке более эффективных электрокатализаторов для электролиза воды».
Зависимое от потенциала переключение способствует расщеплению воды с использованием катализаторов на основе оксида кобальта.
Дополнительная информация: Техуа Ван и др., Травление оксидных слоев фосфида NiFe для облегчения реконструкции поверхности для реакции выделения кислорода, Green Energy & Environment (2021).DOI: 10.1016 / j.gee.2021.03.005
Предоставлено KeAi Communications Co., Ltd.
Ссылка : Процесс травления увеличивает извлечение водорода при электролизе воды (2021, 17 мая) получено 14 октября 2021 г. с https: // физ.org / news / 2021-05-etching-Hydrolysis.html
Этот документ защищен авторским правом. За исключением честных сделок с целью частного изучения или исследования, никакие часть может быть воспроизведена без письменного разрешения. Контент предоставляется только в информационных целях.
Система производства водорода с использованием нетеплового плазменного электролиза в растворе глицерин-КОН
Чаффин, Дж.Х., Боббио, С.М., Иньянг, Х.И., Каанагбара, Л., 2006. Производство водорода с помощью плазменного электролиза. Журнал энергетической инженерии, том 132 (3), стр. 104–108.
Холладей, Д.Д., Ху, Д., Кинг, Д.Л., Ван. Ю., 2009. Обзор технологий производства водорода. Катализ сегодня, том 139, стр. 244–260.
Jinzhang, G., Aixiang, W., Yan, F., Jianlin, W., Dongping, M., Xiao, G., Yan, L., Wu, Y., 2008. Анализ энергичных видов, вызванных контактом Электролиз тлеющим разрядом в водном растворе.Наука и технологии плазмы, Том 10, номер 1.
Мизуно Т., Акимото Т., Омори Т., 2003. Подтверждение аномального образования водорода с помощью плазменного электролиза. В: 4-е заседание Японского исследовательского общества CF, Иватэ, Япония: Университет Иватэ.
Петитпаса, Дж., Роллиера, Дж. Д., Дармонб, А., Гонсалес-Агилара, Дж., Меткемейера, Р., Фулчерия, Л., 2007. Сравнительное исследование технологий реформинга с помощью нетепловой плазмы. Международный журнал водородной энергетики, том 32, стр.2848–2867.
Саксоно, Н., Джайнал, А., Сетиджо, Б., 2010. Проектирование систем производства водорода с помощью плазменного процесса нетеплового электролиза. 1-й Международный семинар по основам и применению химической инженерии, Бали, Индонезия.
