Гальваника в домашних условиях — нужное оборудование и советы
Физико-химические свойства некоторых металлов ухудшают их техническое применение. Некоторые виды стали (сплав на основе железа и углерода) могут вступать в контакт с водой, что приводит к коррозии и разрушению изделия. Чтобы предотвратить подобный сценарий, используется вспомогательная обработка металлов/сплавов. Одним из вариантов обработки является проведение гальванизации. Возможна ли гальваника в домашних условиях? Какие техники гальваники существуют и какое оборудование понадобится мастеру? И о каких правилах техники безопасности не стоит забывать? В статье эти вопросы будут рассмотрены.
Общие сведения
Гальваника (гальванизация) — физико-химическая технология, с помощью которой можно создать на поверхности металла дополнительный слой из другого металла. Толщина дополнительного слоя является небольшой. Обычно она составляет от 0,1 до 2-3 миллиметров. Гальванизация используется для многих целей — повышение прочности, создание антикоррозийного слоя и другие. Покрыть гальваническим слоем можно только металлическую поверхность. Это может быть посуда, детали для автомобиля, инженерные инструменты, декоративные изделия. В качестве гальванизирующего слоя выступают металлы — хром, никель, медь, серебро, цинк + сплавы на их основе.
Покрыть гальваническим слоем можно только металлическую поверхность. Это может быть посуда, детали для автомобиля, инженерные инструменты, декоративные изделия. В качестве гальванизирующего слоя выступают металлы — хром, никель, медь, серебро, цинк + сплавы на их основе.
Схема электролиза
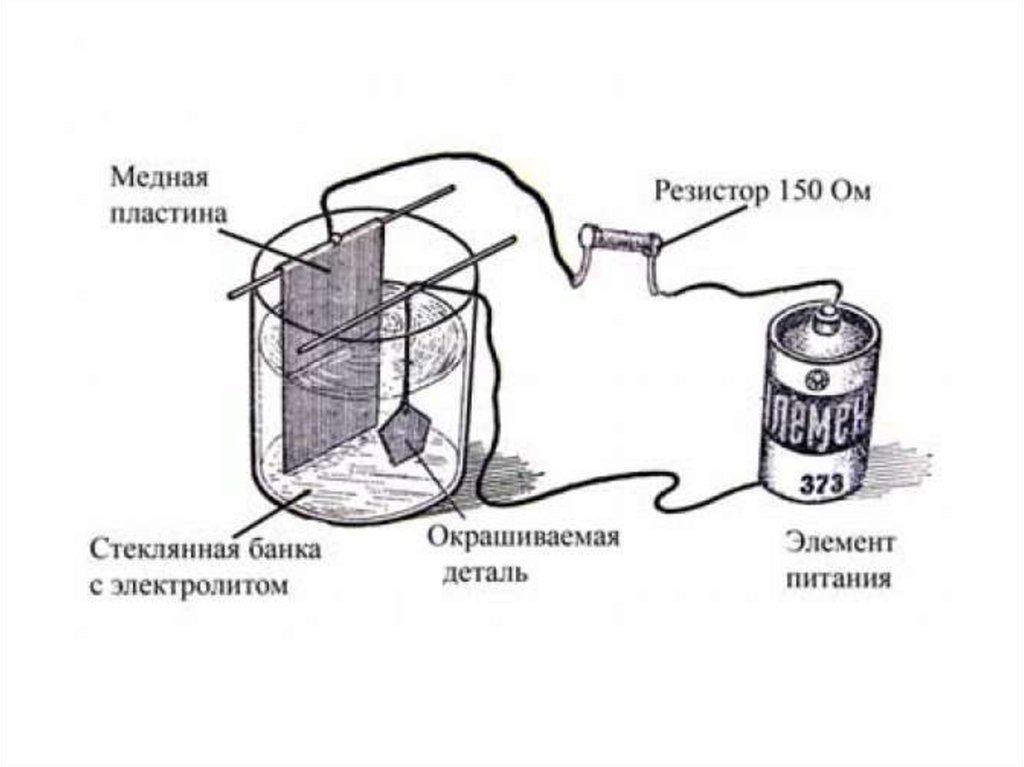
С точки зрения химии и физики гальванизация осуществляется за счет специального процесса под названием электролиз. В упрощенном виде электролиз металлических изделий выглядит так:
- Поверхность запчасти очищается от различных загрязнений (органика, пыль, грязь, легкая коррозия). Очистку рекомендуется дополнять обезжириванием, поскольку эта процедура позволяет получить чистую поверхность, на которую будет наноситься тонкий гальванический слой веществ, полученных из электролита.
- В пластиковую или стеклянную емкость помещается электролит — раствор щелочей, кислот и солей, содержащих нужный металл. Скажем, для электролитического хромирования используется хромовая кислота, которая при электролизе высвобождает хром, переходящий на деталь.
 Для улучшения гальваники электролит может нагреваться до небольших температур (обычно не более 60 градусов).
Для улучшения гальваники электролит может нагреваться до небольших температур (обычно не более 60 градусов). - К электролиту подключается источник постоянного тока (источники переменного тока не используются, поскольку операция не запустится). Для подключения используются два провода — катод и анод. Катод прикрепляется непосредственно к обрабатываемой детали, а анод помещается в раствор электролита. Анод обычно дополняется пластиной из соответствующего металла, что усиливает гальванизацию (скажем, для цинкования нужна цинковая пластина).
- Обрабатываемая деталь прикрепляется к катоду, а потом катод помещается в раствор электролита. Катод с запчастью не должен контактировать с анодом напрямую, поскольку в таком случае случится короткое замыкание либо гальваника не запустится/будет идти медленно. Обрабатываемая запчасть должна находится на хорошем расстоянии от анода с пластинами, чтобы операция прошла успешно.
- Теперь включается электрический ток, что приводит к замыканию цепи.
 Ток сперва попадает на анод, а потом поступает в электролитический раствор. Это запускает ряд химических реакций, в результате которых металлические ионы высвобождаются из вещества и начинаются двигаться вместе с электрическим током по направлению к катоду. При прохождении через катод эти ионы осаждаются на поверхности запчасти, что и приводит к образованию нужного покрытия. Для гальванической обработки одной детали требуется 20-40 минут в зависимости от размеров и формы детали.
Ток сперва попадает на анод, а потом поступает в электролитический раствор. Это запускает ряд химических реакций, в результате которых металлические ионы высвобождаются из вещества и начинаются двигаться вместе с электрическим током по направлению к катоду. При прохождении через катод эти ионы осаждаются на поверхности запчасти, что и приводит к образованию нужного покрытия. Для гальванической обработки одной детали требуется 20-40 минут в зависимости от размеров и формы детали.
Основные технологии
Основные технологии гальваники — это хромирование, серебрение, никелирование и цинкование, при которых деталь покрывается соответственно хромом, серебром, никелем и цинком. Помимо этого существуют и другие операции (скажем, меднение и латунирование). Однако для их осуществления необходимо использование цианистых солей, которые являются ядовитыми даже для человека в защитной одежде. Поэтому эти процедуры обычно выполняются в специальных цехах или мастерских.
Ванночка для гальванизации
Для создания защитного слоя на поверхности металлического изделия понадобится оборудование для гальваники. Основной элемент — это специальная ванночка для гальванизации, которую можно без труда собрать своими руками. Узнаем как это сделать и о чем нужно помнить:
Основной элемент — это специальная ванночка для гальванизации, которую можно без труда собрать своими руками. Узнаем как это сделать и о чем нужно помнить:
- Гальваническая ванночка представляет собой емкость, в которую будет помещаться электролитический раствор или обрабатываемая металлическая деталь. Поэтому объем ванночки должен быть достаточно большим, чтобы все элементы поместились в нее. Объем ванночки нужно подбирать непосредственно под деталь с небольшим запасом, чтобы в него поместилось оптимальное количество электролита (в противном случае реакция будет идти медленно либо гальванизация получится низкокачественной).
- В качестве ванночки следует использовать только пластиковые или стеклянные емкости, поскольку эти вещества отличаются химической устойчивостью и инертностью относительно электролиза. Металлические емкости попадают под полный запрет — во время электролиза металлические ионы будут переходить в электролитический раствор, что испортит гальванизацию. Эмалированные металлические изделия для гальваники тоже лучше не использовать, поскольку во время электролиза есть риск повреждения эмали с последующими переходом металлических ионов в электролит.

Другое оборудование для гальваники
К ванночке необходимо подключить источник постоянного тока, которые будет активировать электролитическую реакцию. Нужно купить стабилизированный блок питания, в состав которого входит выпрямитель электрического тока и регулятор напряжения (оптимальное напряжение — от 1 до 2,5 вольт). К ванночке от источника тока также необходимо подключить два провода, которые будут выполнять роль катода и анода. К аноду следует прикрепить анодные металлические пластины, проводящие ток. Провод-катод напрямую подключается к обрабатываемой детали.
После подключения электрических элементов в ванночку заливается жидкий электролит. Он представляет собой раствор, способный проводить электрический ток за счет диссоциации вещества на электроактивные ионы. В качестве электролита обычно используются нестабильные кислоты, щелочи или соли. Электролитический раствор можно приготовить самому, однако проще всего будет купить его в любом магазине электрических товаров или машинного оборудования. Перед гальванизацией электролит часто придется нагревать (часто его можно нагреть прямо в ванночке). Конкретный состав электролита зависит от типа операции — скажем, для хромирования в качестве электролита Вам понадобится хромовая кислота.
Перед гальванизацией электролит часто придется нагревать (часто его можно нагреть прямо в ванночке). Конкретный состав электролита зависит от типа операции — скажем, для хромирования в качестве электролита Вам понадобится хромовая кислота.
Вспомогательное оборудование
Помимо ванночки, проводов и электролита Вам рекомендуется иметь при себе вспомогательное оборудование:
- Механические или электрические весы. Они будут нужны для взвешивания отдельных гальванических компонентов, что поможет Вам подсчитать оптимальный уровень электролита в ванночки. Также они пригодятся для приготовления обезжиривающего раствора.
- Плитка для нагрева электролита (ванночку можно поставить прямо на плитку). Предпочтение рекомендуется отдать электрическим плиткам, поскольку в случае сгорания газа образуются вещества, которые могут вступить в реакцию с ванночкой и осесть в электролите, что плохо влияет на качество электролитического раствора. Обратите внимание, что электроплитка должна иметь регулятор температуры нагрева.

- Вытяжка для удаления вредных испарений. Во время гальванизации в атмосферу будет выделяться множество газообразных веществ, которые представлять опасность. К тому же они неприятно пахнут, а в случае их оседания на стенах или мебели удалить эти вещества будет весьма непросто. В качестве вытяжки рекомендуется использовать вытяжной вентилятор или похожее оборудование.
Подготовка металлических изделий
Чтобы гальваника в домашних условиях получилась качественной, нужно не только подготовить необходимое оборудование, но и выполнить предварительную обработку детали. Если поверхность детали является шероховатой, то необходимо выполнить ее выравнивание с помощью наждачной бумаги или методом точной шлифовки. Обработку можно также выполнить с помощью пескоструйной технологии, которая подходит для выравнивания поверхностей больших деталей или запчастей.
После зачистки следует также выполнить обезжиривание поверхности запчасти. Обезжиривание удаляет накопившийся слой пыли и грязи, устраняет пятна органического происхождения, повышает уровень сцепления металлических частиц с поверхностью запчасти. Для обезжиривания люди обычно применяют ацетон, спирт или бензин. Чтобы очистка получилась качественной, нужно учитывать химический состав детали:
Для обезжиривания люди обычно применяют ацетон, спирт или бензин. Чтобы очистка получилась качественной, нужно учитывать химический состав детали:
- Если Вы работаете со стальными изделиями, то обезжиривание следует проводить с помощью едкого натрия или калия. Для приготовления 1 литра раствора следует растворить в воде 50-100 г одного из веществ по выбору. После растворения смесь следует нагреть до температуры 75-90 градусов, а потом нужно поместить туда требуемую деталь. Оптимальное время обезжиривания в растворе — 15-25 минут.
- Обезжиривание алюминия выполняется по похожей схеме, но в более щадящем режиме. Для приготовления обезжиривающей смеси растворите в 1 литре воды 50 г углекислого натра или тринатрийфосфата. После этого нагрейте смесь и доведите ее до температуры 55-70 градусов. Держите деталь в нагретом растворе не более 5 минут.
- В случае работы с медными запчастями для обезжиривания следует использовать едкий натр. Оптимальная концентрация веществ — 30 г натра на 1 л воды.
 После приготовления смеси нагрейте раствор до температуры 30-40 градусов. Держать медную запчасть в очищающем растворе следует 5-8 минут (в случае детали сложной формы — 7-10 минут).
После приготовления смеси нагрейте раствор до температуры 30-40 градусов. Держать медную запчасть в очищающем растворе следует 5-8 минут (в случае детали сложной формы — 7-10 минут).
Правила техники безопасности
Во время гальванизации будет происходить множество химических реакций, в атмосферу будут выделяться вредные испарения. В небольших количествах они не представляют опасность для человека. Гальванизация — это долгий процесс, поэтому контакт человека с этими испарениями следует минимизировать. Гальванизацию рекомендуется проводить в гараже или в мастерских (на кухне такую операцию проводить не следует).
Чтобы удалять вредные испарения, помещение должно быть оборудовано вытяжкой или вытяжными вентиляторами. Человеку рекомендуется надеть на руки резиновые перчатки, которые будут минимизировать контакт кожи с химическими реагентами. На лицо следует надеть маску-респиратор и очки, которые будут защищать слизистые оболочки от контакта с газообразными испарениями. Во время гальванизации ни в коем случае нельзя пить или есть. Если во время гальваники Вам стало плохо, то необходимо срочно обесточить генератор и прекратить процедуру.
Во время гальванизации ни в коем случае нельзя пить или есть. Если во время гальваники Вам стало плохо, то необходимо срочно обесточить генератор и прекратить процедуру.
Разновидности гальваники
Итак, мы рассмотрели основы гальваники — узнали химическую основу этого процесса, поняли, как собрать ванночку, изучили правила техники безопасности. Давайте же теперь узнаем, как делается гальваника в домашних условиях. В нашем обзоре мы рассмотрим 4 основных технологии гальванизации — хромирование, цинкование, никелирование и серебрение. Некоторые в домашних условиях также выполняют меднение и латунирование (латунь — сплав на основе меди и цинка). Однако для полноценного латунирования/меднения требуются цианистые соли, которые при электролизе выделяют особо токсичные опасные вещества. Поэтому в обзоре мы эту процедуры рассматривать не будем.
Хромирование
При хромировании на поверхности детали создается тонкий слой, состоящих из хрома. Покрытие на основе хрома отлично защищает деталь от ржавчины, а также улучшает ее теплопроводность и химическую инертность. Еще одна полезная функция хромирования — декоративная (хром обладает приятным металлическим блеском, который радует глаз). В домашних условиях вы не можете сделать глубокое хромирование. Для этого требуется ток большой силы (100 ампер и выше). Однако сделать поверхностное хромирование для улучшения физических и эстетических свойства запчасти Вы сможете.
Еще одна полезная функция хромирования — декоративная (хром обладает приятным металлическим блеском, который радует глаз). В домашних условиях вы не можете сделать глубокое хромирование. Для этого требуется ток большой силы (100 ампер и выше). Однако сделать поверхностное хромирование для улучшения физических и эстетических свойства запчасти Вы сможете.
Этапы хромирования:
- Перед хромированием рекомендуется нанести на поверхность запчасти защитный слой на основе меди и никели. Сделать это можно с помощью операций никелирования. Зачем нужны эти процедуры? Объяснение простое — из-за химических особенностей вещества хромовое покрытие обладает пористой структурой. Это снижает сцепление ионов хрома с поверхности детали. Никель или медь позволяют снизить пористость, что улучшает сцепление хрома с поверхности запчасти.
- После никелирования можно приступать к хромированию. Для этого Вам понадобятся анод-пластинки на основе свинца (93-95%) и олова/сурьмы (до 7%). В качестве электролита используйте смесь хромовой (250-300 г) и серной кислот (2-3 г), оптимальная температура нагрева электролита — 50-60 градусов.
 Срок операции — 30-50 минут. По завершении процедуры рекомендуется промыть запчасть в слабом растворе соды.
Срок операции — 30-50 минут. По завершении процедуры рекомендуется промыть запчасть в слабом растворе соды.
Цинкование
Чтобы увеличить прочность запчасти и защитить ее от коррозии, может применяться процедура цинкования. Как ясно из названия, во время цинкования запчасть покрывается тонким слоем цинка. Операция цинкования — наиболее простая с технологической точки зрения. Для ее проведения нужно небольшое количество цинкового электролита (основным источником цинка будет выступать анод-пластинка). Процедура цинкования выглядит так:
- Приготовьте электролит — в 1 литре воды растворите 175 г сульфатного цинка, добавьте 30-40 г сернокислого аммония и немного ацетата натрия (10 г).
- Погрузите в приготовленный электролитический раствор анод с цинковой пластиной. Размеры пластины могут быть небольшими.
- Погрузите в раствор деталь для цинкования и включите источник постоянного тока. Срок цинкования — 50-60 минут. Электролит для цинкования нагревать не нужно.

Никелирование
Никелирование позволяет получить приятное отражающее покрытие на поверхности детали. С химической точки зрения никель является инертным веществом, поэтому никелевое покрытие будет защищать изделие от воды и легких химических токсинов. Никелирование (как и цинкование) является простой технологической операцией, а начинающий справится с ней. Процедура выглядит так:
- Для приготовления электролита смешайте следующие вещества — водный раствор сернокислого натрия (300 г), водный раствор хлористого никеля (70 г), чистая борная кислота (50 г).
- Нагрейте электролит до температуры 50-60 градусов, поместите запчасть в электролитический раствор, настройте генератор на силу тока 3-5 ампер.
- Проводите обработку в течение 50-60 минут. Обратите внимание, что испарения никеля являются токсичными, поэтому не забудьте надеть перчатки, маску или очки на лицо.
Серебрение
Позволяет получить на поверхности запчасти тонкий прочный слой серебра. Серебрение также можно делать для повышения электропроводности запчасти. По экономическим соображениям эта процедура выполняется редко (серебро является дорогим материалом). Процедура серебрения выполняется так:
Серебрение также можно делать для повышения электропроводности запчасти. По экономическим соображениям эта процедура выполняется редко (серебро является дорогим материалом). Процедура серебрения выполняется так:
- Электролит для серебрения лучше купить в магазине, поскольку приготовить его самому будет нелегко (и дорого). Хотя при желании вы можете сделать его самостоятельно, смешав чистую воду, хлористое серебро, железно цианистый калий и кальцинированную соду.
- Влейте электролит в ванночку. Если температура воздуха находится ниже 20 градусов — нагрейте электролит до этой температуры с помощью электрической плитки.
- Поместите запчасть в ванночку с электролитом. Проводите серебрение в течение 40-50 минут. По завершении процедуры можете помыть изделие в слабом растворе соды.
- Не забывайте о правилах техники безопасности, поскольку железно цианистый калий при электролизе выделяет опасные вещества.
Заключение
Гальваникой называют сложную электрохимическую реакцию, с помощью которой можно на поверхность металлических изделий можно наносить дополнительный слой металла. Дополнительный слой выполняет различные функции — защитную, антикоррозийную, эстетическую. Для гальваники нужно сделать ванночку, подключенную к источнику постоянного тока. Для запуска реакции в ванночку нужно налить электролит и опустить туда обрабатываемую деталь. Состав электролита зависит от типа реакции. Выполнить гальванику можно в домашних условиях. Основные технологии гальваники — никелирование, хромирование, серебрение, цинкование и другие.
Дополнительный слой выполняет различные функции — защитную, антикоррозийную, эстетическую. Для гальваники нужно сделать ванночку, подключенную к источнику постоянного тока. Для запуска реакции в ванночку нужно налить электролит и опустить туда обрабатываемую деталь. Состав электролита зависит от типа реакции. Выполнить гальванику можно в домашних условиях. Основные технологии гальваники — никелирование, хромирование, серебрение, цинкование и другие.
Используемая литература и источники:
- Ф.Ф. Ажогин и гр. авторов. Гальванотехника; Спр. издание / Под редакцией А.М. Гринберга. — Москва: Металлургия, 1987.
- Томашов Н. Д., Чернова Г. П. Пассивность и защита металлов от коррозии. — М., 1965.
- Новаковский В. М. Обоснование и начальные элементы электрохимической теории растворения окислов и пассивных металлов // В сб.: Коррозия и защита от коррозии. Т. 2. — М., 1973.
- Статья на Википедии
технологический процесс и необходимое оборудование :: BusinessMan.
 ru
ruГальваника – это и раздел прикладной науки «Электрохимия», в котором изучаются процессы, протекающие при осаждении катионов металла на катоде, помещенном в электролитический раствор, и технологический процесс. Гальваника в домашних условиях или выполняемая на производстве позволяет наносить на поверхность обрабатываемого изделия тонкий слой металла, который может выступать в роли защитного или декоративного покрытия.
Домашняя гальваническая установка
Методы реализации такого технологического процесса, отличающегося достаточно высокой сложностью, уже хорошо отработаны, поэтому сегодня его активно используют не только производственные предприятия, но и многие домашние мастера.
Общее представление о гальванике
Гальваническое покрытие может быть как технологическим, так и декоративно-защитным. Оно представляет собой тонкий поверхностный слой металла, обладающего хорошим эстетичным видом (золото, серебро) или антикоррозионными свойствами (цинк, медь) на металлических или пластмассовых изделиях.
В общих чертах гальваника металла в домашних условиях выглядит несложно.
В ванночку с электролитом опускаются аноды, которые подключаются к «плюсу», а между ними — в качестве катода — обрабатываемая деталь, подключенная к «минусу». Когда электрическая цепь замыкается, металл, который содержится в электролите, осаждается на катод, то есть изделие.
Гальванопластика и гальваностегия
Что такое гальванопластика? Это метод, который применяется для изготовления точных копий изделий, метод копирования. Его применяют, когда необходимо сделать копию с предметов тончайшей конфигурации – пластинок, чипов и схем. Гальваностегия позволяет усилить механические свойства одного металла путем нанесения на него слоя другого металла, например, хромирование и никелирование стали, никелирование меди и т.д.
Гальванопластика и гальваностегия имеют схожую природу, отличаются лишь способом подготовки металла перед обработкой. При осуществлении гальваностегии поверхность металла должна быть максимально подготовленной для сцепления с наносимым металлом. Метод гальванопластики, наоборот, подразумевает свободное отделение наносимого металла.
Метод гальванопластики, наоборот, подразумевает свободное отделение наносимого металла.
Для гальванопластических процессов применяют чаще всего медь, никель и серебро, а в гальваностегических – практически все виды металлов. Гальванопластика в домашних условиях проводится на том же оборудовании, что и другие гальванические процессы.
Под гальванопластическую ванну прекрасно подойдет большая стеклянная емкость.Её размеры зависят от величины гальванизируемого предмета, поскольку он не должен располагаться слишком близко от анодной пластины.
Гальванопластика дома может применяться для изготовления копий предметов небольшого размера по предварительно отлитым из легкоплавких металлов формам.
Мастер-класс по гальванике (1 видео)
Предметы с гальваническим покрытием (17 фото)
Оборудование для гальваники
В домашних условиях и оборудование можно сделать своими руками. В первую очередь нужен источник питания, так как процесс протекает под действием электрического тока. В показателях силы тока домашние мастера расходятся, называя их в очень большом диапазоне. Но обязательным условием является наличие регулятора напряжения для плавного изменения выходной мощности. Ток должен быть постоянным, поэтому в качестве источника называют выпрямитель собственного или заводского изготовления.
В показателях силы тока домашние мастера расходятся, называя их в очень большом диапазоне. Но обязательным условием является наличие регулятора напряжения для плавного изменения выходной мощности. Ток должен быть постоянным, поэтому в качестве источника называют выпрямитель собственного или заводского изготовления.
Умельцы приспосабливают сварочный аппарат для гальваники в домашних условиях.
Для электролита нужна емкость (ванночка) из химически нейтрального материала. Это может быть стеклянная или пластиковая посудина достаточных размеров, чтобы в нее помещалась для обработки деталь и необходимое количество электролита. Она должна выдерживать высокую, до 80 °С, температуру и быть достаточно прочной.
Еще нужны аноды, площадь которых должна быть больше площади детали. Они служат для подвода электрического тока в электролит и его равномерного распределения по детали. Кроме того, они должны в электролите возмещать убыль металла, который выделяется при покрытии изделий, и выполнять некоторые окислительные процессы.
Нагревательные приборы для доведения электролита до нужной температуры лучше использовать с возможностью регулирования тепловых режимов. Например, бытовая газовая плита для этой цели не подходит. Обычно используют маленькую электроплитку и утюг, в котором можно установить необходимую температуру подошвы.
Оборудование для приготовления электролита
Для хранения химических реактивов и электролитов нужна стеклянная посуда с притертыми крышками.
Для приготовления электролитов необходимые вещества нужно отмерять с точностью до одного грамма. Для этого нужны соответствующие весы. Их можно приобрести или изготовить самостоятельно, используя в качестве гирек советские монетки, номинал которых точно соответствует массе.
Гальваника в домашних условиях – это и приготовление электролита из добытых непростым путем химических реактивов. Специализированные фирмы, торгующие такими высококачественными веществами, не редкость, но их деятельность подконтрольна, и работа с ними требует наличия специальных разрешительных документов даже для юридических лиц. Частным лицам опасные химические вещества не продают.
Частным лицам опасные химические вещества не продают.
Технология хромирования деталей
Существуют следующие виды хромирования:
- В электролитической среде. Атомы Cr осаждаются на токопроводящие наружные слои металла. Реакция протекает при подаче напряжения на электроды. Образуемый слой отличается стойкостью к химически активным средам и механическим воздействиям.
- Химическое хромирование. Это восстановительная реакция хрома из солевого раствора в присутствии реагентов. Наличие фосфора позволяет избавиться от серого оттенка на металле. Метод требует обязательного использования защитной экипировки.
- Декоративное хромирование с применением гальванической кисти. Метод простой и не требует наличия опыта проведения подобных работ. Контроль толщины происходит одновременно с процедурой нанесения хромового покрытия.
Подготовка изделия к гальванике
Собрав все необходимое (найдя в гараже, закупив и смонтировав своими руками), можно приступать к подготовке детали. Этот этап работ очень ответственный. Успешная гальваника в домашних условиях требует тщательной очистки детали. От подготовки поверхности зависит и качество гальванического покрытия. Поэтому, в зависимости от желаемого результата, деталь не только обезжиривают. Во многих случаях требуется пескоструйная обработка, затем шлифовка с помощью наждачной бумаги и шлифовочных паст.
Этот этап работ очень ответственный. Успешная гальваника в домашних условиях требует тщательной очистки детали. От подготовки поверхности зависит и качество гальванического покрытия. Поэтому, в зависимости от желаемого результата, деталь не только обезжиривают. Во многих случаях требуется пескоструйная обработка, затем шлифовка с помощью наждачной бумаги и шлифовочных паст.
Для обезжиривания детали промывают либо в чистых органических растворителях, ацетоне, спирте или бензине, либо в подготовленных растворах. Например, для обезжиривания стальных или чугунных деталей используются горячие, до 90 °С, растворы с едким натром, кальцинированной содой, жидким стеклом, фосфорнокислым натрием.
А изделия из цветных металлов обрабатываются в растворах с хозяйственным мылом и тем же фосфорнокислым натрием.
Окисную пленку снимают в специальных декапирующих растворах с соляной или серной кислотой.
Особенности независимой процедуры
Чтобы правильно и надёжно осуществлять процесс нанесения хрома своими руками, следует принимать во внимание все характерные черты химических и физиологических преображений, которые совершаются. Большая часть химических элементов, участвующих в хромировании, представлена особенно опасными элементами, следовательно, прежде чем приступать к проведению эксперименты с хромированными покрытиями, тщательно изучить необходимо теоретическую сторону процесса.
Большая часть химических элементов, участвующих в хромировании, представлена особенно опасными элементами, следовательно, прежде чем приступать к проведению эксперименты с хромированными покрытиями, тщательно изучить необходимо теоретическую сторону процесса.
Хром придаёт плоскости замечательный наружный вид, благодаря которому продукция приобретает весьма изящный вид. Гальваника открывает большие возможности для усовершенствования декоративных, физиологических и химических качеств материалов. Хром чрезвычайно устойчив к воздействию агрессивных сред, он не темнеет под воздействием окружающей среды, благодаря этому он отыскал обширное применение при конструировании частей кузовов автомобилей и частей элементов, работающих в сложных условиях. Толщина блестящего напыления весьма мала: от 0,075 до 0,25 миллиметров.
В отличие от никеля, в основной массе случаев хром не используют к металлу. Для этого применяют лёгкий слой оцинковки. Такого рода слой состоит из меди и требует применения технологических воздействий, усложняя и без того трудный процесс.
Ещё одна проблема, которая может остановить на пути к осуществлению задачи — получение реактивов. Главным компонентом является соединение хрома (CrO3), иное наименование — ангидрид хрома. Неприятной чертой его применения является то, что оксид хрома является самым мощным ядом, смертельная доза которого — 6 г. Это соединение имеет небольшой оборот, который строго контролируется государством.
Остатки, возникающие в результате завершения хромирования, должны быть утилизированы в соответствии со специальным порядком, а не поступать в канализацию или в почву. Элемент является сильным канцерогеном: если он появляется на коже, будет очень сильное раздражение, в том числе экзема и дерматит, может сформироваться опухоль.
Техника безопасности при работах
Гальваника в домашних условиях (хромирование, меднение, никелирование) — процесс опасный. Во-первых, из-за токсичности используемых веществ. Во-вторых, из-за необходимости нагрева растворов до высоких температур. А в-третьих, из-за риска, с которым связаны любые электрохимические процессы.
А в-третьих, из-за риска, с которым связаны любые электрохимические процессы.
Не стоит воспринимать термин «в домашних условиях» буквально. Лучше заниматься гальваникой в гараже или другом нежилом помещении с хорошей вентиляцией. Используемое электрическое оборудование нужно обязательно заземлять.
И очень важно позаботиться о личной безопасности. Ни в коем случае нельзя что-либо пить или есть во время процесса, чтобы не наглотаться заодно и вредных испарений.
Работать нужно в респираторе, резиновых, прочных и мягких перчатках, плотном клеенчатом фартуке и обуви, защищающей кожу ног. Нужно беречь глаза, чтобы в них не попали мелкие брызги реактивов. Не будет лишним и перечитать специальную литературу по этой теме, чтобы подготовиться к возможным неожиданностям.
Никелирование металлических изделий
Никелирование может быть финишным или промежуточным (перед хромированием) покрытием. Этот процесс не вызывает особых сложностей, поверхности имеют красивый внешний вид, стойки к атмосферным воздействиям.
Температура электролита не выше 25 °С при плотности тока до 1,2 А/кв. дм.
В электролит входят водные растворы сернокислого никеля, натрия и магния, чистая поваренная соль (хлористый натрий) и борная кислота.
Необходимую кислотность электролита – 4-5 рН – проверяют лакмусовой бумагой. Она должна окраситься в красный цвет. Процесс занимает около получаса в зависимости от плотности тока и толщины наносимого покрытия.
После окончания процесса изделие нужно промыть в воде, высушить и отполировать на войлочном круге с полирующей пастой.
Хромирование изделий из металла
Хромируют металлические детали для повышения их твердости и стойкости к коррозии, для получения декоративного эффекта. Из-за пористости хромового покрытия перед его нанесением сначала выполняется гальваника медью в домашних условиях или никелирование, а то и поочередное нанесение этих покрытий.
Стабильный процесс хромирования обеспечивают аноды, изготовленные из сплава свинца с оловом и сурьмой в пропорциях 85%:11%:4% соответственно.
Как гальваника в домашних условиях, хромирование сложней и многообразней никелирования. Во-первых, от температуры электролита зависит оттенок покрытия. При температурах в диапазоне от 35 до 55 °С оно блестящее, выше 55 °С – молочное, ниже 35 °С – матовое.
Во-вторых, от состава электролита зависит цвет и физические параметры хромового покрытия. Оно может быть обычным защитным, темно-голубым, агатовым, синим или даже черным декоративно-защитным.
Износостойкое защитное покрытие в домашних условиях выполнить сложно, так как нужны токи высокой плотности – до 100 А/кв. дм.
При комнатной температуре и плотности тока до 5 А/кв. дм получается декоративное мягкое покрытие.
После завершения гальванического процесса хромирования деталь промывают в воде, затем нейтрализуют в легком растворе обычной пищевой соды, опять тщательно промывают, сушат и полируют со специальными пастами.
Основные методы хромирования
- Процесс химической металлизации.
- Гальванизация.

- Вакуумное напыление.
- Высокотемпературная диффузия.
Два последних метода применяются только на предприятиях промышленности. Дома эти процессы выполнить не получится, поскольку для них необходимы технически сложные установки и повышенные энергетические затраты. А вот химическая металлизация и гальванизация – это как раз те самые процессы, которые могут производиться и в личной мастерской. Рассмотрим подробно, как это делается.
В процессе этой работы используются химические реактивы, компрессор и краскопульт. Выполняются практически те же самые операции, что и при покраске поверхностей акриловым лаком либо эмалью. При хромировании таким способом на детали и конструкции наносится не защитная полимерная пленка, а зеркальный тонкий слой металла.
1-й метод. Поверхность покрывается специальными химикатами. В результате химической реакции образуется осадок, представляющий собой прочный металлический слой. Покрытие можно делать не только из хрома, но также из серебра.
2-й метод. В процессе восстановительной химической реакции из солей образуется слой хрома. Приготовьте набор из уксусной кислоты, хлористого хромила, хлористого хрома, уксуснокислого хрома, гипософита натрия, едкого натра, фосфата хрома. При этом необходимо помнить, что эти вещества очень ядовиты и опасны для здоровья.
И потому следует внимательно проштудировать учебник химии, если уж вы решили провести процесс хромирования этим методом. Но достичь высокого качества очень трудно, даже при наличии подробной инструкции. При всех существующих минусах этот метод используется для хромирования поверхностей в домашних мастерских чаще всего.
Очень удобно проводить процесс покрытия с помощью готовых пробных наборов химических препаратов для хромирования. Их предлагает компания Fusion Technologies. Удобство таких наборов заключается в том, что покрытие можно нанести на любой из перечисленных материалов: металл, керамику, дерево, стекло, пластик.
Получение бракованного покрытия не должно пугать начинающего гальваника. Некачественный слой хрома можно снять в растворе соляной кислоты (100-200 г/л). После этого детали промываются в воде, а процесс хромирования можно повторить.
Чаще всего встречается несколько основных дефектов:
- Отслаивание хромовой пленки. Главной причиной является плохая адгезия (сцепляемость) из-за недостаточного обезжиривания. После снятия покрытия поверхность заново очищается и активируется.
- Наросты (дендриты) хрома на острых краях и углах. Этот дефект свидетельствует о высокой плотности тока на острых гранях. Если можно, края лучше закруглить или установить экраны в проблемных зонах.
- Матовое покрытие. Чтобы добиться блеска, необходимо повысить температуру раствора, снизить силу тока или добавить хромовый ангидрид.
Меднение металлических изделий
Для чего еще может понадобиться гальваника в домашних условиях? Меднение производят для нанесения на поверхность тонкого токопроводящего слоя с малым сопротивлением или для защиты основного металла детали.
Наносить медь на черные металлы в домашних условиях, так как в этом процессе используются цианистые электролиты, смертельно опасно. Поэтому стальные или чугунные детали сначала никелируют, а только потом покрывают медью в электролитах из раствора медного купороса и концентрированной серной кислоты в воде комнатной температуры. Плотность тока при этом невысокая – до 2 А/кв. дм.
Алюминиевые детали тоже требуют предварительной подготовки. Их сначала декапируют (очищают от окисной пленки), затем оксидируют в электролите из водного раствора серной кислоты, затем тщательно промывают. Только потом выполняется гальваника в домашних условиях — меднение в электролите из медного купороса и водного раствора серной кислоты при достаточно низких температурах, до 20 °С, и низкой плотности тока. В качестве анода используется обычная медная пластина подходящей площади.
Причины дефектов покрытия
Существует несколько дефектов:
- Неравномерный блеск – слишком большая сила тока или низкая температура раствора.

- Отсутствие блеска – недостаточное количество серной кислоты или ангидрида.
- Появление коричневых пятен – недостаток серной кислоты или избыток хромового ангидрида.
- Низкая прочность покрытия – низкая сила тока или завышенная температура электролита.
Таблица дефектов при хромировании
Серебрение и золочение изделий
Гальваническое серебрение – это не только декоративное, но и защитное, и электропроводящее покрытие с хорошей отражающей способностью. Изделия из черных металлов предварительно покрываются никелем, на который уже осаждается серебро.
Электролит для серебрения состоит из хлористого серебра, железноцианистого калия, кальцинированной соды и дистиллированной воды. Рабочая температура электролита не выше 20 °С, не требуется и высокая мощность тока – она не больше 0,1 А/кв. дм. В качестве анода используются графические пластины.
Наиболее декоративная и потому соблазнительная гальваника в домашних условиях — золочение. Процесс производят в горячих растворах золота (до 5 г на литр воды) с синеродистым калием. В холодных растворах количество металла нужно увеличивать втрое. Пары синеродистой кислоты очень ядовиты, поэтому процесс золочения в горячем растворе необходимо производить только в помещениях с мощной принудительной вытяжкой.
Процесс производят в горячих растворах золота (до 5 г на литр воды) с синеродистым калием. В холодных растворах количество металла нужно увеличивать втрое. Пары синеродистой кислоты очень ядовиты, поэтому процесс золочения в горячем растворе необходимо производить только в помещениях с мощной принудительной вытяжкой.
При работе с холодным раствором с синеродистой кислотой тоже нужно соблюдать предельную осторожность: не склоняться над ванной, не совать в нее руки, особенно со свежими ссадинами или царапинами.
Еще лучше ядовитую кислоту заменить желтой кровавой солью, то есть железистосинеродистым калием. Перед приготовлением электролита обычное золото превращают в хлорное при помощи царской водки, если, конечно, нет возможности приобрести готовое.
Как сделать гальванику в домашних условиях? Нужно тщательно очистить изделие. Затем, если оно выполнено из свинца, олова, железа, цинка или стали, его нужно предварительно покрыть медью. Затем для того, чтобы облегчить приставание золота, предмет нужно окунуть в раствор азотнокислой ртути.
Плотность тока должна быть не выше 1 А/кв. дм, так как при более сильных токах золото из электролита оседает на дно ванны в виде черного порошка, а позолота на изделии становится буроватого цвета.
Для того чтобы была красивой позолота, нужно у анода подвесить достаточно большой листик золота. После завершения гальванического процесса позолоченное изделие нужно просушить в опилках и отполировать.
Подготовка обрабатываемой детали
Качество и долговечность нанесённого слоя хрома зависит от подготовки окрашиваемой детали. Хромированная поверхность должна идеально удовлетворять все требуемые параметры очистки. Этим можно заняться пока готовый раствор отстаивается после «проработки» электрическим током.
Очистка и обезжиривание
Металлическая деталь должна быть полностью очищена от любого мусора, лакокрасочного покрытия, грунтовки, ржавчины и т. д. Отнестись к этому этапу подготовки следует с особым вниманием, ведь от этого зависит качество хромирования. Даже если деталь подвергалась частой покраске, справиться с этим поможет наждачная бумага или специальная шлифовальная машина. При использовании абразивных насадок или жёстких дисков аналогичных наждачной бумаге очистить поверхность металлического изделия не составит труда. Шлифовальная машина поможет даже сгладить все царапины и сколы, сделав поверхность идеально ровной.
При использовании абразивных насадок или жёстких дисков аналогичных наждачной бумаге очистить поверхность металлического изделия не составит труда. Шлифовальная машина поможет даже сгладить все царапины и сколы, сделав поверхность идеально ровной.
После того как поверхность полностью очищена от грязи и краски, следует перейти к обезжириванию. От качества этой процедуры также зависит качество нанесения слоя хрома.
Обезжиривание — это приготовление специального раствора, который включает следующий компоненты:
- гидроокись натрия — 150 г/л;
- кальцинированная сода — 50 г/л;
- силикатный клей — 5 г/л.
После замешивания раствора для обезжиривания деталей он нагревается до температуры 80−90 градусов по Цельсию. Изделия в нём выдерживаются в течение 20 минут, но если поверхность отличается сложным рельефом или сильно загрязнена, то время увеличивается до 1 часа.
Гальваника в домашних условиях
Подводя итоги о возможности нанесения гальванического покрытия в домашних условиях, можно сказать, что человеку, не разбирающемуся в электрохимии хотя бы на начальном уровне, организовывать процесс не стоит – слишком опасно. Кроме информации на различных сайтах и форумах, нужно обязательно читать специальную литературу. К тому же частное лицо не имеет доступа к реактивам. Поэтому, если нужно восстановить хромирование на одной детали, значительно дешевле обратиться к специалистам.
Кроме информации на различных сайтах и форумах, нужно обязательно читать специальную литературу. К тому же частное лицо не имеет доступа к реактивам. Поэтому, если нужно восстановить хромирование на одной детали, значительно дешевле обратиться к специалистам.
Ну а если уж очень хочется освоить новое производство самостоятельно, то тоже нужно попросить о помощи профессионалов, которые подберут необходимое безопасное оборудование (ведь производство не должно быть совсем уж кустарным), блоки питания, электролиты, не содержащие токсичных веществ, рассчитают параметры ванн и анодов. А также обучат процессам нанесения металлического покрытия, всем тем процедурам (их ведь не так много), которые приводят к желаемому результату.
Гальваника для лица в домашних условиях
После всего описанного выше такое название звучит несколько угрожающе. На самом же деле это всего лишь глубокое очищение кожи с помощью гальванических токов малой мощности. Под воздействием этих токов кожные жиры растворяются и выходят на поверхность лица, покрытого специальным составом, взаимодействуя с которым, превращаются в мыло.
Гальванические токи в медицине используются для усиления работы ионов. Это активно заряженные частицы, отвечающие за многие рабочие процессы в клетках. Под воздействием постоянного тока ионы перемещаются, улучшается проницаемость клеточных мембран, запускается выработка волокон коллагена и эластина, увеличивая прочность, упругость и эластичность кожи.
Гальванические токи проводят в глубокие слои дермы косметические средства с собственным электрическим зарядом. То есть процесс оздоровления кожи проходит изнутри, исчезают глубокие морщины, сужаются расширенные поры, кожа усиленно насыщается кислородом.
Аппарат «Гальваника + микротоки» в домашних условиях M365 Gezatone на сегодня наиболее доступная модель косметологического прибора нового поколения. Он помогает избавиться от угрей, разгладить морщины на увядающей коже, снизить проявления сосудистой сеточки, укрепить сосуды, улучшить контуры лица, убрать второй подбородок.
Процедура гальванической чистки лица
До начала процедуры кожу очищают обычными средствами: молочком или гелем. Затем наносят щелочной состав. Затем начинается непосредственно гальваника в домашних условиях. Gezatone Beauty Lifting — специальный аппарат для процедуры не только гальванической чистки, но и для введения в кожу питательных веществ под действием тех же токов. Процедура длится около пятнадцати минут – только круговые движения наконечником вдоль массажных линий лица, и ничего более – затем образовавшееся при реакции жиров со щелочью мыло смывается теплой водой.
Затем наносят щелочной состав. Затем начинается непосредственно гальваника в домашних условиях. Gezatone Beauty Lifting — специальный аппарат для процедуры не только гальванической чистки, но и для введения в кожу питательных веществ под действием тех же токов. Процедура длится около пятнадцати минут – только круговые движения наконечником вдоль массажных линий лица, и ничего более – затем образовавшееся при реакции жиров со щелочью мыло смывается теплой водой.
Но токи есть токи, даже с приставкой «микро». Запрещено проходить процедуру гальванической чистки людям с вживленным кардиостимулятором, онкологическими заболеваниями, невротическими состояниями, болезнями кожи.
Настолько ли эффективна, как утверждают производители, гальваника для лица в домашних условиях, отзывы женщин, пользующихся приборами, с уверенностью утверждать не могут. Как правило, дамы спешат поделиться впечатлениями в первые месяцы после покупки, когда еще не так ощущаются последствия. Но все равно отзывы оптимистические.
В заключение можно сказать, что гальваника в домашних условиях – это не только опасный для здоровья процесс нанесения металлического покрытия на изделия, который в собственно жилом помещении осуществлять не стоит, но и современная безболезненная, безопасная и достаточно эффективная процедура омоложения кожи лица, шеи и зоны декольте.
технология и оборудование. Меднение металла в домашних условиях
Медь является одним из самых широко применяемых металлов в мире, еще издавна этот материал применяли для изготовления орудий труда. Такое активное использование меди обусловлено ее уникальными техническими и эксплуатационными свойствами. В настоящее время без меди невозможно существование таких отраслей производства, как металлургия, автомобильная промышленность, электротехника и строительство. Этот материал необходим и в бытовых условиях, именно поэтому многих так интересует, как проводить меднение в домашних условиях.
Под меднением принято понимать гальваническое нанесение меди, при этом толщина слоя должна находиться в рамках от одного до трехсот микрометров. Меднение – это покрытие медью металлического изделия в качестве подготовки к хромированию, использованию никеля или серебра. Однако данная процедура может использоваться и как самостоятельная обработка поверхности.
Меднение – это покрытие медью металлического изделия в качестве подготовки к хромированию, использованию никеля или серебра. Однако данная процедура может использоваться и как самостоятельная обработка поверхности.
В качестве подготовительного процесса меднение стали способствует выравниванию поверхности, ведь, как известно, медь прочно держится на стали, чего не скажешь о других материалах. Различные металлы достаточно хорошо осаждаются на омедненное покрытие (намного лучше, чем на чистую сталь).
К отличительным характеристикам медного покрытия специалисты относят высокое сцепление с иными металлами, пластичность и надежность. Однако при постоянном воздействии факторов окружающей среды медное покрытие быстро окисляется и покрывается радужными разводами, пятнами и налетом.
Меднение можно производить на поверхностях из стали, цинка и даже алюминия. Только что нанесенный слой меди имеет малиновый оттенок со слегка заметным металлическим блеском.
Где используется?
Выделяют несколько основных случаев применения меднения:
- Для декорирования.
 В последнее время увеличился спрос на старинные медные изделия. При помощи специальной обработки нанесенный слой меди придает поверхности «состаренный вид».
В последнее время увеличился спрос на старинные медные изделия. При помощи специальной обработки нанесенный слой меди придает поверхности «состаренный вид». - Данный способ нанесения железа используется для производства копий отдельных медных деталей различных форм и размеров. Сначала создается основа из воска или пластика, которую в последствии покрывают электропроводящим раствором и медным слоем. Такая технология широко применяется при изготовлении сувенирной продукции, ювелирных изделий, а также барельефов и волноводов.
- В электротехнике. Низкая стоимость меднения выгодно выделяет этот метод – по сравнению с покрытиями из серебра или золота, медные изделия могут применяться в электротехнических отраслях (для производства электродов, контактов под напряжением и в качестве основы под пайку).
Технологию меднения также совмещают с различными типами гальванизации:
- Для создания многослойного декоративного покрытия со слабыми защитными характеристиками.
 В таком случае используется медь, хром и никель – трехслойный защитно-декоративный слой, который повышает степень сцепления с основным материалом поверхности.
В таком случае используется медь, хром и никель – трехслойный защитно-декоративный слой, который повышает степень сцепления с основным материалом поверхности. - Для защиты определённого участка детали при цементации. При гальванизации свинцовых изделий медью необходимо предохранение покрытий стальных элементов от науглероживания. Меднению поддаются только те участки, которые в дальнейшем будут подвергаться механической обработке.
- При реставрационных работах. В процессе омеднения на восстанавливаемой детали образуется промежуточный слой, который в дальнейшем послужит основой для более прочного покрытия (хромирования, никелирования). Для гальванического способа характерно нанесение толстого слоя меди, до двухсот пятидесяти микрометров. Это связано с необходимостью ликвидации всех повреждений и дефектов поверхности.
На видео: гальваническое меднение в декоративных целях.
Особенности процесса в быту
Омеднение металлических предметов носит название – гальваностегия. Принцип заключается в погружении предмета в раствор электролита с осажденным медным купоросом.
Мало кто знает, что гальванизацию можно проводить и в домашних условиях, для этого не требуется наличие специального оборудование. Данная операция способствует подготовке поверхности к последующим обработкам либо служит промежуточной стадией при нанесении никеля, хрома, латуни.
Принцип заключается в погружении предмета в раствор электролита с осажденным медным купоросом.
Мало кто знает, что гальванизацию можно проводить и в домашних условиях, для этого не требуется наличие специального оборудование. Данная операция способствует подготовке поверхности к последующим обработкам либо служит промежуточной стадией при нанесении никеля, хрома, латуни.
Изделия, обработанные таким способом, с добавлением в медь других металлов, весьма устойчивы к агрессивным факторам. Меднение не предполагает особых навыков и профессиональных знаний, однако есть несколько нюансов, которые необходимо учитывать.
В быту осуществляется именно химическая гальванизация небольших деталей, поскольку она не требует больших финансовых затрат и дополнительного оборудования.
На видео: принцип меднения металлических предметов.
Как проводится химическое меднение на дому?
Чтобы нанести медь в домашних условиях, вам в первую очередь необходимо приготовить рабочий раствор и создать два разноименных электрода, так как в процессе омеднения ионы меди, находящиеся в электролитическом растворе, будут притягиваться к отрицательному полюсу. Нанесение на металлическую поверхность меди в промышленных условиях и в промышленных масштабах чаще всего используется как завершающая операция в обработке изделия.
Нанесение на металлическую поверхность меди в промышленных условиях и в промышленных масштабах чаще всего используется как завершающая операция в обработке изделия.
Однако если вы собираетесь проводить меднение металла собственными силами, то должны знать порядок работы. Далее мы рассмотрим, как покрыть деталь медью в домашних условиях химическим способом с погружением в раствор электролита. Этот процесс легко можно выполнить на дому, если знать все особенности применения меди. Алгоритм выполнения:
1. Для растворителя меди на металле можно взять обычный аккумуляторный электролит. Он продается в любом хозяйственном магазине, однако его можно изготовить и собственными силами. Необходимо соблюдать пропорцию 100:3 дистиллированной воды и серной кислоты с поправкой на необходимый объем электролита. Затем в смесь добавляется до 20 грамм сульфата меди (медный купорос).
Важно! К медному купоросу могут добавляться и другие специализированные составы, в зависимости от конченой цели.
2. Предварительно деталь необходимо очистить абразивными материалами, для удаления оксидного слоя. Далее поверхность покрываемой детали обезжиривается горячим раствором карбоната натрия и промывается проточной водой (чтобы на металлах не скапливались различные загрязнения).
3. Гальванизационная емкость заполняется электролитическим раствором до нужного объема, после чего в раствор помещаются две медные пластины (на покрытиях которых будут образовываться ионы меди) на проводниках, а между ними размещается деталь, предназначенная для омеднения.
4. Концы проводников и подвесы для детали подключаются к источнику тока, в качестве которого могут выступать гальванические элементы либо аккумуляторные батареи (плюс на пластины, минус на деталь). В цепь предварительно необходимо последовательно подключить амперметр и реостат.
5. Процесс гальванизации занимает от пятнадцати до двадцати минут, после чего нужно отключить электропитание и извлечь деталь из раствора. Этого времени достаточно чтобы деталь покрылась тонким слоем меди. Для получения более толстого покрытия необходимо увеличить продолжительность процесса. Металлическая поверхность становится более прочной, повышаются ее технические и эксплуатационные свойства.
Этого времени достаточно чтобы деталь покрылась тонким слоем меди. Для получения более толстого покрытия необходимо увеличить продолжительность процесса. Металлическая поверхность становится более прочной, повышаются ее технические и эксплуатационные свойства.
Как сделать раствор для домашнего меднения (3 видео)
Детали покрытые медью (25 фото)
Освоить технологию гальванического покрытия металлами материалов можно довольно быстро, для этого не потребуются обширные познания в физике или химии, а вот представление о том, что вы хотите получить «на выходе» — все же желательно иметь:)
Сам принцип омеднения заключается в осаждении меди на поверхности предмета-основы с помощью электро-химической обработки формы-полуфабриката.
По большому счету, доступный способ покрытия форм медью — всего один.
Технология омеднения различных неметаллических предметов называется «гальванопластика» («электроформинг» — западный аналог названия). Гальванопластическим способом вполне возможно изготовить самые разнообразные детали украшений.
Необходимым условием получения качественного медного покрытия является точное соблюдение технологии меднения. Итак, перейдем к созданию установки для омеднения.
Омеднение (меднение) производят в емкостях, имеющих обычно округлую или прямоугольную форму. Другая форма емкости так же не помешает процессу. Объем емкости определяется размером и количеством изделий (предметов), подлежащих меднению. Вполне подходят глазурованные емкости из керамики, стекла или пластмассы .
Вам понадобится источник постоянного тока низкого напряжения (от 2 до 6В). Для этого идеально подходит выпрямители для зарядки аккумуляторов, а если такового в вашем хозяйстве не обнаружилось, то сойдут и аккумуляторные батареи или элементы питания (батарейки).
Силу тока регулировать можно с помощью ползункового реостата (не пугайтесь, его можно заметить подходящим переменным резистором, это выглядит как регулятор громкости, такая ручка или бегунок).
Так же понадобится мультиметр для контроля силы тока (от 0 до 3-5 ампер) и для измерения напряжения. Как правило, амперметр на зарядных устройствах все же присутствует и отдельно его приобретать не нужно.
Для создания электролита запаситесь медным купоросом и серной кислотой . Вместо серной кислоты прекрасно подходит электролит, которым обычно заправляют аккумуляторы для автомобилей.
Для нанесения токопроводящего слоя на поверхность детали, подлежащей омеднению, потребуется токопроводящий лак .
В качестве анода можно использовать медные пластины , а за неимением таковых — обычную медную проволоку — жилу, добытую из обычного силового кабеля, который можно купить в любом магазине электротехнических товаров. Площадь этой пластины или проволоки должна быть примерно равна площади покрываемого медью предмета, в любом случае — чем она больше, тем лучше. Задача анода — потихоньку растворяться, отдавая медь в раствор
Еще для омеднения необходим будет этиловый спирт .
Электролит приготавливается следующим образом :
на 1 литр воды берется 230-250 грамм медного купороса и 40-50 мл. серной кислоты (серную кислоту можно приобрести в виде состава с названием «Электролит» в авто и хозяйственных магазинах).
* Будьте осторожны при обращении с электролитом — он может повредить кожу, глаза и даже ткань одежды.
* Следует помнить, хотя растворы не содержат сильно ядовитых веществ, но обращаться с ними все же следует с определенной осторожностью, чтобы не получить отравление или ожог.
* Растворы целесообразно хранить в темной стеклянной емкости с хорошо закрывающейся крышкой (но прекрасно подойдет и обычная пластиковая бутылка).
Гальваника представляет собой раздел электрохимической науки, которая изучает осаждение некоторых элементов на любую поверхность. С помощью гальваники в домашних условиях или в промышленности можно нанести на изделие тонкий слой металла, который будет выступать в роли защитного слоя или выполнять декоративные функции. В последнее время декоративное покрытие набирает популярность у тех, кто хочет сделать оригинальный подарок своим друзьям и родным.
Общие сведения
Покрытие гальваникой бывает технологическим или декоративно-защитным. Это тонкий металлический тонкий слой, который в зависимости от гальванических элементов может выполнять эстетические функции. Гальванопластика не увеличивает прочность изделия, поскольку в этом случае требуются большие производственные мощности, но для красоты и придания «свежести» вполне подойдет.
Гальванические реакции происходят с помощью постоянного электрического тока. В специальную емкость-диэлектрик наливают раствор — электролит, в который погружают два анода. Аноды должны быть изготовлены из металла, который будет осаждаться на покрываемом изделии.
Обрабатываемая деталь присоединяется к минусовому выводу и помещается между анодами. Она выполняет роль катода. Аноды, в свою очередь, присоединяются к плюсовому контакту источника питания. Они становятся частью цепи, проводя ток в электролит и отдавая ему свои металлические элементы. Электролит передает необходимые частицы обрабатываемой детали, они постепенно обволакивают её тонким слоем. Аноды по площади должны превышать в несколько раз размер заготовки.
Другими словами, гальванизация представляет собой перенос молекул металла раствора на изделие в момент протекания через них электротока.
Любой гальванический процесс можно разбить на общие этапы:
- Сборка гальванической установки.
- Подготовка электролитного раствора.
- Обработка и подготовка образца.
- Запуск гальванического процесса.
Оборудование можно подготовить самостоятельно. Сначала подбирается подходящий источник питания. Это может быть батарейка (для обработки изделий небольшого размера) или аккумулятор. Подойдет понижающий блок питания, который выдает на выходе постоянный ток до 12 вольт. Иногда используют инвертор от сварочного аппарата. Подбирается реостат для регулирования силы тока.
Из нейтрального, устойчивого к химически агрессивным веществам материала подбирается широкая и глубокая ванночка. Надо учитывать, что электролитический раствор при гальваническом процессе может нагреваться до девяноста градусов по Цельсию.
Подготавливаются две пластины, которые будут токопроводящими анодами.
Для нагрева ёмкости с электролитом нужен электрический прибор с возможностью плавной регулировки температурного режима. Чаще всего используют подошву утюга или небольшую электроплитку. С их помощью происходит нагрев раствора до необходимой температуры и ускорение реакции.
Химические реактивы необходимо хранить в плотно закупоренной стеклянной посуде. Желательно каждый предмет подписывать.
Потребуются весы для точного измерения массы веществ, поскольку необходимая точность веса компонентов составляет один грамм. Такие весы можно приобрести, а можно сделать самостоятельно, используя вместо гирек старые советские монеты. Вес «желтых» монет точно соответствует их номиналу.
После того как собраны необходимые вещества, найдены ёмкости, собрана электрическая схема с питанием и подготовлена система подогрева, можно заняться чисткой заготовки.
Если недостаточно хорошо почистить деталь, гальваническое покрытие непрочно осядет или будет неравномерным. Иногда хватает простого обезжиривания предмета. Раствор ацетона или спирта может хорошо обезжирить поверхность, можно использовать бензин.
Некоторые мастера держат изделия из стали в разогретом до 90 градусов по Цельсию растворе фосфорнокислого натрия. Цветные металлы можно очищать в том же растворе, не нагревая его.
Если на изделии есть коррозия или другие изъяны, то поверхность заготовки шлифуется наждачной бумагой.
Иногда про технику безопасности при различных работах в домашних условиях рассказывают вскользь. Но при выполнении любых гальванических работ нужно строго соблюдать безопасность.
Опасность заключается в использовании токсичных химических веществ, высокой температуре нагрева раствора и повышенными рисками, которые сопровождают электрохимические реакции.
Лучше всего гальванические работы проводить в гараже или мастерской при обязательном проветривании или вентилировании помещения. Особое внимание следует уделить заземлению оборудования. Нужно соблюдать меры личной безопасности, а именно:
- Дыхательные пути следует защитить респиратором.
- Руки и запястья должны быть спрятаны в высокие и прочные резиновые перчатки.
- Обувь должна защищать от ожогов, а одежда прикрыта клеенчатым фартуком.
- Обязательно ношение специальных защитных очков.
Перед началом работ по меднению в домашних условиях нужно подготовить необходимые материалы и оборудование. Надо позаботится об источнике напряжения и постоянного тока. Существует много рекомендаций касательно силы тока, разброс которого может быть большим. Поэтому желательно иметь реостат с возможностью плавной регулировки напряжения и для постепенного завершения процесса. Источником может служить автомобильный аккумулятор или выпрямитель с напряжением на выходе не больше 12 вольт. Для первых опытов будет достаточно обычной батарейки от 4.5 до 9 вольт.
Затем выбирается ёмкость для электролитического раствора, лучше всего из жаропрочного стекла. В любом случае все ёмкости для электролиза должны быть диэлектриками и выдерживать температуру не менее, чем 80 градусов по Цельсию.
В качестве анодов подойдут два больших медных листа. Они должны перекрывать по размеру заготовку. Из химических реактивов потребуются:
- Купорос медный.
- Кислота соляная либо серная.
- Вода дистиллированная.
Меднение в домашних условиях пользуется заслуженной популярностью, поскольку очень хорошо и надежно держится на стальных изделиях. Главное условие — правильно соблюдать технологию процесса.
Имеется два способа нанесения меди на поверхность:
- Помещение заготовки в раствор электролита.
- Неконтактный способ. В этом случае изделие не погружается в раствор.
Подготавливается и обрабатывается поверхность изделия при помощи тонкого наждака и щеточки. После этого деталь моется в проточной воде, обезжиривается и еще раз промывается.
Этапы процесса омеднения следующие:
- Два медных анода подключают в сеть к положительным контактам и размещают их в стеклянную банку.
- К обработанному изделию подводят контакт с отрицательным значением напряжения и свободно подвешивают между анодами.
- Подключают реостат согласно электрической схеме для возможности регулирования силы тока.
- Подготавливается раствор в правильных пропорциях. На 100 г дистиллированной воды надо 20 г медного купороса и 2−3 г соляной кислоты. Вместо соляной кислоты можно использовать другую.
- Раствор выливается в посуду с медными пластинами и деталью таким образом, чтобы они полностью скрылись под поверхностью раствора.
- Подключается источник напряжения. Реостатом добиваются необходимой силы тока из примерного расчета 10−15 миллиампер на каждый квадратный сантиметр площади детали.
Весь процесс занимает примерно 15−20 минут. После обязательного выключения источника питания и остывания раствора готовое изделие с медным слоем на поверхности вынимается из банки.
Этот метод интересен тем, что его можно использовать для обработки не только стальных предметов, но и сделанных из других материалов. Например, алюминия и цинка. Порядок процесса следующий:
- Из многожильного медного провода изготавливается «кисточка». Конец провода оголяется. Из медных проводков создается подобие кисточки, чтобы затем прикрепить ее к деревянной ручке-держателю.
- Второй конец провода подключается к плюсовому контакту электрической цепи.
- В широкую ёмкость заливается стандартный электролитный раствор из медного купороса и соляной кислоты.
- Предварительно очищенная и промытая металлическая заготовка присоединяется к отрицательному контакту и размещается в пустой ёмкости.
- Импровизированная кисточка окунается в раствор электролита и проводится по поверхности заготовки без контакта. Это действие повторяется до получения результата.
Когда деталь полностью покроется слоем меди, выключается блок питания и процесс завершается. Деталь ополаскивается в воде и просушивается.
Часто с помощью медного электролиза обновляют столовые приборы, сделанные из алюминия. Если нет опыта проведения этого процесса, то можно потренироваться нанести медь на алюминиевые пластинки. Порядок проведения процесса:
Гальванопластика — это электрохимический способ придания предмету определенной формы с помощью осаждения на него металла. Чаще всего этот метод используют при обработке металлом неметаллических предметов или при изготовлении копий ювелирных изделий.
Если при гальванопластике изделие не обладает электропроводящими свойствами, то его предварительно покрывают графитом, иногда бронзой. Затем мастер делает с копии слепок и начинает гальванический процесс. В качестве материала слепка используют гипс, графит или легко плавящийся металл.
Гальваника — это очень интересный и познавательный процесс, но он связан с активными веществами, которые могут навредить здоровью и нанести вред имуществу или окружающей среде. Поэтому перед тем как начинать гальванику своими руками, нужно принять все меры безопасности, изучить немного теории процесса и особенности поведения химических реактивов.
Меднение — это процесс нанесения на поверхность медного слоя гальваническим способом.
Медный слой придает изделию внешнюю привлекательность, что позволяет использовать прием гальванического покрытия медью в дизайнерских проектах. Также он придает металлу высокую электропроводность, что позволяет подвергать изделие дальнейшей поверхностной обработке.
Меднение можно использовать в качестве основного процесса для создания поверхностного слоя, а также как промежуточную операцию для дальнейшего нанесения другого металлического слоя. К такому способу можно отнести, например, процесс серебрения, или никелирования.
Меднение можно проводить в домашних условиях. Это дает возможность решить много бытовых проблем.
Чтобы выполнить покрытие медным слоем самостоятельно, нужно приобрести необходимое для процесса оборудование и материалы.
Прежде всего, нужно подготовить источник электрического тока. Разные домашние мастера советуют использовать силу тока, разброс которой в большом диапазоне. Работа должна проводиться на постоянном токе.
В качестве источника тока можно взять батарейку КБС-Л напряжением 4,5 вольт или новую батарейку марки «Крона» с рабочим напряжением 9 вольт. Можно также вместо нее использовать выпрямитель малой мощности, дающий напряжение не более 12 вольт, или автомобильный аккумулятор.
Обязательным является использование реостата для регулировки напряжения и плавного выхода из процесса.
Для раствора электролита должна быть заготовлена нейтральная емкость, например из стекла, а также пластиковая широкая посуда, имеющая достаточные размеры для размещения в ней детали. Емкости должны выдерживать температуру не менее 80оС.
Также понадобятся аноды, обеспечивающие покрытие всей поверхности детали. Они предназначены для подведения тока в электролитный раствор и его распределение по всей площади детали.
Для проведения гальваники в домашних условиях понадобятся также химреактивы для приготовления раствора:
- медный купорос,
- соляная или другая кислота,
- дистиллированная вода.
Заготовив все необходимое, можно приступать к работе.
Меднение стальных изделий
Меднение стали медным купоросом является одним из основных процессов в области гальваники потому, что оно используется для предварительного покрытия медью. Она отличается высокой адгезией к стальной поверхности, в отличие от других металлов, которые не обладают хорошим сцеплением со сталью. Медный слой при соблюдении технологии держится на стальных изделиях прекрасно.
Есть две технологии нанесения покрытия: с погружением изделия в электролитный раствор и способ неконтактного покрытия поверхности медью без помещения в жидкий электролитный раствор.
Меднение путем погружения в раствор
Процесс выполняется с соблюдением следующих этапов:
- С поверхности стальной детали удаляется окисная пленка с помощью наждачной бумаги и щетки, а затем деталь промывается и обезжиривается содой с финишной промывкой водой.
- В стеклянную банку помещаются две медные пластины, подсоединенные к медным проводникам, которые служат анодом. Для этого их соединяют вместе и подводят к положительной клемме прибора, используемого в качестве источника тока.
- Между пластинами свободно подвешивается обрабатываемая деталь. К ней подводится отрицательный полюс клеммы.
- В цепь встраивается тестер с реостатом, чтобы регулировать силу тока.
- Готовится электролитный раствор, в состав которого обычно входит медный купорос — 20 грамм, кислота (соляная или серная) — от 2 до 3 мл, растворенная в 100 мл (лучше дистиллированной) воды.
- Готовый раствор заливается в подготовленную стеклянную банку. Он должен покрыть помещенные в банку электроды полностью.
- Электроды подключаются к источнику тока. С помощью реостата устанавливается ток (10-15 мА должны приходиться на 1см2 площади детали).
- Через 20-30 минут ток отключается, и деталь, покрытая медью, достается из емкости.
Покрытие медью без помещения в электролитный раствор
Такой способ используется не только для стальных изделий, но и алюминиевых предметов и изделий из цинка. Процесс осуществляется так:
- Берется многожильный медный провод, с одного конца которого снимается изоляционное покрытие, а проводкам из меди придается вид своеобразной кисточки. Для удобного использования «кисть» закрепляют на ручке — держателе (можно взять деревянную палку).
- Другой конец провода без кисти подсоединяется к положительной клемме используемого источника напряжения.
- Готовится электролитный раствор на основе концентрированного медного купороса с добавлением небольшого количества кислоты. Он наливается в широкую емкость, необходимую для удобного окунания кисти.
- Подготовленная металлическая деталь, очищенная от оксидной пленки и обезжиренная, помещается в пустую ванночку и подсоединяется к отрицательной клемме.
- Кисть смачивается приготовленным раствором и водится вдоль поверхности пластины, не прикасаясь к ней.
- После достижения необходимого медного слоя, процесс заканчивается, а деталь промывается и сушится.
Между поверхностью детали и импровизированной медной кистью всегда должен быть слой из раствора электролита, поэтому кисть необходимо обмакивать в электролит постоянно.
Меднение алюминия медным купоросом
Нанесение на поверхность меди — отличный способ обновления алюминиевых столовых приборов и других изделий из алюминия, используемых дома.
Меднение алюминия медным купоросом можно провести самостоятельно. Упрощенный вариант для демонстрации процесса — это покрытие медью алюминиевой пластинки простой формы.
На этом примере можно потренироваться. Выполнение процесса происходит так:
1. Поверхность пластинки необходимо сначала зачистить, а затем обезжирить.
2. Затем нужно нанести на нее немного концентрированного раствора сернокислой меди (медного купороса).
3. Следующим действием является подсоединение к алюминиевой пластинке провода, подсоединенного к отрицательному полюсу. Подсоединять провод к пластинке можно с помощью обычного зажима.
4. Положительный заряд подается на устройство, состоящее из оголенного медного провода с диаметром от 1 до 1,5 мм, конец которого распределяется между щетинами зубной щетки.
Во время работы этот конец провода не должен касаться поверхности алюминиевой пластины.
5. Обмакнув щетину в раствор медного купороса, начинают водить щеткой в подготовленном для покрытия медью месте. При этом не нужно допускать замыкания цепи, прикасаясь к поверхности алюминиевой пластины концом медного провода.
6. Омеднение поверхности сразу становится визуально заметно. Чтобы слой был качественным, с окончанием процесса не нужно торопиться.
7. После завершения работы слой меди нужно выровнять дополнительной очисткой, удалив остатки медного купороса и протерев поверхность спиртом.
Гальванопластика в домашних условиях
Гальванопластикой называют процесс электрохимического воздействия на изделие с целью придания ему необходимой формы осаждаемым на поверхности металлом.
Обычно эту технологию используют для покрытия металлом неметаллических изделий. Широко применяют ее в ювелирной области и дизайне бытовых предметов.
Медные покрытия, как правило, не применяются в качестве самостоятельного покрытия ни для декоративных целей, ни для защиты стальных деталей от коррозии.
Это связано с тем, что медь в атмосферных условиях легко окисляется, покрываясь налетом окислов.
Однако благодаря хорошему сцеплению осажденной меди с различными металлами медное покрытие применяется в многослойных защитно-декоративных покрытиях в качестве промежуточного подслоя, а также для защиты стальных деталей от цементации.
В гальванопластике медные осадки применяются для изготовления металлических копий, барельефов, волноводов и матриц.
Электролиты меднения подразделяют на кислые и щелочные . Из кислых электролитов используют сернокислые и борфтористоводородные. Наибольшее применение нашли сернокислые электролиты, отличающиеся простотой состава, устойчивостью и высоким выходом по току (до 100%). Недостатком этих электролитов является невозможность непосредственного покрытия стальных и цинковых деталей вследствие контактного выделения меди, имеющей плохое сцепление с основным металлом.
Поэтому перед меднением стальных детален в кислых электролитах их предварительно меднят в цианистых электролитах или осаждают тонкий подслой никеля. К недостаткам сернокислых электролитов относятся также их незначительная рассеивающая способность и более грубая: структура осадков по сравнению с другими электролитами.
К щелочным электролитам меднения относятся цианистые, пирофосфатные и другие электролиты.
Цианистые медные электролиты обладают высокой рассеивающей способностью, мелкокристаллической структурой осадков, возможностью непосредственного меднения стольных деталей. К недостаткам относятся низкая плотность тока и неустойчивость состава вследствие карбонизации свободного цианида под действием двуокиси углерода воздуха. Кроме того, цианистые электролиты характеризуются пониженным выходом по току (не более 60-70%).
Кислые электролиты меднения
Медь сернокислая — 150-250 г/л
Никель хлористый — 50-70 г/л
Температура = 18-25°С
Плотность тока = 1-4 А/дм2
При перемешивании электролита сжатым воздухом можно довести катодную плотность тока до 6-8 А/дм2.
Для приготовления сернокислого электролита меднения растворяют медный купорос, фильтруют его в рабочую ванну и при непрерывном помешивании добавляют серную кислоту.
При нанесении медных покрытий из сернокислого электролита медные аноды растворяются в основном с образованием двухвалентных ионов, которые, разряжаясь на катоде, осаждаются в виде металлической меди.
Однако наряду с этими процессами происходят п другие, нарушающие нормальное течение электролиза. Возможно также анодное растворение с образованием одновалентных ионов, хотя и в меньшей степени.
В электролите, омывающем металлическую медь, идет также химический обратимый процесс: Cu + Cu2+ = 2Cu+.
Накопление в растворе ионов одновалентной меди в больших количествах приводит к сдвигу реакции влево, в результате чего выпадает металлическая губчатая медь.
В растворе, кроме того, происходит окисление сернокислой одновалентной меди за счет кислорода воздуха н серной кислоты, особенно при воздушном перемешивании: Cu2SO4 + ½O2 + h3SO4 = 2CuSO4 + h3O.
На катоде процесс заключается в разряде двухвалентных и одновалентных ионов меди, но в связи с тем, что концентрация ионов одновалентной меди приблизительно в 1000 раз меньше концентрации ионов двухвалентной меди, катодный процесс выглядит так: Cu2+ + 2е- = Cu. Выход по току составляет 100%.
Для получения плотного гладкого осадка в электролите необходимо присутствие серной кислоты.
Меднение гальваникой и гальванопластика в домашних условиях
Серная кислота выполняет ряд функций:
значительно повышает электропроводность электролита;
понижает активность ионов меди, что способствует образованию мелкозернистых осадков;
предотвращает гидролиз сернокислой закисной меди, который сопровождается образованием рыхлого осадка закиси меди.
Дефекты при эксплуатации сернокислого электролита меднения и способы их устранения
Причина дефекта | Способ устранения | |
Грубая крупнокристаллическая структура осадков | Недостаток кислоты | Добавить кислоту |
Высокая плотность тока | Снизить плотность тока | |
Шероховатые осадки | Загрязнение электролита механическими примесями | Отфильтровать электролит |
Черные и коричневые полосы на покрытии | Присутствие в электролите примесей тяжелых металлов, мышьяка, сурьмы | Проработать электролит, при большом содержании примесей электролит заменить |
Пористые, рыхлые осадки | Наличие в электролите солей железа | |
Светлые блестящие полосы на покрытии, осадки хрупкие | Присутствие в электролите органических примесей | Отфильтровать электролит, проработать его током |
Борфтористоводородный электролит обладает несколько более высокой рассеивающей способностью, чем сернокислый.
Кроме того, в борфтористоводородных электролитах можно применять высокие плотности тока. Состав электролита (г/л) и режим меднения:
Медь борфтористоводородная – 35-40 г/л
Кислота борная – 15-20 г/л
Кислота борфтористоводородная – 15-20 г/л
Никель хлористый – 50-70 г/л
Температура = 18-25°С
Плотность тока = до 10 А/дм2
Электролит перемешивают сжатым воздухом или механической мешалкой.
Для приготовления борфтористоводородного электролита в борфтористоводородную кислоту небольшими порциями вводят свежеосажденную углекислую медь.
Раствор углекислой меди готовят подливанием подогретого концентрированного раствора соды к раствору сернокислой меди при перемешивании. Полученный осадок декантируют, промывают и растворяют в борфтористоводородной кислоте. В приготовленный раствор добавляют свободную борфтористоводородную и борную кислоту до требуемого значения рН (1-1,5). В ванну с полученным электролитом доливают воду до рабочего уровня.
(Деканта́ция, деканти́рование — в химической лабораторной практике и химической технологии механическое отделение твёрдой фазы дисперсной системы (суспензии) от жидкой путём сливания раствора с осадка.)
Электрохимический процесс — электро-тип, то есть. осаждение более толстого массивного слоя металла на поверхность объекта, форма которого должна быть распространена, скопирована, достаточно распределена. Например, гальванопластика используется в тех случаях, когда металлическая деталь имеет очень сложную форму и ее трудно или невозможно изготовить обычными способами (литье или механическая обработка).
Таким образом, скульптуры иногда воспроизводятся по образцам (автомобиль «Аполлон» на пьедестале Большого театра выполнен гальванопластикой).
Этот процесс относительно прост и может быть легко воспроизведен в домашних условиях.
Печать копируется из статьи или статьи для копирования, то есть из легкого металла, воска, пластика или гипса. Субъект, который нужно скопировать, вымыть с мылом, добавляется к картонной коробке и выливается низкоплавким сплавом из древесины или других сплавов.
После литья объект удаляют и полученную форму обезжиривают и ударяют путем литья в электролитической ванне.
Чтобы не откладывать металл по бокам формы, где нет никакого впечатления, они покрываются щеткой с расплавленным воском или парафином. После литья меди низкоплавкий металл растворяется в кипящей воде и получается матрица. Матрица заливается штукатуркой или свинцом, и копия готова. Следующая композиция для воска используется для изготовления пресс-форм:
Воск …………… 20 веков.
Гальванический. Бейкер, покрывающий алюминий.
час
Парафин ……… 3 v. час
Графит ……….. 1 v. час
Если форма изготовлена из диэлектрика (воск, пластик, парафин, гипс), его поверхность
покрытый электропроводящим слоем.
Передаточный слой может быть осажден с извлечением определенных металлов (серебра, меди, никеля) или механическими средствами — путем протирания поверхности графитом в виде листьев из щетки мягких волос.
Графит тщательно измельчают в фарфоровом растворе, просеивают через сито или марлю и наносят на поверхность продукта мягкой кистью или ватой. Графит лучше держит глину. Формы гипса, дерева, стекла, пластика и папье-маше покрыты раствором воска в бензине. На поверхности, которая не успевает высохнуть, поместите графит в порошок и излишек, без контроля графита.
Гальваническое покрытие просто отделено от графитовой формы. Если форма выполнена из металла, необходимо создать проводящую фольгу из оксида, сульфида или другой нерастворимой соли, такую как серебро — серебросодержащий хлорид свинца — сульфид свинца, чтобы обеспечить хорошее отделение от покрытия.
Медь, серебро и свинцовые поверхности обрабатываются 1% раствором сульфида натрия, что приводит к образованию нерастворимых сульфидов.
Отложение металла на поверхности пресс-формы. Готовая форма погружается в гальваническую ванну, схема которой находится под напряжением, так что снимаемая пленка не растворяется. Во-первых, «уплотнение» (покрытие) проводящего слоя меди осуществляется при низкой плотности тока в растворе этого
состав:
Серокислотная медь (сульфат меди) … 150-200 г.
Серная кислота 7-15 г
Этиловый спирт 30-50 мл
Вода …………………………………………. 1000 мл
Рабочая температура электролита составляет 18-25 ° С, плотность тока составляет 1 — 2 А / дм2.
Алкоголь необходим для
увеличить смачиваемость поверхности. Когда вся поверхность «подталкивается» медным слоем, форма переносится на электролит, предназначенный для гальванопластики. При гальванизации (медь) рекомендуется следующая композиция:
Серийно кислотная медь (сульфат меди) …..
340 c. час
Серная кислота 2 v. час
Вода …………………………………………. .1000 v. час
Температура электролита составляет 25-28 ° С. Плотность тока составляет 5-8 А / дм2.
Используя метод электроформовки, вы можете взять металлическое кружево для декоративно-художественного декоративно-художественного оформления различных предметов. Кружево растягивается на раме и пропитано парафином.
Затем вы протираете их между бумажными листами, чтобы удалить лишний парафин. Затем наносят электропроводящий слой тонкого графита, а избыток тщательно подталкивают кружевом. Путь провода — край кружева, он прикреплен к пластиковой раме или раме толстой проволоки с изолированным винилхлоридом вместе с кружевом, погруженным в электролит.
Лак, покрытый медью, обрабатывается латунной щеткой. Припаяйте их свинцовым припоем.
Гальваноспециальная обработка металлических кружев — использование декоративного слоя из серебра или золота или окисления.
Технологии -> пекарь
пекарь
Покрытие баком
Медные покрытия обычно не используются как самостоятельное покрытие для декоративных целей, а также для защиты стальных деталей от коррозии. Это связано с тем, что медь в атмосферных условиях легко окисляется, покрывается окислением.
Однако из-за хорошей адгезии осажденной меди к различным металлам медное покрытие используется в многослойных защитных и декоративных покрытиях в качестве промежуточных подошв, а также для защиты стальных деталей от газификации.
Для электроформования медные нанотрубки используются для изготовления металлических копий, рельефов основания, волноводов и матриц.
Медные электролиты делятся на кислотные и щелочные.
Кислотные электролиты используются сульфатными и борфтористоводородными. Наибольшее применение было доступно для сульфатных электролитов, характеризующихся их простым составом, стабильностью и высокой силой тока (до 100%).
Недостатком этих электролитов является невозможность непосредственного применения стальных и цинковых деталей для отделения медных контактов, которые плохо склеиваются с основным металлом.
Поэтому перед нанесением меди на стальные детали в кислотных электролитах они предварительно сохраняются в цианидных электролитах или наносимых тонких никелевых пластин. Недостатки сульфатных электролитов также являются их незначительной рассеивающей способностью и более грубыми: структура осаждения по сравнению с другими электролитами.
Электролиты щелочной меди покрывают цианидом, пирофосфатом и другими электролитами.
Цианид-медные электролиты обладают высокой дисперсионной способностью, мелкокристаллической структурой осаждения, возможностью непосредственных медных табличных объектов. К недостаткам относятся низкая плотность тока и нестабильность состава за счет карбонизации свободного цианида под воздействием углекислого газа в воздухе.
Быстрое накопление меди.
Кроме того, цианидные электролиты характеризуются сниженной мощностью тока (не более 60-70%).
Будьте осторожны! Компания «LV-Engineering» не предоставляет услуги по гальванизации! Наша организация осуществляет проектирование гальванических изделий, производство гальванических ванных комнат и полипропиленовых линий, монтажные и пуско-наладочные работы в данном направлении.
Кислотные электролиты
Сульфат меди — 150-250 г / л
Никель-хлорид — 50-70 г / л
Температура = 18-25 ° C
Плотность тока составляет 1-4 А / дм2
Когда электролит смешивается со сжатым воздухом, плотность катодного потока может быть подключена к 6-8 А / дм2.
Для приготовления медносульфатного электролита растворите сульфат меди, процедите в рабочую пантеру и добавьте серную кислоту при непрерывном перемешивании.
Когда медные покрытия наносят из сульфатного электролита, аноды меди сначала растворяются с образованием двухвалентных ионов, которые осаждаются в виде металлической меди при выгрузке на катод.
Однако наряду с этими процессами существуют и другие, которые препятствуют нормальному течению электролиза. Анодное растворение возможно также при образовании одновалентных ионов, хотя и в меньшей степени.
В электролите, который удаляет медный металл, существует также химически обратимый процесс: Cu + Cu2 + = 2Cu +.
Накопление ионов иона иона в растворе в больших количествах приводит к тому, что реакция перемещается влево, а это означает, что к нему принадлежит медная медь.
Раствор также окисляет сульфаты меди из-за атмосферной серной кислоты N, особенно воздуха во время смешивания: Cu2SO4 + 1 / 2O2 + h3SO4 = 2CuSO4 + h3O.
На катоде в процессе отходящий двухвалентных и одновалентных ионов меди, но из-за того, что концентрация ионов одновалентной меди около 1000 раз ниже, чем концентрация ионов двухвалентной меди, катодная методом электроосаждения выглядит следующим образом: Cu 2+ + 2e = Cu. Токовый выход составляет 100%.
Присутствие сорбиновой кислоты требуется для получения плотного гладкого осадка в электролите.
Серная кислота выполняет множество функций: она значительно увеличивает электропроводность электролита; он уменьшает активность ионов меди, что способствует образованию мелких зерен; предотвращает гидролиз сульфата железа, что сопровождается образованием свободного осадка из оксида меди.
Ошибки электролита медно-сульфатного электролита и методы их устранения
| ошибка | Причина ошибки | средство |
| Грубая структура грубых осадков | Кислотный дефицит | Добавить кислоты |
| Высокая плотность тока | Уменьшить плотность тока | |
| Грубые сквозняки | Загрязнение электролита механическими примесями | Фильтровать электролит |
| Черные и коричневые линии на обложке | Наличие в электролитных примесях тяжелых металлов, мышьяка, сурьмы | Проверьте электролит с высоким содержанием примесей, замените электролит |
| Пористые, рыхлые отложения | Присутствие солей железа в электролите | |
| На крышке есть яркие блестящие линии, которые являются хрупкими | Присутствие органических примесей в электролите | Фильтруйте электролит и заряжайте его электричеством |
Борфторогидроэфир имеет немного большую мощность распыления, чем серная кислота.
Кроме того, флюсы высокой плотности могут использоваться в борфтористоводных электролитах. Состав электролита (г / л) и способ применения меди:
Гидрохлорид борфторида меди — 35-40 г / л
Борная кислота — 15-20 г / л
Соляная кислота — 15-20 г / л
Никель-хлорид — 50-70 г / л
Температура = 18-25 ° C
Плотность тока = до 10 А / дм2
Электролит смешивают со сжатым воздухом или механической мешалкой.
Свежую измельченную углеродную медь вводили небольшими порциями для приготовления скважинного углеводородного электролита в борфтористовородной кислоте.
Раствор углеродной меди готовят путем нагревания нагретого концентрированного раствора сульфата натрия в раствор сульфата меди путем смешивания. Полученный осадок декантируют, промывают и растворяют в борфтористой кислоте. К желаемому раствору добавляют свободную бороновую кислоту и борную кислоту до желаемого значения рН (1-1,5). Добавить воду на рабочую поверхность в ванне с электролитом.
Если перед вами стоит задача омеднения каких-либо деталей в автомобиле, то оказывается это вполне возможно сделать в домашних условиях. Для этого не потребуется особых знаний и умений, да и все материалы и реагенты вполне можно найти в магазинах или своих запасах. Что же, давайте посмотрим как можно сделать омеднение.
Когда делают омеднение и можно ли его использовать для коррозионного покрытия
Прежде чем рассказать о самом процессе, хотелось бы сказать пару слов о прагматичности такой операции.
Многие из автолюбителей не особо знакомых с химией сейчас скажут о необходимости омеднения всего чего попадется под руку, но мы вас предостерегаем от этого! Почему!? Да потому что все металлы между собой образуют гальваническую пару. Такая гальваническая пара образуется даже при попадании воды, а если средой будет еще и кислота, то процесс пойдет в разы быстрее.
Суть процесса в гальванической паре сводится к следующему. Более активный металл отдает свои электроны, а менее активный принимает. Вот так и образуется самая простая «батарейка» в которой протекает электрический ток.
Давайте теперь взглянем на стандартные электродные потенциалы:
— для меди Е0(Сu2+/Cu)=0,34В;
— для железа E0(Fe2+/Fe)=-0,44В.
В итоге получается не все так гладко.
Ведь в такой гальванической паре У железа электродный потенциал более активным. Опять же у меди электродный потенциал более положителен, чем у железа, поэтому она будет менее активна.
В итоге электроны потекут от железа к меди, что приведет к коррозии железа.
Все это мы рассказали к тому, что бездумно покрывать медью все что вам попадется под руку на машине не рекомендуется. Ведь в этом случае вы можете значительно сократить жизненный цикл многих железных деталей (крепеж, кузовные детали).
Гальваническое меднение
Не зря для сохранения железа применяют цинк, там ситуация с электродными потенциалами обратная.
Однако омеднение может применяться для декоративной отделки железа, если покрытие будет находиться в сухости.
Также медь может применяться в случаях, где необходимо обеспечить передачу электрического тока между контактами. Опять же надо следить за их чистотой.
Медь может применяться в условиях применения пар с незначительным трением скольжения. Все это в целом вполне жизнеспособные варианты. А значит и омеднение все же имеет шанс на его реализацию.
Тогда не будем более медлить, расскажем непосредственно о процессе омеднения.
Процесс омеднение деталей в домашних условиях (расчет слоя покрытия при определенном токе)
Омеднение происходит в растворе. По сути этот процесс обратный гальванической паре, то есть тому, о чем мы рассказывали в абзаце выше.
Для раствора нам понадобиться кислота, можно взять электролит используемых для аккумуляторов. Воду и медный купорос.
Для раствора берется 100 мл электролита на 20 мл воды и добавляется 20 г медного купороса.
В качестве донора меди можно взять медные пластинки или обычный медный провод, предварительно очищенный от изоляции. Итак, именно в этот самый раствор и помещаем медь. При этом подключаем блок питания постоянного напряжения питания к меди (+) и к железу (-). Ток на блоке питания выставляем тот, при котором мы планируем за определенный период времени нанести определенный слой меди.(-7)
* желаемое время, скажем 3 часа – 10800 секунд). Считаем…
I=8920*0,1*0,0001/0,0000066*10800=0,0892/0,07128=1,25 А
То есть за 3 часа при токе 1,25 А у нас будет покрытие в 0,1 мм на детали площадью 0,1 м3. Вот как-то так и считаем все аналогичные вариации.
А да, время от времени не забываем помешивать раствор, чтобы процесс шел равномерно.
После того как омеднение завершено, вытаскиваем детали из раствора и отмываем хорошо с щелочью, то есть с мылом.
Если есть каике-то заусенцы и отклонения от формы, то их вполне можно пройтись наждачной бумагой и заполировать.
Собственно вы теперь не меньше знаете, как производить омеднение поверхности.
Надо сказать, что по тому же принципу производится и оцинкование и хромирование… В итоге понимая принцип происходящего процесса можно перенести процесс покрытия поверхности и на другие металлы.
Состояние электрического тока растворов цианистого меди значительно отличается от тех, которые считаются наиболее благоприятными в кислотных растворах. Из-за того, что образуются сильные сложные ионы и очень низкая скорость диссоциации, активность ионов меди в цианидном растворе настолько мала, что потенциал около 1 В становится более отрицательным, чем раствор серной кислоты.
Увеличивая плотность тока, катодный потенциал меди в цианидных электролитах, в отличие от кислоты, сильно изменяется в направлении электроотрицательных значений (рис.
84), который определяет условия кристаллизации и распределения металла на поверхности катода; С этой точки зрения условия в цианидных электролитах чрезвычайно благоприятны.
Но именно из-за потенциала катода быстро растет с плотностью тока, это не может быть существенно увеличено, в противном случае выходной ток металла может быть сведен к нулю.
Рис. 84. Кривые поляризации медных электролитов:
1-сульфатного электролита 1,5-n. CuSO4 + 1,5-n.
h3S04; 2-цианидный электролит композиции 0,25-n.
CuCN + 0,6-n. NaCN + 0,25-n. Na2C03; 3 — тот же электролит при 45 ° C; 4 представляет собой тот же электролит в присутствии Na2S2O3
Еще одно важное различие в кислотности цианидных электролитов следует рассматривать как значительные изменения в характеристиках меди в зависимости от концентрации свободного цианида, в то время как свободная серная кислота оказывает очень мало влияния на характеристики меди в кислотных электролитах.
Если в растворе, содержащем 9 г меди на литр в форме цианидной соли (0,1 м.
Гальванизация собственными руками дома: технологии и оборудование
CuCN) и 13 г / л KCN, медный потенциал -0,60 В, в присутствии 26 г / л KCN этот потенциал равен -0,964 В и в присутствии 65 г / л -1,169 В.
Катодная поляризация также сильно зависит от концентрации солей меди в электролите, в то время как кислотные электролиты оказывают незначительное влияние.
Анодный процесс в цианидных электролитах также сопровождается значительной поляризацией, размер которой в основном определяется содержанием свободного цианида.
Отсутствие цианидного анода неактивно до полного растворения их растворения. Таким образом, содержание свободного цианида оказывает диаметрально противоположное воздействие на процессы катодного и анодного; Сначала требуется минимальное содержание свободного цианида (катодная плотность тока может быть выше, чем ниже цианид в электролите), второй — по величине (анод пассивации начать с самой высокой плотностью тока, тем выше содержание цианида).
Это значительно ограничивает выбор концентрации цианида, который является основным компонентом электролита из соли меди.
Для большинства цианидов электролиты не могут полностью использовать методы, которые позволяют им использовать увеличенную плотность тока, такую как смешивание или значительное повышение температуры, по той причине, что эти процессы ускорили гидролиз цианида. Даже в состоянии покоя при комнатной температуре цианид электролита разрушается быстрее, чем кислота, что приводит к абсорбции углекислого газа из воздуха.
Электролиты из цианид-меди, нанесенные на катод, извлечение из одновалентных ионов, т. Е. При 1 Ач теоретически получают в два раза больше меди, чем в кислотных электролитах, где медь присутствует в виде двухвалентных ионов.
Тот факт, что цианистые электролитный баланс потенциал медь сильно отрицательная с более высоким потенциалом плотности тока переместился от электрических величин служат в качестве основы для суждения невозможности осаждения меди из цианистых электролитов при высоких плотностях тока (по заказу 10 А / дм 2) с теоретическим или вблизи теоретического выхода поток.
На самом деле это справедливо только для разбавленных цианидных электролитов, не страдают от перемешивания и нагрева. При определенных условиях медь может выделяться на электролитах с цианидным катодом, особенно при низком содержании свободного цианида в электролите при высоких температурах и при смешивании при достаточно высокой плотности тока и эффективности тока, близкой к теоретической.
Хромирование в домашних условиях
Содержание:
1. Хромирование дома своими руками.
2. Проблемы гальваники хромом в домашних условиях.
1. Хромирование своими руками.
Многим гальваника кажется делом легким и дешевым. Сегодня очень часто можно встретить в сети сайты, рассказывающие о хромировании в домашних условиях. Бытует мнение: «макнул бампер в раствор — вот тебе и идеально блестящее, прочное покрытие». А так как не у многих найдется лишняя сотня квадратных метров бесхозной площади, то первым в очереди на заселение становится гараж. Оттого домашнюю гальванику называют еще «гаражной».
Найти профессиональную литературу по электрохимическим покрытиям в интернете — не проблема. Однако мало знать технологию. Тем более, многое, что написано в книгах зачастую вообще не работает в конкретных условиях. В данной статье приведены некоторые организационные проблемы, с которыми можно столкнуться при создании участка хромирования у себя дома.
2. Проблемы гальваники хромом в домашних условиях.
1. Кроме непосредственно ванны хромирования требуется еще большое число ванн для подготовительных операций. Качественное декоративное покрытие невозможно получить без полировки поверхности. Легко ли отполировать до блеска автомобильный диск? Даже для обработки того же бампера требуется умение. После мехобработки потребуется обезжиривание, затем травление (после всех операций придется делать минимум 3 промывных ванны), которое не всегда проводится в серной кислоте. Положим, что аккумуляторную кислоту достать можно. С соляной и азотной кислотой дело обстоит сложнее, как и со всеми последующими реактивами по той простой причине, что легально реактивы могут продаваться ТОЛЬКО ЮРИДИЧЕСКИМ ЛИЦАМ или на худой конец ИП. И уж точно никто в здравом уме не продаст левому человеку хромовый ангидрид, являющийся основным компонентом ванны хромирования. А серная кислота в этой ванне потребуется уже не аккумуляторная, техническая, а чистая, определенной квалификации. Даже приготовление электролита — сложная задача, которая включает в себя проработку током в нужном режиме
2. Электролит хромирования требует определенной температуры, соотношения ангидрид/кислота и плотности тока. Для такой ванны необходим высоковольтный, по сравнению с обычной гальваникой, выпрямитель тока большой мощности. Посчитайте площадь поверхности покрываемого диска (всю, так как нормально заизолировать ненужные части не удастся — выделяющийся на катоде водород сорвет любой лак или пленку) — плотность тока для хромирования может достигать 30 А/дм2. Теперь умножьте площадь в дм2 на эту величину. Это потребный для покрытия ток. Если умножить этот ток на напряжение для хромирования, то Вы получите мощность выпрямителя и она окажется немаленькой. Скорее всего, выпрямитель будет трехфазным, а такая сеть есть не во всех гаражах.
3. Теперь — ванны. На все операции может потребоваться до 12 ванн, если используется 1 ванна хромирования. В электролизной ванне придется ставить свинцовые аноды и медные штанги большого сечения. Эти вещи тоже нелегко достать, так как нужно их относительно немного, а продавать их поштучно почему-то не хотят. В основном — мелкий опт. В каждой ванне нужна будет дистиллированная вода. Если принять примерный объем одно ванны 250 л, то, умножив эту цифру на 12 ванн, получим 3 кубометра дистиллированной воды. Это 3000 л. Согласитесь, покупать 3000 бутылок дистиллята в автомагазине — не лучшая идея. Дистиллятор же потребует много денег и обязательно наличия холодного водоснабжения, которое есть не во всех гаражах.
4. Хромовый электролит не предусматривает использования расходуемых анодов. Это означает, что концентрации компонентов в нем постоянно меняются. Добавим сюда низкий выход по току и получим, что корректировка электролита потребует целой аналитической лаборатории. А там — приборы и специфические реактивы. И навыки. Без опытного технолога будет очень непросто обойтись.
5. Отдельно поговорим про экологию. Помним, что хромовый ангидрид — сильнейший яд и канцероген. Промывную воду после хромирования придется менять часто. Куда девать весь этот объем стоков? Слив на улицу — последнее, что должно прийти в голову, за это можно загреметь по уголовному делу и сильно, не говоря про штрафы. Вывозить за город — не навывозишься. А если электролит выйдет из строя? За выброс такого количества канцерогенов в окружающую среду можно смело приписывать статью «терроризм». И это на самом деле так — это тяжелейшее преступление против тех, кому в питьевую воду потом попадет этот источник рака.
Из всего этого заключу, что организация гальваники в домашних условиях — дело не только сложное, рискованное, малорентабельное, но и НЕЛЕГАЛЬНОЕ и УГОЛОВНО НАКАЗУЕМОЕ. Затрат придется внести куда больше, чем кажется, проблем — не оберешься. И если даже что-то получится, конкурировать с профессиональной гальваникой «гаражная» вряд ли сможет. Стоит ли браться? Решайте сами. В конце концов, если Вы решили зарабатывать, то можно найти много более выгодных способов вложения денег, а если вам нужен конкретный продукт — обратитесь к профессионалам. Только имейте в виду, что кроме гальванического хромирования есть еще другие виды: мета-хром, напыление, трибо-гальваника. Все они НЕ ДАЮТ КАЧЕСТВЕННО СЦЕПЛЕННОГО покрытия и ваш блестящий повод для гордости на копытах железного коня очень скоро может стать поводом для покупки колпаков, чтобы закрыть обсыпавшееся и прокорродировавшее непотребство. И это на стальном диске. А если диск алюминиевый или титановый? Такие материалы даже гальванически ЧРЕЗВЫЧАЙНО сложны для покрытия и требуют куда более сложной обработки. Из чего вытекает, что качественное хромирование будет по карману далеко не каждому.
Покрытие медью железа. Гальваника своими руками в домашних условиях: технология и оборудование
В современном мире больше распространение получил медный сплав. Он наносится на поверхность для придания внешней привлекательности различных изделий. Меднение в домашних условиях зачастую проводится для существенного повышения показателя электропроводности. В некоторых случаях рассматриваемый процесс является промежуточной операцией, которая позволяет нанести другое вещество на поверхность.
Использование меднения
Покрытие медью различных заготовок в последнее время часто проводится в домашних условиях. В большинстве случаев технология применяется для достижения следующих целей:
- Декорирование металла или пластика. Меднение металла в домашних условиях часто проводится для того, чтобы получить старинные на вид изделия, которые пользуются большой популярностью. Специальная процедура состаривания позволяет создать эффект длительного использования изделия. Кроме этого, медь после нанесения напоминает золото. Именно поэтому небольшой слой можно нанести для получения статуэтки или сувенира.
- Гальванопластика. Меднение стали подобным образом также может проводиться в домашних условиях. Суть технологии заключается в создании восковой или пластиковой основы, которая покрывается слоем рассматриваемого сплава. Гальванопластика часто применяется для получения ювелирных изделий или сувениров, матриц и волноводов. Применение специальных материалов позволяет существенно повысить качество покрытия.
- Получение деталей, используемых при создании различных механизмов. Меднение чугуна или другого металла проводят на производственных площадках при различных технологий. Покрытие заготовки медью позволяет существенно повысить электротехнические качества. Подобным образом можно получить клеммы или прочие подобные элементы, которые будут эксплуатироваться под напряжением. Изделия из чистой меди обходятся очень дорого. Именно поэтому часто применяется рассматриваемая технология.
Меднение пластика в домашних условиях проводится крайне редко, так как подобный материал не выдерживает воздействие высокой температуры. Кроме этого, пластичность основания приводит к появлению структурных трещин.
Особенности меднения в домашних условиях
Меднение металла – особая технология нанесения слоя меди толщиной 1-300 мкм и больше. Особенности применяемых технологий определяют то, что медное покрытие будет прочно держаться на поверхности металла. Среди особенностей, которые приобретает заготовка, отметим следующие моменты:
- Пластичность.
- Высокая электропроводность. Медные изделия хорошо известны с тем, что могут проводить электричество и при этом не нагреваются. Именно поэтому часто создаются изделия, которые покрываются подобным сплавом.
- Более привлекательный вид. Медь блестит на солнце, на поверхности появляются блики.
- В атмосферных условиях сплав легко окисляется и покрывается налетом. Этот момент стоит учитывать при рассмотрении того, где и как именно будет использоваться изделие.
- Медная пленка со временем покрывается пятнами и радужными разводами.
Обмеднение в домашних условиях может проводиться при применении специального раствора. Стоит учитывать, что процесс предусматривает использование специальных реагентов. Поэтому нужно предусмотреть наличие эффективной приточной вентиляции, а также индивидуальных средств защиты. Меденение пластика несколько отличается, предусматривает применение особой технологии.
Разновидности меднения
Рассматриваемая процедура доступна для выполнения даже новичкам в сфере металлургии. Для получения качественной поверхности нужно знать все особенности процесса. Меднение свинца и других металлов в домашних условиях может проводиться при применении двух различных технологий:
- С погружением в электролит. Подобная технология предусматривает окунание заготовки в подготовленный раствор, после чего подводится напряжение. Зачастую применяется в том случае, если размеры заготовки небольшие, так как требуется меньшее количество специального электролита. Для погружения заготовки требуется ванная или другая емкость, которая не реагирует на воздействие применяемого раствора.
- Без погружения в заранее подготовленную емкость. Она сложна в исполнении, но также позволяет достигнуть высокое качество медной поверхностной пленки.
В обоих случаях предусматривается подвод электричества, за счет чего вещество активизируется.
Наиболее подходящий способ обработки выбирается в зависимости от того, какой нужно достигнуть результат. Примером назовем:
- Получение защитно-декоративного слоя. В этом случае часто проводится смешивание хрома с никелем и медью. За счет подобного сочетания сплавов можно получить надежную поверхность.
- Для защиты поверхности на момент цементирования. Нанесение тонкого слоя меди позволяет защитить заготовку от цементирования. Покрывается раствором поверхность, которая в дальнейшем будет обрабатываться резанием.
- Восстановление и ремонт деталей. При восстановлении хромированных деталей автомобиля и мотоциклов может применяться рассматриваемая технология. При нанесении слоя не более 250 мкм можно скрыть поверхностные дефекты металла.
Обе технологии обработки характеризуются своими определенными особенностями, которые нужно учитывать.
Меднение в растворе с электролитом
Гальваническое покрытие медью в домашних условиях с погружением проводится крайне часто. Подобная технология позволяет получить равномерное покрытие. К особенностям подобного способа обработки можно отнести следующие моменты:
- Для удаления оксидной пленки перед меденением заготовка обрабатывается наждачной бумагой. После этого изделие промывается и обезжиривается горячей смесью из соды. Если не уделить внимание подготовительному этапу, то проводимый процесс не позволит получить устойчивое к механическому воздействие изделие. Металл, который подвержен воздействию коррозии, должен быть хорошо очищен, так как даже мелкая крошка может сделать поверхность неоднородной.
- В банку или другую емкость на медных проволоках опускается две пластины из этого же сплава. Они выступают в качестве анода. Применяемая тара должна быть из стекла.
- Между двумя анодами подвешивается обрабатываемая деталь, которая подключается к минусу, а пластины к плюсу. В качестве источника питания может использоваться батарея, выдающее напряжение 6В.
- Гальваническое меднение предусматривает применение определенного раствора. Он является связующим элементом между деталью и анодами. Раствор для гальванического меднения можно создать изготовить, для чего берется 20 грамм медного купороса и 3 миллилитра серной кислоты. Для разбавления и смешивания этих ингредиентов можно использовать 100 миллилитров дистиллированной воды. При работе с полученным раствором нужно быть крайне внимательным, так как при попадании вещества на открытые участки кожи могут возникнуть ожоги.
- Меднение алюминия медным купоросом в домашних условиях может проводиться только в том случае, если электроды были полностью покрыты раствором. Если они будут находиться в сухом состоянии, то они могут нагреться и расплавиться. При длительной обработке вещество может нагреться и его объем уменьшится.
При применении рассматриваемой технологии сила тока устанавливается на уровне 15 мА на каждый квадратный сантиметр. На покрытие всей поверхности специальным сплавом, как правило, уходит не менее 20 минут. При увеличении протяженности срока покрытие становится толще.
Меднение без опускания в раствор
Подобный метод применяется для покрытия стали, цинка или алюминия. Покрытие изделия медью в домашних условиях в этом случае проводится проводом, с которого предварительно снимается изоляция для получения своеобразной кисти. Обратный конец провода подключают к плюсу источнику энергии. Химическое меднение в домашних условиях также предусматривает использование специального раствора, который повышает эффективность процесса.
Среди особенностей создания требующего раствора можно отметить следующие моменты:
- Используется раствор медного купороса. Его можно приобрести в специализированных магазинах. Кроме этого, специальный электролит изготавливается при смешивании различных химических элементов.
- Состав немного подкисляют. За счет этого существенно повышается эффективность проводимой процедуры.
Вещество наносится на поверхность, после чего подготавливается металлическая поверхность. Она очищается от загрязняющих веществ, после чего обезжиривается. После этого подготовленная заранее пластина укладывается в ванночку и к ней подводится минус от источника тока.
Подобный процесс предусматривает, чтобы между собранными проводками и пластиной постоянно был слой электролита. За счет этого обеспечивается высокая степень проводимости. Для того чтобы покрыть изделие небольших размеров требуется сего несколько секунд.
После нанесения покрытия изделие сушится на воздухе. Нельзя допускать попадания различных загрязняющих веществ. Следующий шаг заключается в натирании медной прослойки шерстяной тряпкой или другим сукном. В большинстве случаев рассматриваемая технология применяется в том случае, когда изделие имеет большие размеры и не может погружаться в ванную.
Необходимое оборудование
Медное покрытие может наноситься в домашних условиях при применении даже самого обычного оборудования. Установка ванной для проведения рассматриваемой процедуры проводится примерно также, как и гальванических. Стоит учитывать, что существует два типа активных растворов: кислые и щелочные.
При работе может применяться:
- Небольшие медные пластины в качестве электродов.
- Проволока для подачи тока.
- Источник тока, к примеру, АКБ, который рассчитан на подачу тока напряжением 6 В.
- Для регулировки силы тока может устанавливаться реостат.
Меднение алюминия и других сплавов в домашних условиях не требует большого количества времени. Для очистки получаемой поверхности могут применяться различные ткани.
Медные покрытия не рекомендуются для защиты железа и стали от коррозии. Омедненные изделия могут быть защищены от атмосферной коррозии лишь! в том случае, когда медные покрытия совершенно свободны от пор даже микроскопических размеров. При наличии пор изделия не только не будут защищены от коррозии, но, напротив, в присутствии корродирующего агента, между железом и медью начнет работать коротко замкнутый гальванический элемент, в котором железо будет играть роль анода и его коррозия будет протекать более интенсивно, чем неомедненного железа.
Медные покрытия не могут также рассматриваться как защитно-декоративные. Хотя химическая стойкость меди больше, чем железа, но в наружной атмосфере с небольшой относительной влажностью медные покрытия тускнеют в результате окисления, которое протекает по параболическому закону. При повышенной влажности в порах медных покрытий происходит ржавление стали (анода). На беспористых медных покрытиях в наружной атмосфере с повышенной влажностью постепенно образуется зеленая патина, которая, по некоторым данным, представляет собой основной сульфат меди CuSO 4 3Cu(OH) 2 ; на морском побережье может образоваться основной хлорид меди. Устойчивость патины в различной атмосфере, по-видимому, объясняется образованием закиси меди. При анодном окислении в соответствующих электролитах можно искусственно получать патину.
Довольно широко распространен процесс меднения участков стальных деталей, подлежащих обработке резанием после термической обработки — цементации. Стальные детали иногда подвергают меднению с последующим химическим или электрохимическим окрашиванием в различные цвета. Однако наиболее широко медные покрытия используют в качестве промежуточных слоев при защитно-декоративном хромировании стальных и цинковых деталей. Широкое применение электролитических осадков меди в качестве промежуточных слоев при нанесении различных гальванических покрытий в известной мере определяется хорошим сцеплением электроосажденной меди с различными металлами. В отличие от горячих методов нанесения металлических покрытий, при которых между основным металлом и покрытием образуется промежуточный диффузионный слой, при электролитическом осаждении меди на сталь не удается обнаружить промежуточный диффузионный слой. Решающую роль для обеспечения прочного сцепления в данном случае играет тщательная подготовка поверхности основного металла — обезжиривание и травление, причем в случае химического или электрохимического удаления деформированного слоя часто наблюдается продолжение структуры основного металла в электроосажденном металле. Прочность сцепления между основным металлом и покрытием при этом приближается по величине к прочности связи между отдельными атомами в твердом металле.
Продолжение микроструктуры основного металла в электролитическом осадке, по-видимому, обеспечивается в тех случаях, когда основной металл имеет относительно крупнокристаллическую структуру и электролиз протекает при условиях, соответствующих образованию кристаллов примерно таких же размеров. При включении посторонних ионов, атомов или молекул осадки получаются мелкокристаллическими и продолжения структуры основного металла не наблюдается (рис. 82).
Рис. 82. Продолжение структуры основного металла электроосажденной меди (снизу вверх): серебра (а), никеля (б) (нет продолжения), в — катаной меди
При защитно-декоративном хромировании стальных и цинковых деталей роль медного слоя сводится к максимальной экономии стратегического никеля при сохранении защитных свойств суммарных покрытий (Cu+Ni+Cr) и снижению трудоемкости операций механической подготовки поверхности стальных деталей.
Как известно, медь значительно пластичнее стали и в процессе ее полировки удается получать гладкую, блестящую поверхность, на которую легко наносить блестящие никелевые покрытия. Здесь необходимо оговорить, что в последнее время достигнуты большие успехи в получении блестящих покрытий, не требующих полировки, но эта задача решена еще не полностью. При нанесении относительно тонких слоев из цианистых или пирофосфатных электролитов на стальные или цинковые детали удается получать блестящие или полублестящие медные покрытия, поверх которых после промывки можно наносить блестящие никелевые покрытия.
Меднением называется процесс гальванического нанесения меди на различные поверхности. Слой меди обладает сильной адгезией к металлам, сглаживает дефекты покрываемой поверхности, имеет высокую электропроводность и пригоден для дальнейшей обработки. Меднение может использоваться как самостоятельный процесс, так и как часть более сложных (серебрение, никелирование, хромирование). Наряду с промышленным способом практикуется меднение в домашних условиях, позволяющее решить множество бытовых задач. Кроме высоких технических характеристик, данное покрытие прекрасно выглядит, что определяет его использование в различных дизайнерских решениях.
Технология меднения
В промышленных условиях меднение происходит в мощных гальванических ваннах, укомплектованных средствами автоматики и другим специальным оборудованием. Однако, этот процесс доступен для выполнения и дома, позволяя обойтись без сложной химической аппаратуры.
Последовательность технологических операций следующая:
1. С металлической поверхности удаляется оксидная пленка. Используется наждачная бумага, щетка, полировочные пасты;
2. Покрываемый предмет обезжиривается раствором соды и тщательно промывается водой;
3. В стеклянную емкость на медной проволоке погружаются две медные пластины (аноды), между ними подвешивается деталь;
4. Аноды подключаются к «плюсу» источника постоянного тока, а омедняемая деталь к «минусу»;
5. В электрическую цепь последовательно включается реостат, регулирующий силу тока, и амперметр. В качестве источника постоянного тока можно применить автомобильный аккумулятор или блок питания;
6. Электролит наливается в емкость таким образом, чтобы он полностью покрывал поверхность анодов. Выполнять эту операцию следует особенно аккуратно, не допуская попадания едкой жидкости на открытые участки тела!
7. Плотность тока устанавливается на уровне 2А на дм2 обрабатываемой поверхности, температура электролита: 20–26 градусов, продолжительность обработки: 20-25 минут;
8. Омедненная деталь извлекается из емкости, процесс закончен. Толщина медного слоя может быть увеличена за счет большего времени пребывания детали в гальванической ванне.
Состав электролита не сложен: кислота серная – 40 г, сернокислая медь – 190 г, вода – 980 г.
Несколько советов по меднению:
- сернокислую медь можно приобрести в магазинах для садоводов и огородников, а серную кислоту и дистиллированную воду — в автомагазинах;
- в качестве гальванической ванны необходимо использовать емкость из материала, устойчивого к действию агрессивных сред. Можно взять стеклянную банку или небольшую пластмассовую канистру;
- чтобы слой наносимой меди не получился рыхлым, следует максимально тщательно отполировать подготавливаемую поверхность. Кроме того, рабочий ток должен быть не слишком большим. Потеря времени будет компенсирована качеством получившегося изделия.
Примеры меднения своими руками
Иногда требуется заменить вышедшую из строя медную мебельную фурнитуру, а в продаже имеются только никелированные изделия. В этом случае можно легко собрать установку для нанесения меди. Необходимые приборы и материалы: блок питания 12 В / 3 А, серная кислота и медный купорос.
Сначала необходимо удалить никелировку. Для этого деталь удерживается пинцетом, на который подается «минус» от блока питания. Тряпочкой, закрепленной на
плюсовом электроде, смоченной в 5% серной кислоте, протирается поверхность изделия.
При снятии никелировки образуются ядовитые пары, от которых необходимо защищать органы дыхания. Желательно использовать специальные очки и респиратор с угольным фильтром. Очищенная поверхность полируется.
Следующий шаг – сборка простейшей гальванической установки. В банку помещается медный электрод, соединяемый с «плюсом» БП, и обрабатываемая деталь, подключаемая к «минусу».
Заливается электролит, состоящий из медного купороса, воды и 5% серной кислоты в пропорции 1/5/3 и подается ток. Готовые изделия полируются до приятного блеска.
Для домашнего меднения существует множество различных применений. Наносить медь можно на алюминиевые столовые приборы, давая им вторую жизнь, на рыболовные блесны, подсвечники и многое другое. Особенно впечатляют работы, в которых декоративное покрытие нанесено на неметаллические предметы: стебли растений, листья, желуди и даже на высушенных насекомых. Природная фактура исходного материала, сочетаясь с красотой гальванического покрытия, создает неповторимый художественный эффект.
Технология изготовления подобных изделий несколько сложнее, но вполне осуществима дома. В покрываемом материале отсутствует токопроводящий слой, поэтому вместо него используется специальный электропроводный лак, наносимый на поверхность. Рецептура лака включает в себя органические растворители, пленкообразователи и тонкодисперсный графитовый порошок, обеспечивающий электропроводность.
Лак наносится тонким слоем на сухое растение, высыхает, и через час все готово для меднения. После гальванической обработки можно дополнительно улучшить внешний вид изделия. Существует несколько способов придания гальванической меди различных цветовых оттенков, в том числе с помощью патинирования, химического окрашивания и оксидирования.
Качество художественных работ, полученных по этим технологиям, находится на уровне настоящих ювелирных украшений.
Уважаемые читатели, комментируйте статью, задавайте вопросы, подписывайтесь на новые публикации — нам интересно ваше мнение:)
Для того чтобы подготовить металлический предмет к дальнейшей обработке, его нужно покрыть медью — такой процесс называют гальваностегией. Принцип его действия заключается в осаждении на поверхность обрабатываемой детали из другого металла, который растворен подходящим средством. Из данной статьи вы узнаете, как покрыть медью металл в домашних условиях, чтобы реализовать все последующие свои задумки с заготовкой.
Для чего это нужно?
Технология гальваностегии включает в себя создание раствора и образование различных электродов. Во время этого процесса медные ионы, которые растворены в электролите, притягиваются минусовым полюсом обрабатываемой детали на свою поверхностную точку.
Гальваностегия металлических деталей в промышленности применяется не только как завершающий обрабатывающий процесс. Она может применяться для того, чтобы подготовить детали к последующей операции (к примеру, хромированию, никелированию, серебрению каких-либо предметов).
В домашних условиях чаще всего проводится химическое меднение деталей. Также стоит заметить, что есть множество способов проведения такой процедуры, каждый из которых имеет свои преимущества и недостатки.
Сферы использования гальваностегии
Покрывать медью металл в домашних условиях в последнее время стало очень полезно. Чаще всего к такой процедуре подходят в следующих целях:
- В декоративных. Например, таким способом состаривают различные детали для того, чтобы придать винтажный вид.
- В гальванопластике. Очень часто наносят медный слой на сувениры, ювелирные украшения.
- В отрасли техники. Это связано с низкой стоимостью омеднения.
- Для нанесения защитно-декоративной прослойки того или иного изделия.
- Для того чтобы реставрировать или восстанавливать какие-либо детали.
Гальваностегия электролитным раствором
Таким способом можно покрыть медью сталь в домашних условиях, а также другие детали за исключением алюминия и цинка.
Для дальнейшей процедуры необходимо подготовить следующие материалы:
- Небольшие пластины из меди.
- Токопроводящая проволока (лучше запастись несколькими метрами).
- Источник тока, напряжение которого не должно быть более, чем 6 В.
- Реостат, чтобы регулировать ток.
- Амперметр.
- Электролит.
Важно! Последний компонент можно приобрести в специальном магазине, а можно и изготовить самостоятельно. Для этого нужно сделать раствор серной кислоты и дистиллированной воды при соотношении 2/100 мл. Нужный раствор получится, когда вы добавите к составу не больше 20 г медного купороса.
Суть работы заключается в следующем:
- Очистить обрабатываемую деталь наждачной бумагой — это нужно для того, чтобы снять оксидную пленку. Далее покрыть медью металл в домашних условиях будет не так трудно.
- Обезжирить металлическим предмет горячим раствором соды, промыть его чистой водой.
- В подходящую по объему емкость из стекла налить приготовленный электролит.
- Опустить в жидкость две пластины из меди на подготовленных токопроводящих проводках. Между двумя пластинками из меди подвешивается уже обезжиренная деталь на таком же проводке.
Важно! Проследите за тем, чтобы пластины из меди были полность погружены в электролит.
- Далее концы проводов от пластин из меди присоединяются к положительной клемме источника тока, а деталь — к отрицательной. Далее в созданную электросеть нужно подключить амперметр с реостатом. После того, как ток подключится к цепи, реостатом нужно установить его примерно 15 мА на 1 см площади детальной поверхности.
- Далее деталь выдерживается примерно 15-20 минут.
- По истечении времени нужно отключить электропитание и вытащить обрабатываемый металл из раствора.
В конечном итоге вы заметите, что смогли покрыть медью металл в домашних условиях, ведь он полностью покроется тонкой блестящей пленкой.
Важно! Толщина медного слоя будет зависеть от того, как долго была выдержана деталь в электролите.
Гальваностегия другим способом
Данный способ отлично подойдет для металлов-исключений, что были названы ранее — цинка и алюминия.
Алгоритм работы:
- Вооружиться многожильным проводом из меди, снять изоляцию с обоих его концов.
- Растеребить мягкий провод с одной стороны, получив имитированную кисточку. Привязать к этому концу предмет, похожий на рукоятку.
- Противоположную сторону провода необходимо соединить к плюсовой клемме источника электротока.
Важно! Напряжение должно быть не более, чем 6 В.
- Подготовить электролит описанным выше способом, вылить его в широкую тару — это нужно для удобства макания туда “кисточки”.
- Положить внутрь подготовленной емкости небольшую деталь из металла. Соединить ее, используя при этом провод, к отрицательной клемме токового источника также с напряжением 6 В.
Важно! Деталь должна быть предварительно очищена и обезжирена.
- Процесс покрытия алюминия медью в домашних условиях заключается в следующем: кистообразный конец провода нужно промакивать электролитным раствором и проводить им по поверхности обрабатываемого металлического предмета, не касаясь его. Дальше — отрицательно заряженный металл притянет к себе медные ионы и ее поверхность приобретет медную пленку.
Важно! Следите за тем, чтобы между концом растеребленной проволоки и металла был маленький слой электролитного раствора (и катод, и анод обязательно должны быть смочены этим раствором).
Кому-то может будет интересно, как провести процесс омеднения в домашних условиях. Этому обучает нас видео из Ютуба, загруженное ютубером TOKARKA.
Кому может пригодится этот урок? Я думаю многие умельцы из Самоделкина захотят украсить свои предметы путем омеднения. Вот несколько способов применения на фото.
Теперь, когда вы загорелись желанием быстрее узнать как это делается, посмотрите видео и потом пошагово изучим технологию.
В первую очередь определимся, что необходимо для проведения процесса омеднения:
1) Туалетный утенок или другое чистящее средство в составе которого имеется соляная кислота.
2) Медные провода, самого мелкого сечения,кусочки меди, монеты,содержащие медь.
3) олово
4) пластиковая бутылка с водой
5) железный предмет для омеднения
В пластиковую бутылочку с водой заливается жидкость из «Туалетного утенка». Делается раствор.
В бутылочку помещается медный провод.
Закупоривается бутылочка и взбалтывается.
После этого тара ставится в теплое место примерно на месяц, чтобы произошли химические реакции. Скорость реакции зависит от концентрации раствора, количества меди и тепла.
Пока раствор готовится,надо подготовить предмет металлический для омеднения.
Металлическая поверхность очищается от пыли, грязи, ржавчины, масляных пятен, которые остаются от прикосновения пальцами.
Это достигается кипячением в растворе щелочи или в растворе пищевой соды, которая имеется в любой кухне.
Перед омеднением необходимо зашкурить поверхность наждачной бумагой N100, чтобы поверхность была шероховатой. Чем больше шероховатости, тем лучше пройдет процесс омеднения.
После зачистки шлифшкуркой идет обезжиривание, средство против обезжиривания тоже есть на кухне.
Заготовка берется заранее приготовленной салфеткой.
В пластмассовую посуду, которая выбирается по размеру заготовки, заливается раствор,предварительно размешанная в бутылке.
Хирургическим зажимом, пинцетом или даже щипчиками для ощипывания бровей заготовка опускается в раствор.
Во время омеднения емкость лучше покачивать для лучшего и быстрого прохождения реакции.
Переворачивать заготовку время от времени.
Примерно через полтора часа или больше можно уже увидеть воочию, что происходит с погруженным в раствор предметом.
На поверхности обычной стали омеднение держится очень хорошо.
Теперь говорим «спасибо» нашему мастеру TOKARKA за урок. Что дает омеднение в двух словах. Улучшается электропроводность металлических предметов, болты не пригорают к поверхности, особенно где имеются большие температуры (коллектор, глушитель и тд.) Можно применить омеднение одноразовых болтов, особенно на иномарках, когда необходимо собрать узел, а необходимых болтов нет негде. В декоративных целях.Остальное зависит от вашей фантазии. Пользуйтесь.
Гальваника крупногабаритных деталей. Элекросамоделки своими руками. — Электро самоделки — Мастеру — Сделаем сами
Гальваника крупногабаритных деталей. Элекросамоделки своими руками.Гальванические покрытия одних металлов другими отличаются от химических (без применения электрического тока) быстрым ростом толщины наносимого металла и хорошей адгезией. Известно, что гальваника предполагает наличие громоздкого электротехнического оборудования, гальванической ванны и т.п. В домашних условиях это практически не выполнимые требования. Однако умельцы решили задачу с оборудованием, как будет видно, с большим успехом.
Гальваника (с применением нового оборудования) позволяет в домашних условиях, например, посеребрить неказистый бабушкин самовар, отхромировать поржавевший бампер автомобиля, поцинковать или покадмировать инструмент (чтобы не ржавел). А то, может быть, взяться и оцинковать днище автомобиля – заветная мечта автомобилиста. Все это возможно при применении нехитрого устройства для гальваники крупногабаритных (и небольших) металлических деталей.
Устройство представляет собой следующее. Основа его – цилиндр 1 (см. рис.) из прозрачной пластмассы. Сверху у цилиндра 1 приклеена крышка 2. На ней имеются заливное отверстие 3 с пробкой и металлический контакт 4, вклеенный в крышку.
Снизу в цилиндр 1 вклеена (клей «Момент») щетина 5 от кисти, затянутая шпагатом и обвернутая несколькими витками свинцовой проволоки 6. Конец этой проволоки припаян к контакту 4. Вместо свинцовой проволоки можно использовать узкую полоску свинца, вырезанную из оболочки кабеля.
Выше над щетиной 5 вклеена мембрана 7, представляющая собой кружок пенопласта (толщиной 8-10 мм), в котором проделано несколько мелких сквозных отверстий.
В цилиндр заливают электролит. К устройству подключают зарядный агрегат для аккумуляторов, позволяющий получить силу тока до 5 А.
Плюс подключают к контакту 4, минус – к детали, которую покрывают металлом.
Через мембрану 7 и щетину 5 электролит понемногу выходит наружу. В это время своеобразной кистью натирают поверхность детали, при этом на ней начинает появляться пленка металла. Электролит собирают и еще раз используют, разбавляя его свежим электролитом.
Необходимо отметить, что качество подготовки деталей должно быть высоким (шлифовка, полировка, химическое обезжиривание, промывка дистиллированной водой).
Рассмотрим состав некоторый электролитов (все дано в г/л).
Для меди. 1. Медь сернокислая – 190, серная кислота – 70. Температура раствора
20 С, катодный ток 1 А*. Матовое меднение.
2. Медь сернокислая – 250, серная кислота – 20, хромовый ангидрид – 2.
Температура раствора 20 С, катодный ток 2,2 А. Полуматовое меднение.
3. Медь сернокислая – 200, меласса – 0,8, серная кислота – 50, тиомочевина – 0,04.
Температура раствора 20 С, катодный ток 1,8 А. блестящее меднение.
Для цинка. 1. Натрий сернокислый – 30, цинк сернокислый – 215, аммоний сернокислый – 27, декстрин – 10. Температура раствора 20 С, катодный ток 0,3 А. Блестящее цинкование.
2. Аммоний хлористый – 250, борная кислота – 23, цинк сернокислый – 250, клей столярный (сухой) – 1,5, окись цинка – 13. Температура раствора 20 С, катодный ток
0,3 А. Блестящее цинкование.
Для кадмия. 1. Кадмий сернокислый – 65, алюминий сернокислый – 30, аммоний сернокислый — 35, клей столярный – 0,6. Температура раствора 20 С, катодный ток 0,4 А.
Полуматовое кадмирование.
2. Окись кадмия – 30, аммоний сернокислый – 300, борная кислота – 20, клей столярный – 2. Температура раствора 20 С, катодный ток 0,4 А. Полуматовое кадмирование.
Для никеля. 1. Никель хлористый – 250, борная кислота – 25. Температура раствора 20 С, катодный ток 1,3 А. Полуматовое никелирование.
2. Никель сернокислый – 80, аммоний хлористый – 20, натрий хлористый – 55, борная кислота – 20. Температура раствора 20 С, катодный ток 0,35 А. Полуматовое никелирование.
3. Никель сернокислый – 150, никель хлористый – 5 , борная кислота – 30, магний сернокислый – 5, натрий сернокислый – 3, натрий хлористый – 5. Температура раствора 20 С, катодный ток 0,15 А. Блестящее никелирование.
Для хрома. 1. Хромовый ангидрид – 375, едкий натр – 50, сахар (рафинад) – 2, серная кислота- 2. Температура раствора 18 с, катодный ток 2,5 А. Полуматовое хромирование.
2. Хромовый ангидрид – 300, кальций сернокислый – 15, кальций углекислый – 60.
Температура раствора 18 С, катодный ток 2,5 А. Полуматовое хромирование.
Для серебра. 1. Серебро хлористое – 20, железистосинеродистый калий (желтая кровяная соль) – 60, натрий углекислый – 50, калий роданистый – 55. Температура раствора 20 С, катодный ток 0,05 А. Полуматовое серебрение.
2. Серебро азотнокислое – 25, сульфит натрия – 400. Температура раствора 20 С, катодный ток 0,06 А. Полуматовое серебрение.
3. Серебро азотнокислое – 20, трилон Б – 40. Температура раствора 18 С, катодный ток 0,175 А. Блестящее серебрение.
После покрытия металлом поверхность детали протирают слабым раствором кальцинированной (или питьевой) соды и промывают теплой водой.
Примечание: 1. во всех рецептах вещества должны быть чистыми («Ч»), а вода – дистиллированной.
2. Рабочая посуда – эмалированная или из жаропрочного стекла.
Сайт Пан-Ас, сайт самоделок — на сайте есть все, что можно сделать своими руками: поделки, самоделки, украшения, детские поделки. Сделай их сам, своими руками и получи от этого настоящее удовольствие.
Похожие материалы:
Меднение гальваникой и гальванопластика в домашних условиях. Гальваника своими руками в домашних условиях: технология и оборудование
Гальваника представляет собой раздел электрохимической науки, которая изучает осаждение некоторых элементов на любую поверхность. С помощью гальваники в домашних условиях или в промышленности можно нанести на изделие тонкий слой металла, который будет выступать в роли защитного слоя или выполнять декоративные функции. В последнее время декоративное покрытие набирает популярность у тех, кто хочет сделать оригинальный подарок своим друзьям и родным.
Общие сведения
Покрытие гальваникой бывает технологическим или декоративно-защитным. Это тонкий металлический тонкий слой, который в зависимости от гальванических элементов может выполнять эстетические функции. Гальванопластика не увеличивает прочность изделия, поскольку в этом случае требуются большие производственные мощности, но для красоты и придания «свежести» вполне подойдет.
Гальванические реакции происходят с помощью постоянного электрического тока. В специальную емкость-диэлектрик наливают раствор — электролит, в который погружают два анода. Аноды должны быть изготовлены из металла, который будет осаждаться на покрываемом изделии.
Обрабатываемая деталь присоединяется к минусовому выводу и помещается между анодами. Она выполняет роль катода. Аноды, в свою очередь, присоединяются к плюсовому контакту источника питания. Они становятся частью цепи, проводя ток в электролит и отдавая ему свои металлические элементы. Электролит передает необходимые частицы обрабатываемой детали, они постепенно обволакивают её тонким слоем. Аноды по площади должны превышать в несколько раз размер заготовки.
Другими словами, гальванизация представляет собой перенос молекул металла раствора на изделие в момент протекания через них электротока.
Любой гальванический процесс можно разбить на общие этапы:
- Сборка гальванической установки.
- Подготовка электролитного раствора.
- Обработка и подготовка образца.
- Запуск гальванического процесса.
Оборудование можно подготовить самостоятельно. Сначала подбирается подходящий источник питания. Это может быть батарейка (для обработки изделий небольшого размера) или аккумулятор. Подойдет понижающий блок питания, который выдает на выходе постоянный ток до 12 вольт. Иногда используют инвертор от сварочного аппарата. Подбирается реостат для регулирования силы тока.
Из нейтрального, устойчивого к химически агрессивным веществам материала подбирается широкая и глубокая ванночка. Надо учитывать, что электролитический раствор при гальваническом процессе может нагреваться до девяноста градусов по Цельсию.
Подготавливаются две пластины, которые будут токопроводящими анодами.
Для нагрева ёмкости с электролитом нужен электрический прибор с возможностью плавной регулировки температурного режима. Чаще всего используют подошву утюга или небольшую электроплитку. С их помощью происходит нагрев раствора до необходимой температуры и ускорение реакции.
Химические реактивы необходимо хранить в плотно закупоренной стеклянной посуде. Желательно каждый предмет подписывать.
Потребуются весы для точного измерения массы веществ, поскольку необходимая точность веса компонентов составляет один грамм. Такие весы можно приобрести, а можно сделать самостоятельно, используя вместо гирек старые советские монеты. Вес «желтых» монет точно соответствует их номиналу.
После того как собраны необходимые вещества, найдены ёмкости, собрана электрическая схема с питанием и подготовлена система подогрева, можно заняться чисткой заготовки.
Если недостаточно хорошо почистить деталь, гальваническое покрытие непрочно осядет или будет неравномерным. Иногда хватает простого обезжиривания предмета. Раствор ацетона или спирта может хорошо обезжирить поверхность, можно использовать бензин.
Некоторые мастера держат изделия из стали в разогретом до 90 градусов по Цельсию растворе фосфорнокислого натрия. Цветные металлы можно очищать в том же растворе, не нагревая его.
Если на изделии есть коррозия или другие изъяны, то поверхность заготовки шлифуется наждачной бумагой.
Иногда про технику безопасности при различных работах в домашних условиях рассказывают вскользь. Но при выполнении любых гальванических работ нужно строго соблюдать безопасность.
Опасность заключается в использовании токсичных химических веществ, высокой температуре нагрева раствора и повышенными рисками, которые сопровождают электрохимические реакции.
Лучше всего гальванические работы проводить в гараже или мастерской при обязательном проветривании или вентилировании помещения. Особое внимание следует уделить заземлению оборудования. Нужно соблюдать меры личной безопасности, а именно:
- Дыхательные пути следует защитить респиратором.
- Руки и запястья должны быть спрятаны в высокие и прочные резиновые перчатки.
- Обувь должна защищать от ожогов, а одежда прикрыта клеенчатым фартуком.
- Обязательно ношение специальных защитных очков.
Перед началом работ по меднению в домашних условиях нужно подготовить необходимые материалы и оборудование. Надо позаботится об источнике напряжения и постоянного тока. Существует много рекомендаций касательно силы тока, разброс которого может быть большим. Поэтому желательно иметь реостат с возможностью плавной регулировки напряжения и для постепенного завершения процесса. Источником может служить автомобильный аккумулятор или выпрямитель с напряжением на выходе не больше 12 вольт. Для первых опытов будет достаточно обычной батарейки от 4.5 до 9 вольт.
Затем выбирается ёмкость для электролитического раствора, лучше всего из жаропрочного стекла. В любом случае все ёмкости для электролиза должны быть диэлектриками и выдерживать температуру не менее, чем 80 градусов по Цельсию.
В качестве анодов подойдут два больших медных листа. Они должны перекрывать по размеру заготовку. Из химических реактивов потребуются:
- Купорос медный.
- Кислота соляная либо серная.
- Вода дистиллированная.
Меднение в домашних условиях пользуется заслуженной популярностью, поскольку очень хорошо и надежно держится на стальных изделиях. Главное условие — правильно соблюдать технологию процесса.
Имеется два способа нанесения меди на поверхность:
- Помещение заготовки в раствор электролита.
- Неконтактный способ. В этом случае изделие не погружается в раствор.
Подготавливается и обрабатывается поверхность изделия при помощи тонкого наждака и щеточки. После этого деталь моется в проточной воде, обезжиривается и еще раз промывается.
Этапы процесса омеднения следующие:
- Два медных анода подключают в сеть к положительным контактам и размещают их в стеклянную банку.
- К обработанному изделию подводят контакт с отрицательным значением напряжения и свободно подвешивают между анодами.
- Подключают реостат согласно электрической схеме для возможности регулирования силы тока.
- Подготавливается раствор в правильных пропорциях. На 100 г дистиллированной воды надо 20 г медного купороса и 2−3 г соляной кислоты. Вместо соляной кислоты можно использовать другую.
- Раствор выливается в посуду с медными пластинами и деталью таким образом, чтобы они полностью скрылись под поверхностью раствора.
- Подключается источник напряжения. Реостатом добиваются необходимой силы тока из примерного расчета 10−15 миллиампер на каждый квадратный сантиметр площади детали.
Весь процесс занимает примерно 15−20 минут. После обязательного выключения источника питания и остывания раствора готовое изделие с медным слоем на поверхности вынимается из банки.
Этот метод интересен тем, что его можно использовать для обработки не только стальных предметов, но и сделанных из других материалов. Например, алюминия и цинка. Порядок процесса следующий:
- Из многожильного медного провода изготавливается «кисточка». Конец провода оголяется. Из медных проводков создается подобие кисточки, чтобы затем прикрепить ее к деревянной ручке-держателю.
- Второй конец провода подключается к плюсовому контакту электрической цепи.
- В широкую ёмкость заливается стандартный электролитный раствор из медного купороса и соляной кислоты.
- Предварительно очищенная и промытая металлическая заготовка присоединяется к отрицательному контакту и размещается в пустой ёмкости.
- Импровизированная кисточка окунается в раствор электролита и проводится по поверхности заготовки без контакта. Это действие повторяется до получения результата.
Когда деталь полностью покроется слоем меди, выключается блок питания и процесс завершается. Деталь ополаскивается в воде и просушивается.
Часто с помощью медного электролиза обновляют столовые приборы, сделанные из алюминия. Если нет опыта проведения этого процесса, то можно потренироваться нанести медь на алюминиевые пластинки. Порядок проведения процесса:
Гальванопластика — это электрохимический способ придания предмету определенной формы с помощью осаждения на него металла. Чаще всего этот метод используют при обработке металлом неметаллических предметов или при изготовлении копий ювелирных изделий.
Если при гальванопластике изделие не обладает электропроводящими свойствами, то его предварительно покрывают графитом, иногда бронзой. Затем мастер делает с копии слепок и начинает гальванический процесс. В качестве материала слепка используют гипс, графит или легко плавящийся металл.
Гальваника — это очень интересный и познавательный процесс, но он связан с активными веществами, которые могут навредить здоровью и нанести вред имуществу или окружающей среде. Поэтому перед тем как начинать гальванику своими руками, нужно принять все меры безопасности, изучить немного теории процесса и особенности поведения химических реактивов.
Основной задачей гальванического покрытия медью в домашних условиях или по-другому меднения является подготовка поверхности металла к его дальнейшей обработке. Такой операции могут подвергаться различные металлы, и не металлы, среди которых следует выделить:
- сталь,
- латунь,
- никель и другие.
Использование меди
Благодаря своим многочисленным преимуществам данный металл получил широкое распространение. На сегодняшний день медь и ее многочисленные сплавы широко используются в промышленности. Металл актуальный для авиастроения, автомобилестроения, приборостроения и других отраслей. Не меньшей популярностью металл и изделия из него пользуются и в бытовой сфере. Меднение само по себе является одним из лучших способов покрытия тонким слоем металлической поверхности. В домашних условиях меднение можно выполнить нескольким способами.
Гальваническое меднение в домашних условиях
Для этого понадобится:
- Вода;
- Соляная кислота в чистом виде.
Гальваническое меднение в домашних условиях
Приготовления раствора
Делаем насыщенный раствор медного купороса, после чего нужно будет добавить 1/3 этого раствора в соляную кислоту. После приготовления раствора медного купороса его следует тщательно размешать, чтобы не было частиц. Далее нужно соляную кислоту тонкой струйкой добавить в этот раствор. Не следует забывать про технику безопасности и использовать перчатки и защитные очки. После того, как вы добавили в раствор соляную кислоту, его следует тщательно перемешать.
Итак, раствор готов и можно приступать к меднению в домашних условиях. Для этого нужно взять металлическую деталь, на которую вы собрались наносить слой меди и подготовить ее к работе. Подготовка включает в себя ее обработку наждачной бумагой. Данная процедура позволяет не только зачистить металлическую поверхность, но и обезжирить ее. Такая же процедура будет актуальна и для детали из латуни или свинца. После этого, покрытие нужно тщательно промыть в растворе кальцинированной соды. Это позволит более тщательно обезжирить материал.
Кальцинированная соды для обезжиривания материала
Далее поверхность нужно погрузить в раствор медного купороса и соляной кислоты. Следует обратить внимание на то, что первый слой меди является очень тонким и слабым, поэтому его желательно снять при помощи металлической щетки. После того, как вы это сделали, поверхность стали или свинца следует повторно промыть в растворе кальцинированной соды и опять погрузить в раствор для меднения. Данные манипуляции приведут к тому, что слой меди в домашних условиях на поверхности будет гораздо толще и гораздо крепче, поскольку его убрать можно будет с предмета, только используя наждачную бумагу, а не металлическую щетку как прошлый раз.
Этот способ позволяет сделать очень качественное медное покрытие, которое можно снять только наждачкой. Для улучшения медного покрытия в домашних условиях следует деталь еще раз погрузить в раствор. Указанный способ отличается своей простотой и высокой эффективностью в том числе и для изделий из свинца.
Процедура меднения
Меднением принято называть процедуру гальванического нанесения меди, толщина слоя меди в таких случаях может составлять-от 300 мкм и больше. Меднение стали это один из наиболее важных процессов в гальванике, поскольку используется, как дополнительный процесс перед нанесением других металлов для хромирования, никелирования, покрытие серебром.
Слой меди прекрасно держится на стали и способен выравнивать различные дефекты на поверхности.
Для медных покрытий характерно высокое сцепление с другими поверхностями, изделиями из свинца особенно металлическими, а также высокая электропроводность и пластичность. Нанесенное недавно покрытие имеет ярко-розовый матовый или же блестящий цвет. Под воздействием влияний атмосферы медные покрытия могут окисляться, покрываться налетом окислов с различными пятнами радужного вида.
Сферы использования омеднения
Как правило, гальваническое омеднение может использоваться:
- В декоративных целях. С учетом огромной популярности в нынешнее время старинных изделий из меди. Существуют методы искусственного состаривания изделий из стали;
- В гальванопластике. Широко распространена в ювелирной сфере, среди сувенирной продукции, для изготовления барельефов и т.д;
- В технической отрасли. Меднение металла очень важно в электротехнической области. Низкая стоимость меднения по сравнению с покрытиями из золота или серебра позволяет снизить расходы на изготовление электродов, электротехнических шин, контактов и других элементов из сталии свинца.
Меднение происходит вместе с нанесением других гальванических покрытий
- Если нужно нанести многослойное защитно-декоративное покрытие на слой стали. В подавляющем большинстве случаев здесь медь используют вместе с никелем и хромом. Это позволяет улучшить сцепление с основным металлом и получить блестящее покрытие высокой прочности;
- Во избежание цементации участка. Меднение свинца позволит избежать появления углероживания на стальных участках. Для нанесения медного слоя используют только те участки, на которых будет проводиться обработка резанием;
- При выполнении реставрационных и восстановительных работ. Данный метод наиболее часто используется для восстановления хромированных частей автомобилей и мотоциклов. Для этих целей наносится довольно толстый слой меди, порядка 100-250 мкм и более того, что позволяет закрыть все дефекты и повреждения металла для нанесения последующих покрытий;
Разновидности меднения
- Используя погружение в электролит;
- Без погружения в электролит.
Первый способ предполагает обработку металлического изделия наждачной бумагой, щеткой и промывки водой. После чего обезжиривания в горячем содовом растворе с повторной промывкой. Далее в стеклянную емкость опускают на медных проволочках две медные пластины –аноды. Между пластинками на проволоке подвешивают деталь, после чего пускается ток.
Второй способ актуальный для изделий из стали, алюминия и цинка.
Домашнее омеднение
Данная процедура актуальна для различных случаев, поскольку нанесение слоя меди может использоваться для алюминиевых столовых приборов, сувениров, подсвечников и т. д. Неповторимый эффект оказывают изделия не из металла, на которые был нанесен слой меди. Это могут быть стебли растений, листья и др. Ввиду того, что в покрываемых предметах отсутствует токопроводящий слой, вместо него используется специальный электропроводный лак, который наносят на поверхности.
В состав лака входит ряд органических растворителей, пенкообразователей и тонкодисперсионный графитовый порошок, благодаря которому создается электропроводность. Лак наносят тонким слоем на сухую поверхность, и после высыхания через час можно приступать к омеднению. При желании можно меди придавать различные цветовые оттенки, используя для этого специальные способы. Высокое качество и уникальность таких изделий вполне заслуженно приравнивается к настоящим ювелирным украшениям.
Видео: Меднение в домашних условиях
Те, кто хорошо помнит школьную программу по курсу «Химия», сразу ответят на вопрос, что такое гальваника. Тем, кто немного подзабыл, напомним, что это раздел электрохимии, так называют процесс, когда на практически любое изделие наносится покрытие из металла. Этот процесс применяется и в промышленных масштабах, например, как при оцинковке или хромировании металлических изделий, так и при изготовлении декоративных предметов.
Процесс оседания электролитов на нужную поверхность достаточно сложный, требует соблюдения техники безопасности и определенных навыков обработки дома. Гальваника в домашних условиях не позволит вам усилить прочность металлического изделия (для этого нужны промышленные мощности), но может использоваться для декорирования отдельных предметов.
Для организации процесса вам потребуется:
- Гальваническая ванна своими руками – банка (из стекла или прочной пластмассы, достаточна большая, чтобы поместилось обрабатываемое изделие, термостойкая) с раствором электролита.
- Провод, разделенный на анод («плюс») и катод («минус»). При этом аноды должны быть по площади больше, чем обрабатываемое изделие. Они проводят ток в электролит и замещают убыль металла в нем, того, что будет оседать на гальванируемом изделии.
- Оборудование для взвешивания, например, точные электронные весы.
- Источник постоянного тока с регулировкой напряжения, домашняя розетка не подойдет.
- Электроплитка с обязательной регулировкой температурного режима.
Сам процесс нанесения гальванического покрытия в домашних условиях достаточно прост: в емкости развести электролит, нагреть, погрузить туда аноды, подключенные к «плюсу», на расстоянии закрепить гальванируемое изделие (в нашем случае – катод), который подключают к «минусу». При подключении к источнику тока металл из электролита начинает оседать на «минусе», то есть на изделии.
Что нужно для приготовления электролита?
Как сделать электролит дома? Сначала выберем правильную посуду для хранения: это должна быть емкость из неактивного вещества (стекла или пластика), прочная, плотно закрывающаяся крышкой, чтобы избежать доступ кислорода для электролита.
Совет! Выпрямитель для гальваники своими руками легко получается из обычного автомобильного аккумулятора.
Химия – наука точная. Каждое используемое вещество придется отмерять с точностью до сотых грамма. Вам потребуется качественное весовое оборудование, удобнее всего электронное. Если возможности или желания купить весы нет – берите мелочь советского периода, монеты тогда имели точный вес.
Самое труднодоступное для простого гражданина – приобретение реактивов для изготовления электролита. Многие вещества запрещены к продаже физическим лицам, только промышленным предприятиям при наличии особого разрешения. Простым людям опасные реактивы не продадут!
На видео: Ток 60А в домашних условиях или кустарная гальваника.
Как подготовить изделие
Собрав вес необходимых компонентов, подготовив емкости, систему подогрева и источник тока, переходим к подготовке изделия, которое хотим обработать.
Чтобы металл из электролита ровным слоем осел на предмет, его нужно очень хорошо очистить, иначе гальваническое покрытие в домашних условиях получится неровным и непрочным. Некоторые предметы достаточно будет просто обезжирить, некоторые потребуют чистки наждачной бумагой и шлифовки, чтобы удалить с поверхности коррозию и «заусенцы».
Важно! Качественное обезжиривание обеспечивает раствор ацетона, спирт и даже бензин.
Стальные изделия держат несколько минут в растворе фосфорнокислого натрия, разогретого до 90 градусов. Цветные металлы обезжиривают тоже в растворе натрия, только без подогрева.
Техника безопасности
Прежде чем начинать процесс гальванизации, не забудьте о технике безопасности. Гальваника своими руками не подразумевает проведения манипуляций, например, на кухне. Речь идет скорее о гараже или сарае, нежилом месте с хорошей вентиляцией, где можно организовать заземление.
Важно! Не отравитесь ядовитыми испарениями! Гальванизация может нанести реальный вред здоровью. Организуйте вытяжку и закройте лицо маской-респиратором.
На руки обязательны плотные резиновые перчатки. Глаза защитите очками. Перед началом манипуляций почитайте специальную литературу. При каких-либо проявлениях недомогания незамедлительно обратитесь к врачу.
Варианты обработки
Нанесение покрытия из никеля на металлические предметы – несложный процесс, в результате которого ваши изделия получат роскошный блестящий вид, станут более стойкими к дождю и прочим явлениям.
От вас потребуется:
- Приготовить электролит для гальваники, смешав сульфат никеля, натрий, магний, хлористый натрий (поваренная соль) и борную кислоту. Проверьте рН, он должен быть в диапазоне 4–5.
- Разогрейте электролит до 25 градусов.
- Поместите в емкость изделие и подключите ток 1,2 А/кв. дм.
- Примерное время – около получаса.
Указанное время зависит от таких факторов, как размер изделия, плотность тока и температура электролита. Чем больше время, тем толще получится слой наносимого никеля. По окончании промойте предмет и отполируйте любой полировочной мазью.
На видео: химическое никелирование.
Хромирование
Один из самых популярных способов придания прочности и внешнего вида изделиям из металла – хромирование. Пусть дома добиться высокой прочности не удастся, для этого нужен ток плотностью 100 А/кв. дм., декоративное покрытие нанести вы все же сможете.
Покрытие из хрома пористое. Перед его применением предмет покрывают медью или никелем. Зато домашнее хромирование позволяет добиться большего разнообразия оттенков, что достигается разной температурой электролита: чем она выше, тем более блестящим получится покрытие.
Процесс хромирования в домашних условиях выглядит следующим образом:
- Аноды из свинца, олова и сурьмы (85%/11%/4%).
- Погрузите изделие в электролит нужной вам температуры и подождите около получаса.
- Промойте в слабом растворе пищевой соды, просушите, отполируйте.
На видео: декоративное хромирование в домашних условиях.
Меднение
Покрытие поверхностей металлов медью в домашних условиях применяют для создания слоя, который будет впоследствии проводить ток, или для защиты от коррозии.
Сделать гальванику медью дома на черных металлах в домашних условиях невозможно, поскольку для этого используются смертельно опасные цианиды. Первоначально стальные и чугунные предметы надо никелировать, а затем уже проводить гальванизацию меднением с использованием солей медного купороса, разведенных в серной кислоте. Покрытие медью алюминиевых изделий потребует первоначальной очистки последних от окиси в электролите, содержащем серную кислоту, а потом гальванизируют также, как и сталь.
На видео: гальваническое меднение.
Цинкование
Самый простой в домашнем исполнении метод гальванизации – это обработка цинком. Его используют для защиты предметов из металла (электропроводящих и неэлектропроводящих) от появления коррозии. При цинковании в электролит в качестве анода погружают пластинку из цинка, соответствующую по площади оцинковываемому предмету, и подключают к источнику тока.
В состав электролита входит: сернокислый цинк (200 г), сернокислый аммоний (50 г), уксусный натрий (15 г) из расчета на 1 л воды. Примерно за полчаса анод растворится и его молекулы плотным слоем покроют обрабатываемый предмет.
На видео: оцинковка металла в домашних условиях.
Латунирование
Самый декоративный метод гальваники – латунирование (нанесение пленки из сплава меди и цинка). Покрытые латунью изделия используют для мебельной фурнитуры, в качестве дверных ручек и т.д. Латунь придает предметам благородный золотой цвет и насыщенный блеск.
Электролит для латунирования должен содержать соли меди и цинка, растворенные в растворе цианида. Данный вид гальванизации также не рекомендуется для применения в домашних условиях из-за возможности отравления цианидами.
Каким бы ни был увлекательным процесс гальванизации, повторять его дома без предварительной подготовки не рекомендуется – может быть опасно для жизни. Оборудование стоит денег, а некоторые необходимые для изготовления электролитов реагенты вы просто не сможете приобрести. Затевать процесс, например, для хромирования одной детали того не стоит – дешевле будет обратиться в специализированные предприятия.
Серебрение и золочение
Гальваническое нанесение серебра на изделия имеет не только декоративное предназначение, оно также защищает от появления коррозии и образует электропроводящее покрытие. Как и в случае с медью, чугунину и сталь предварительно покрывают никелем, затем серебрят.
Электролит для серебрения содержит:
- хлористое серебро;
- железноцианистый калий;
- кальцинированную соду;
- дистиллированную воду.
Электролит необходимо подогреть до температуры до 20 градусов. Высокой мощности не требуется – хватит 0,1 А/кв. дм. Анодом станет пластина из графита, размером, соответствующем размеру гальванизируемого изделия.
Гальваника золотом — наиболее декоративный метод.
Для этого потребуется подогретый раствор золота в пропорциях 5 г на 1 л воды, смешанный с синеродистым калием. Можно использовать и холодный электролит, но тогда золота необходимо будет в 3 раза больше.
Будьте крайне аккуратны – испарения синеродистой кислоты крайне опасны, как в горячем виде, так и в холодном. Не пренебрегайте вентиляцией, не допускайте попадания ее на открытые участки кожи. При возможности замените её на железистосинеродистый калий.
Предварительно тщательно очистите изделие. Если оно выполнено из черного металла, покройте сначала медью, затем золотите. Чтобы золото лучше «приставало», окуните изделие в азотнокислую ртуть.
На видео: гальваническое золочение серебряной ложки.
Главное правило: аккуратно при использовании тока – он должен быть не мощнее 1 А/кв. дм. Более сильный ток приведет к тому, что золото будет черными хлопьями падать на дно емкости, а гальванизируемый предмет вместо золотого превратится в бурый. После окончания процесса изделие просушивают и полируют с применением полировочной мази.
Гальванопластика и гальваностегия
Что такое гальванопластика? Это метод, который применяется для изготовления точных копий изделий, метод копирования. Его применяют, когда необходимо сделать копию с предметов тончайшей конфигурации – пластинок, чипов и схем. Гальваностегия позволяет усилить механические свойства одного металла путем нанесения на него слоя другого металла, например, хромирование и никелирование стали, никелирование меди и т.д.
Гальванопластика и гальваностегия имеют схожую природу, отличаются лишь способом подготовки металла перед обработкой. При осуществлении гальваностегии поверхность металла должна быть максимально подготовленной для сцепления с наносимым металлом. Метод гальванопластики, наоборот, подразумевает свободное отделение наносимого металла.
Для гальванопластических процессов применяют чаще всего медь, никель и серебро, а в гальваностегических – практически все виды металлов. Гальванопластика в домашних условиях проводится на том же оборудовании, что и другие гальванические процессы.
Под гальванопластическую ванну прекрасно подойдет большая стеклянная емкость.Её размеры зависят от величины гальванизируемого предмета, поскольку он не должен располагаться слишком близко от анодной пластины.
Гальванопластика дома может применяться для изготовления копий предметов небольшого размера по предварительно отлитым из легкоплавких металлов формам.
Мастер-класс по гальванике (1 видео)
Предметы с гальваническим покрытием (17 фото)
Гальванопластика — техника электролитического осаждения металлов на поверхности различных предметов (матриц) с целью получения точных металлических копий — впервые была разработана и применена на практике в 1838 году русским ученым, академиком Б. С. Якоби. При его непосредственном участии было изготовлено много замечательных произведений искусства, статуи и барельефы для Исаакиевского собора, Эрмитажа, Зимнего дворца, Петропавловского собора, в том числе знаменитая квадрига для фронтона Большого театра в Москве.
Гальванопластика основана на кристаллизации металлов из водных растворов их солей при пропускании через них постоянного электрического тока. Этот процесс называется электролизом.
Ток подводится с помощью двух металлических пластин — электродов, помещенных в электролит. Пластина, соединенная с положительным полюсом источника тока, называется анодом. Другая пластина, соединенная с отрицательным полюсом источника тока, — катод.
В гальванопластике катодами служат предметы (матрицы), на которые осаждается металл, а анодами — пластины или прутки металла, которым этот предмет (матрицу) покрывают.
Схематически процесс электролиза представлен на рисунке 1. При прохождении тока через электролит анод притягивает к себе отрицательно заряженные ионы, а катод — положительно заряженные ионы. Когда ионы достигают электродов, они теряют заряд, выделяясь в виде нейтральных атомов или групп атомов.
Гальванопластика широко применяется в промышленности для изготовления прессформ, полых тонкостенных трубок, сложных деталей с толщиной стенок от нескольких микрон до десятков миллиметров. Габариты деталей ограничиваются только объемом электролитных ванн.
Матрицы изготавливают из пластмасс, стекла, нержавеющей стали, алюминия, различных легкоплавких сплавов, свинца. На поверхность матрицы из изоляционного материала предварительно наносят электропроводный слой.
Матрицы бывают разрушаемые и постоянные. Первые изготавливают из легкоплавких металлов и из сплавов пластмасс. Материалом для изготовления вторых служат сталь, медь, никель или алюминий и его сплавы.
Для изготовления металлических трубок в домашних условиях необходимы ванночка из стекла, керамики или винипласта, медный купорос, серная кислота, реостат на 20 Ом (максимальный ток 1 А), амперметр с током максимального отклонения стрелки 1 А, источник питания, проволока (медная, стальная или из легкоплавких материалов и их сплавов, например, оловянисто-свинцовых) в качестве матрицы.
Диаметр проволоки соответствует внутреннему диаметру изготавливаемой трубки, а длина первой должна быть вдвое больше длины второй.
Если нужны трубки с внутренним диаметром меньше 1 мм, в качестве матрицы используют стальную проволоку. При изготовлении трубочек с внутренним Ø 5 мм и более матрицу делают из легкоплавких металлов и их сплавов (например, прутковый припой).
Проволока должна быть гладкой и ровной. Для этого ее шлифуют мелкой наждачной бумагой, а затем доводят микрошкуркой («нулевкой»). Затем проволоку облуживают, излишки припоя снимают, протягивая нагретую проволоку через зажатую в кулаке тряпочку. Нерабочие участки матрицы покрывают пластилином.
В теплой воде (50-60° С) растворяют медный купорос (200-250 г соли на 1 л воды), воспользовавшись стеклянной посудой. Отстоявшийся электролит фильтруют и затем в него вливают серную кислоту из расчета 50-60 г на 1 л раствора.
Следует помнить, что вливать раствор в концентрированную серную кислоту нельзя. Соприкасаясь с водой, она вызывает бурную реакцию с большим выделением тепла и парообразованием. В результате может произойти выброс кислоты из сосуда. Поэтому лить надо кислоту в раствор медного купороса тонкой струйкой, непрерывно помешивая деревянной палочкой.
Чтобы медный осадок был плотным и мелкозернистым, в электролит рекомендуется добавить немного этилового спирта (5-10 г на 1 л электролита).
Готовый электролит переливают в рабочую ванночку, куда уложены матрицы и медная пластинка или проволока.
Матрицы подключаются к «минусу», а медная пластинка или проволока к «плюсу» источника питания. Площадь анода должна быть в 5-10 раз больше площади катода.
Схема установки для домашней гальванопластики представлена на рисунке 2. Трансформатор блока питания имеет следующие данные: сердечник Ш20Х20, обмотка I содержит 2200 витков провода ПЭВ-1 0,12 (на 220 В) или 1300 витков ПЭВ-1 0,15 (на 127 В), обмотка II-35 витков ПЭВ-1 0,8.
Процесс электролиза и качество покрытия зависят в основном от состава электролита, его температуры и плотности тока.
Температура электролита 18-25° С.
Плотность тока — величина тока, приходящаяся на единицу поверхности, — рассчитывают по формуле:
где i – ток в цепи, А,
S – поверхность изделия, дм 2 .
На практике j=1-1,5 A/дм 2 .
Пример 1. Определить величину рабочего тока электролиза для изготовления трубки с наружным Ø 5 мм и длиной 100 мм. Возьмем плотность тока равной 1 А/дм 2 , тогда
I=jS=1*3,14*0,05*1 =0,16А.
Расчет времени выдержки деталей под током в гальванической ванночке для получения слоя толщиной σ мм определяется по формуле:
t=σ*d*1000/j*C*η,
где t — время выдержки, ч.;
σ — толщина трубки, мм;
d — удельный вес меди, г/мм 3 ;
j — плотность тока, А/мм 2 ;
С — электрохимический эквивалент меди, г/А-ч; η — расчетный выход по току.
Конкретно для нашего случая имеем
d = 8,95 г/мм 2 , i = 1 А/мм 2 ; С = 1,186 г/А-ч; η = 95.
Пример 2. Определить время выдержки матрицы под током в гальванической ванночке для получения медной трубки с толщиной стенок 0,5 мм.
t=σ*d*1000/j*C*η=0,5*8,95*1000/1*1,2*95= 40 час.
По истечении расчетного времени матрицу извлекают из гальванической ванночки и промывают водой. Конец проволоки на расстоянии 1,5-2 мм от трубочки обкусывают и после прогревания до температуры 200-250° С наращенная трубочка легко снимается с матрицы.
Таким же способом изготавливают трубки из никеля, хрома, железа.
В. БУШУЕВ, А. НОВИКОВ, г. Воронеж
Заметили ошибку? Выделите ее и нажмите Ctrl+Enter , чтобы сообщить нам.
Что такое гальваника и с чем ее едят?
Гальваникой называют раздел электрохимии, включающий в себя два подраздела, которые изучают осаждение электролитов на поверхности металла с разными целями. Например, защита от коррозии. В жизни такое же название носит и сам процесс покрытия изделий, например, хромом или медью. В последнее время стала очень популярна декоративная гальваника в домашних условиях, которая приносит немалый доход тем, кто готов поработать.
Что в составе
Гальваника — достаточно размытое определение, включающее в себя несколько процессов, название которых связано с применением различных электролитов. Пример — золочение, т. е. покрытие тонким слоем золота, или хромирование. Также популярно медение и серебрение.
Гальваника в домашних условиях. Возможно ли это?
Декоративное покрытие различных предметов металлом становится все популярнее среди начинающих предпринимателей. Прежде всего благодаря тому, что стартовые вложения сведены к минимуму. Но гальваника в домашних условиях — не самая лучшая идея по одной простой причине: токсично. Лучше подобрать хорошо проветриваемое нежилое помещение. И прочитать соответствующую литературу на эту тему, чтобы быть готовым ко всему.
Необходимое оборудование для гальваники
Все необходимое для первого опыта возможно сделать своими руками или приобрести без особых затруднений. Сам процесс связан с действием силы тока, поэтому необходим блок питания. У него должен быть регулятор напряжения, а сила тока на выходе — один Ампер. Также нужна небольшая ванночка из токонепроводящего, химически стойкого материала, например пластиковый лоток с тонкими стенками. Также домашняя гальваника требует наличия специальной кисточки или ручки, которая представляет собой полую форму, в которую заливается электролит.
Технологический процесс
Гальванические процессы происходят под действием тока. В специальную ванночку устанавливаются два анода и заливается электролит. Обрабатываемую деталь подключаем к «минусу», а аноды — к «плюсу». При замыкании цепи металл, содержащийся в электролите, осаждается на рабочий объект. Приготовление раствора для каждого металла индивидуально, причем пропорции необходимо строго соблюдать, так же как и силу тока, изменение которой может значительно повлиять на процесс.
Гальваника в домашних условиях. Подготовка деталей
Прежде чем приступать к самому процессу, с рабочих объектов необходимо удалить загрязнения. В некоторых случаях достаточно обойтись лишь обезжириванием поверхности, но иногда приходится прибегать к шлифовке и другим более сложным способам.
Домашняя гальваника опасна для здоровья
Химический процесс всегда связан с риском, поэтому необходимо соблюдать элементарные правила безопасности:
- позаботьтесь о наличии заземления;
- хорошая вентиляция помещения обязательна;
- необходимо соблюдать правила личной безопасности при работе с вредными веществами.
В качестве заключения
Помните, что гальваника — очень опасный процесс, связанный с применением активных веществ, которые могут нанести вред вашему здоровью и имуществу. Поэтому внимательно изучите все опасные аспекты и лишь тогда принимайтесь за работу.
Химия «сделай сам»: научитесь гальванике
Адам Гольфер
Когда вы видите тонкий слой металла — на чем угодно, от хромированных деталей автомобилей до сверл и ювелирных изделий — гальваника, вероятно, работает. Процесс прост: пропустите ток через раствор соли металла, чтобы покрыть проводящую поверхность ионами металла. В этом проекте мы покрываем графит (в виде карандашного рисунка) медью, материалом электропроводки.Это превращает изображение в цепь, которая может подавать питание на светодиод. Новый способ подключить ваш дом? Нет. Круто? Определенно.Принадлежности
• Медный купорос (например, Zep Root Kill)
• Белый уксус
• Пластиковая трубочка
• Прозрачная пленка
• Наждачная бумага, лента
• № 2 карандаш
• Аккумулятор 9 В
• Грифель механический карандаш № 2
• Два набора соединителей типа «крокодил»
• Светодиод с присоединенным резистором
1. В прозрачной миске смешайте 3 столовые ложки медного купороса с 1 стаканом белого уксуса. Перемешайте соломинкой. Когда уксус становится синим, медь растворяется.
2. Используйте мелкую наждачную бумагу для придания шероховатости куску прозрачной пленки.
3. Нарисуйте изображение на поцарапанной пленке карандашом № 2. Изображение должно состоять из одной толстой линии и доходить до края пленки.
4. Прикрепите красный зажим типа «крокодил» к положительной клемме 9-вольтовой аккумуляторной батареи.Другой красный зажим закрепите на графитовом механическом карандаше.
5. Закрепите зажим из черной кожи аллигатора на отрицательной клемме аккумулятора. Прикрепите второй черный зажим к краю рисунка.
6. Не позволяя зажиму из крокодиловой кожи касаться жидкости, погрузите пленку в чашу. Приклейте зажим к краю чаши.
7. Погрузите грифель карандаша в раствор. Приклейте к миске зажим из кожи аллигатора. Растворенная медь будет нанесена на ваш рисунок.(Вы увидите, как на поводке образуются пузыри.)
8. Когда рисунок будет полностью покрыт медью, отсоедините зажимы от аккумулятора и просушите рисунок бумажным полотенцем.
9. Проверьте медь с помощью двух отдельных плакированных рисунков. Подключите один рисунок к положительной клемме аккумулятора с помощью зажима типа «крокодил», а другой — к отрицательной клемме с помощью второго зажима. Прикоснитесь к каждому рисунку одной ножкой светодиода; да будет свет!
Сара Хансен преподает химию в Колумбийском университете и занимается изучением химии в педагогическом колледже Колумбийского университета.
Этот контент создается и поддерживается третьей стороной и импортируется на эту страницу, чтобы помочь пользователям указать свои адреса электронной почты. Вы можете найти больше информации об этом и подобном контенте на сайте piano.io.
Гальваника в домашних условиях — Простой метод гальваники
Гальваника в домашних условиях — Простой метод гальваники — Перед тем, как приступить к гальванике медью, серебром или другим металлом, тщательно очистите изделия, так как малейшее пятно жира или грязи предотвратит образование отложений. придерживаясь.
Затем отполируйте изделия и протрите их тканью с мелким порошком пемзы, чтобы слегка придать поверхности шероховатость.
Выдержка из книги: МАЛЬЧИК МЕХАНИЧЕСКИЙ ОБЪЕМ I / 700 ЧЕМ МОЖНО СДЕЛАТЬ С 800 ИЛЛЮСТРАЦИЯМИ 1913, HH WINDSOR CHICAGO POPULAR MECHANICS CO. PUBLISHERS
Наконец, чтобы удалить все следы смазки, окуните предметы, которые нужно покрыть в кипящем растворе поташа, полученном путем растворения 4 унций. Ясень американский в 1-1 / 2 балла. воды.
Больше не прикасаться к работе руками.
Чтобы не прикасаться к нему, повесьте предметы на тросы, на которых они будут подвешиваться в гальванической ванне, перед тем, как окунуть их в раствор поташа; затем подержите их за проволоку под проточной водой в течение десяти минут, чтобы полностью удалить все следы поташа.
Аппарат для гальваники
Для покрытия медью приготовьте следующий раствор: 4 унции. сульфат меди, растворенный в 12 унциях. воды; добавить крепкий раствор аммиака до тех пор, пока не перестанут выпадать зеленые кристаллы.
Затем добавьте еще аммиака и перемешивайте до тех пор, пока зеленые кристаллы снова не растворятся, давая насыщенный синий раствор.
Медленно добавляйте крепкий раствор цианида калия до исчезновения синего цвета, оставляя прозрачный раствор; снова добавьте цианид калия, примерно в четверть от объема, используемого в процессе обесцвечивания.
Затем доведите раствор до 2 кварт. с водой. При электрическом давлении от 3,5 до 4 вольт это обеспечит равномерное нанесение меди на покрываемом изделии.
Раствор для серебряного покрытия можно приготовить следующим образом:
Растворить 3/4 унции. товарного нитрата серебра в 8 унциях. воды и медленно добавляйте крепкий раствор цианида калия, пока не перестанет выпадать белый осадок.
Затем жидкость слить и тщательно промыть осадок.
Для этого лучше всего наполнить бутылку водой, встряхнуть, дать осадку осесть, а затем слить воду.
Повторить шесть раз.
Закончив промывку осадка, медленно добавить к нему раствор цианида калия до полного растворения осадка.
Затем добавьте избыток цианида калия — примерно столько, сколько было использовано для растворения осадка, — и доведите раствор до 1 кварты. с водой.
Этот раствор при электрическом давлении от 2 до 4 вольт даст хороший белый серебряный слой за двадцать минут — полчаса; используйте 2 вольта для больших предметов и 4 вольта для очень маленьких.
Если требуется больше раствора, необходимо только удвоить все заданные количества.
Перед нанесением серебряного покрытия такие металлы, как железо, свинец, олово, цинк, должны быть покрыты медью в описанной щелочной медной ванне, а затем обработаны как медь.
На латунь, медь, немецкое серебро, никель и другие подобные металлы серебро можно наносить напрямую.
Серебро будет тусклым, и его необходимо отполировать.
Лучше всего использовать вращающуюся щетку для царапин; если у вас нет полировальной машины, подойдет ручная щетка для царапин.
Делайте быстрые легкие движения.
Окончательно отполируйте изделия обычным порошком для пластин.
На эскизе показано, как подвешивать изделия в гальванической ванне. Если используются аккумуляторы, что рекомендуется, обязательно подключите положительную (или красную) клемму к серебряному предмету, висящему в ванне, а отрицательную (или черную) клемму — к покрываемому изделию.
Там, где используются элементы Бунзена, угольный вывод заменяет положительный вывод аккумулятора.
Как золочение делаются, шаг за шагом
Выберите страну / регион *Выберите страну / regionUnited StatesCanadaAfghanistanAlbaniaAlgeriaAmerican SamoaAndorraAngolaAnguillaAntarcticaAntigua и BarbudaArgentinaArmeniaArubaAustraliaAustriaAzerbaijanBahamasBahrainBangladeshBarbadosBelarusBelgiumBelizeBeninBermudaBhutanBoliviaBosnia и HerzegovinaBotswanaBouvet IslandBrazilBritish Индийского океан TerritoryBrunei DarussalamBulgariaBurkina FasoBurundiCambodiaCameroonCape VerdeCayman IslandsCentral африканского RepublicChadChileChinaChristmas IslandCocos (Килинг) IslandsColombiaComorosCongoCongo, Демократический Республика Острова КукаКоста-РикаКот-д’ИвуарХорватияКубаКипрЧешская РеспубликаДанияДжибутиДоминикаДоминиканская РеспубликаВосточный ТиморЭквадорЭгипетЭль-СальвадорЭкваториальная ГвинеяЭритреяЭстонияЭфиопияФолклендские острова (Мальвинские острова) Франция Югославия ГвинеяФранция, Франция, Франция, Мордия, Франция ermanyGhanaGibraltarGreeceGreenlandGrenadaGuadeloupeGuamGuatemalaGuineaGuinea-BissauGuyanaHaitiHeard и McDonald IslandsHoly Престол (Ватикан) HondurasHong KongHungaryIcelandIndiaIndonesiaIran (Исламская Республика) IraqIrelandIsraelItalyJamaicaJapanJordanKazakstanKenyaKiribatiKorea, Корейские Народно-Демократической RepKorea, Республика ofKuwaitKyrgyzstanLao Народный Демократической RepLatviaLebanonLesothoLiberiaLibyan Arab JamahiriyaLiechtensteinLithuaniaLuxembourgMacauMadagascarMalawiMalaysiaMaldivesMaliMaltaMarshall IslandsMartiniqueMauritaniaMauritiusMayotteMexicoMicronesia, Федеративные StatesMoldova, Республика ofMonacoMongoliaMontserratMoroccoMozambiqueMyanmarNamibiaNauruNepalNetherlandsNetherlands AntillesNew CaledoniaNew ZealandNicaraguaNigerNigeriaNiueNorfolk IslandNorthern Mariana IslandsNorwayOmanPakistanPalauPanamaPapua Нового GuineaParaguayPeruPhilippinesPitcairnPolandPortugalPuerto RicoQatarReunionRomaniaRussian FederationRwandaSaint HelenaSaint Китс и НевисСент-ЛюсияСент-Пьер и Мике lonSamoaSan MarinoSao Томе и PrincipeSaudi ArabiaSenegalSeychellesSierra LeoneSingaporeSlovakiaSloveniaSolomon IslandsSomaliaSouth AfricaSpainSri LankaSth Georgia & Sth Sandwich Институт социальных Винсент и GrenadinesSudanSurinameSvalbard и Ян MayenSwazilandSwedenSwitzerlandSyrian Arab RepublicTaiwan, провинция ChinaTajikistanTanzania, Объединенная Республика ofThailandTogoTokelauTongaTrinidad и TobagoTunisiaTurkeyTurkmenistanTurks и Кайкос IslandsTuvaluUgandaUkraineUnited Арабские EmiratesUnited KingdomUruguayUS Малые отдаленные IslandsUzbekistanVanuatuVenezuelaVietnamVirgin острова (Британские) Виргинские острова ( U.S.) Острова Уоллис и ФутунаЗападная СахараЙеменЮгославияЗамбияЗимбабве
Гальваника Easy DIY Никель Медь Цинк
Никель
Электро
покрытие
это несложно, вам нужен контейнер, какой-то тип небольшого зарядного устройства это старый телефон если вы не можете найти источник питания, на выход будет меньше одного ампера, пара батареек будет работать уксус, просто старая соль из белого уксуса, как вы посыпаете стейк, и кусок любого металла, которым вы хотите покрыть пластину, начните сникель
, но где мне взятьникель
с ebay поищитеникель
анод добавьте уксус в контейнер, вы можете смешатьоколо столовой ложки соли, теперь я собираюсь сделать это через секунду, чтобы я мог показать текущий раньше и после посола сделайте
никель
на две части изникеля
подвесьте каждую часть над краем контейнера, подключите источник питания к каждой частиникель
положительный к одному элементу отрицательный к другому, вот и все, теперь вы делаетеникель
электролит это действительнолегкий
пит а что насчет соли единственная причина, по которой мы добавляем соль, — это увеличить проводимость жидкости смотреть на мультиметр поскольку ядобавляю соль, если вы не знаете полярность вашего источника питания, но сторона со всеми выходящими пузырьками будет отрицательной, вам нужно знать, что позже, когда раствор станет зеленым, вы успешно сделали
никель
электролит, который должен занять около двух часов в зависимости от источника питания, при условии, что вы его не сломаете, вам нужно только приготовить раствор, когда он прослужит вечно в герметичном контейнере. А как насчет других металлов, давайте попробуеммедь
то же самое дайте ему поработать, покараствор не станет синим, а как насчет раковины, я понятия не имею, давайте выясним, извините, гигантские аноды
цинк
у меня уже были они и извините коробку для завтрака У меня закончилась банка sцинк
не заставляет раствор менять цвет, просто оставьте питание на пару часов и предположите, что он работает, пока три электролита варятся, давайте подготовим несколько тестовых образцов, чтобы получить успешную пластину, ваши детали должны быть безупречно чистыми и обезжирены, если вы имеете дело с ржавыми частями, вам придется пройти через весь процесс, чтобы вернуть их к хорошему чистому металлу, но для этих маленьких тестовых образцов подойдет капля чистки, если на части будут капли воды он не будет обклеивать вашу деталь сейчас подключите вашу деталь к какой-то медной проволоке
теперь эта следующая деталь является необязательной Я всегда окунаю свои детали в соляную кислоту непосредственно перед нанесением покрытия это протравит деталь и будет действовать как окончательная очистка это просто соляная кислота из хозяйственного магазина смешать около 50 50 воды и кислоту в контейнере для натурального йогуртав смеси 50 50 я оставляю свои части примерно на одну минуту хорошо, электролиты должны быть готовы, и мы все готовы к работе давайте получим покрытие
вот как должен выглядеть ваш электролитникель
через час или два заваривания он должен быть определенно зеленым, как вкусный водянистый гатор, он станет более концентрированным, когда вы его используете, так что не беспокойтесь слишком о нем как зеленый это выглядит для начала приготовьте немного воды из-под крана это просто для смывания кислоты с деталей, чтобы выне испортили электролит, повесьте один из кусочков никеля
над контейнером часть в электролит как можно дальше от анода подключите отрицательный к вашей части подключите положительный кникелевый анод
и включите питание, вы должны увидеть пузыри на части поздравляем, выэлектро
покрытие
если вы просто возиться сгальваническим покрытием
для удовольствия около 20 минут следует сделать это, убедитесь, что вы поворачиваете деталь пару раз во время процесса, так что, чтобы она покрывала равномерно, если вы планируете При использовании деталей для всего, что вы, вероятно, захотите увеличить время покрытия
примерно до 45 минут и еще больше увеличить для первых нескольких пластин, пока раствор не повысит концентрацию сейчасмедь
обратите внимание, приятный синий цвет не Science amazing не будет наносить пластину непосредственно на сталь, но она будет накладываться на никель, поэтому любая сталь должна быть сначала покрыта никелем, а оттуда это точно такой же процесс, что и для никеля ицинка
, я нена самом деле знает, сработает это или нет, давайте выясним, хорошо ли он пузырится, поэтому, если в электролите будет
цинк
, это будет покрытие, вы можете увидеть, что он становится тускло-серым, этоцинк
, так что да, нет проблем, ладно я думаю, что все готово, давайте проверим результаты первый квадрат — это стальной элемент управления без покрытия, а вот деталь с никелевым покрытием, если вы что-то не запихиваетеникель
всегда отключается ну хорошо, вы будете счастливы, и для справки вот ключ патрона, который я сделал и, покрытый тем же никелем
, следующийцинк
цинк
тоже получился прекрасным, тускло-серый — это то, что вы собираетесь получить без использования отбеливателей, тусклая сторона покрыта металлическим покрытием Я быстро отполировал другую сторону вручную с помощью некоторого количества автозоля и, наконец, медь это немного грязно, медь, которую я использовал, это всего лишь лист меди из хобби хранить не обязательно в чистом виде, но это оказалось нормально, однако я, очевидно, не накрывал его достаточно долго, потому что я почти отполировалмедь
нас другой стороны, но вы поняли, что все, я не показал вам Окончательная установка покрытия
Цель этого видео — просто показать, что нет никаких препятствий для того, чтобы попробовать это на себе, поэтому попробуйте, это весело, и вы рискуете испортить немного уксусаИсточник: Джеффри Croker
Гальваника 101 — Как покрыть толстое розовое золото Страница 1 из 0
Нельзя отрицать, что за последние несколько лет розовое золото стало огромной эстетической тенденцией.Вы видите это повсюду, от телефонов до всех видов украшений, и теперь вы можете сделать это самостоятельно с помощью этого руководства. Хотите узнать, как настроить гальваническую станцию? Прочтите этот пост, который проведет вас через процесс и расскажет, что вам нужно.
Вам может быть интересно, в чем разница между обычным раствором розового золота и раствором розового золота большой толщины. Розовое золото большой толщины придаст любому предмету покрытия более толстое покрытие из розового золота, что сделает его более долговечным по несколько более высокой цене.
Ванна для гальваники
Пора ставить ванну из драгоценных металлов для гальваники! Налейте 1 литр раствора розового золота TWL 5N-4G в стеклянный стакан на 1 литр и бросьте туда магнитную гранулу для перемешивания. Поместите химический стакан на плиту магнитного миксера и нагрейте до 100 ° F, давая ему перемешаться на среднем-медленном режиме в течение 15 минут. Установите изогнутый анод из нержавеющей стали в форме леденца так, чтобы длинный конец находился в стакане. Подключите положительный вывод выпрямителя к аноду и установите напряжение выпрямителя равным 2.0-2,5 (рекомендуется 2 вольта) и время плакирования от 30 секунд до 5 минут. Теперь вы готовы к тарелке!
Покрытие
Теперь, если вы покрываете новый предмет, вы можете перейти к шагу 5, но если вы покрываете старую деталь или выполняете ремонт, вы должны выполнить все 13 шагов. Примечание: когда мы говорим об использованной дистиллированной воде, это потому, что дистиллированная вода не содержит герметиков и обеспечивает сушку без пятен.
- Отполируйте изделие. Обязательно удалите лак с изделия как можно скорее после нанесения.Если у вас есть ультразвуковой очиститель, мы рекомендуем использовать его с ювелирным раствором, чтобы полироль не затвердел на кольце. Это поможет раствору для покрытия более прочно закрепиться, поскольку он устранит все загрязнения.
- Отрежьте кусок медного провода диаметром 4 дюйма. Сделайте петлю, чтобы удерживать элемент и подсоединить его к отрицательному проводу выпрямителя.
- Промойте в дистиллированной воде.
- Электроочистка в течение 1 минуты при 125 ° F, 5 В.
- Промыть дистиллированной водой Визуально проверить наличие полировального масла.При необходимости снова выполните электроочистку.
- Поместите в стакан для активации кислоты на 10 секунд.
- Прополоскать дистиллированной водой.
- Гальваническое покрытие из розового золота 5N-4G в течение от 30 секунд до 5 минут при 110 °, 2 В.
- Прополоскать дистиллированной водой.
- Вернитесь к электроочистителю для 10-секундной обработки для стабилизации слоя покрытия из розового золота 5N-4G.
- Прополоскать дистиллированной водой. Совет: горячая дистиллированная вода сохнет быстрее.
- Высушите предмет с небольшим феном или мягкими тканями без лосьона.
- Утилизируйте все химикаты надлежащим образом! Ознакомьтесь с местными законами и постановлениями.
Профессиональный совет: вы можете повторно использовать гальванические растворы и растворы для активации кислоты, но вам следует заменять их еженедельно. Все ополаскиватели дистиллированной водой следует заменять ежедневно.
Если вы хотите ссылаться на видео, посмотрите это!
Есть вопросы? Дайте нам знать ниже
🙂О домашнем никелировании (для восстановления износа)
Как и я, у меня обычно есть более глубокий план. Никель примерно такой же твердости, как сталь.Когда я учился в начальной школе, мой учитель давал классные гроши и пятак с уксусом, водой и поваренной солью.
Он также устойчив к коррозии, но это плюс. Я вижу четкую дорожку износа на нижней стороне задней бабки токарного станка. Я также вижу оригинальные следы обработки на неизношенных участках. Внутренние части клиновидного патрубка 45 °, который проходит над направляющими призмы, подверглись бы аналогичному износу.
Предположим ..
Во-первых, электролитическое «удаление ржавчины» в чем-то щелочном (карбонат натрия), известном также как стиральная сода, с использованием угольного электрода, который является самоограничивающимся.Он не грызет металл и не делает его подверженным появлению свежей ржавчины в тот момент, когда микроструктура высокой площади видит воздух. Он заботится обо всех порах. Это касается только неокрашенных, немаскированных участков. Я бы использовал воск, краску или другой резист.
Затем нанесите никелированное покрытие, достаточно толстое, чтобы выдержать износ, примерно от 0,0015 до 0,002 дюйма. Это покрытие также образует поверхности изношенного клина. Толщина покрытия может быть очень точно рассчитана по току x времени x весу осажденных ионов, но достаточно легко, чтобы просто измерять через определенные промежутки времени.
Тогда отрежьте. Притирайте его к плоской поверхности. Ровно протяните опилку, но удаляйте никель до тех пор, пока следы обработки снова не будут видны на неизношенных участках. Как вариант, возьмите 1/10 микрометра или, в моем случае, 0,001 мм и продолжайте проверять уменьшение притирки.
То, что происходит с V-образным вырезом, измеряется при помощи вделанного в него заземляющего дюбеля. Если связь с неизношенными поверхностями известна, а она известна, то использование дюбеля правильного размера, подходящего для вписанного круга, позволяет разместить все это на пластине для измерения.Мы должны иметь возможность оттереть или иным образом скорректировать покрытие в V-образном вырезе, но оно уже должно быть близко к коррекции для плоскости. В случае необходимости особой регулировки не требуется.
Придуманный план, возможно, просто безумный, но мне трудно сказать, что он не сработает. Если покрытие можно надеть контролируемым образом, и оно будет хорошо держаться, я думаю, это может быть способом восстановить изношенную вещь, как новую!
Хром и никелирование латуни
Латунь — это универсальный бинарный сплав цинка и меди, обладающий множеством преимуществ: он доступен по цене, имеет низкое трение и легко обрабатывается, а также сохраняет хорошую теплопроводность и электрическую проводимость.Вы можете использовать латунь по-разному, но вы также можете улучшить ее общую отделку и свойства с помощью нескольких процессов нанесения покрытия.
КомпанияHard Chrome Specialists, сертифицированная по ISO, предлагает внутренние услуги в короткие сроки. Мы добиваемся качественных результатов, анализируя ваши требования и формируя оптимальные решения.
Можно ли хромировать латунь?
Это может показаться неортодоксальным, но ответ на поставленный выше вопрос — твердое «да».«
Мы начнем работу с тщательной очистки поверхности компонентов растворителем от грязи, мусора и других видов грязи. Мы также можем отполировать предмет полировальной подушечкой, чтобы обеспечить чистую поверхность без дефектов, которые будут отражать хром. Затем мы погрузим его в хромовую ванну, сначала без напряжения, чтобы обеспечить нагрев и травление.
Подается электричество, и мы тщательно отрегулируем напряжение в соответствии со стандартными процедурами гальваники.Мы отшлифуем финишную постобработку, чтобы исключить неровные наросты.
Преимущества хромирования латуни
Хромирование латуни увеличивает естественную долговечность этого ковкого сплава, придавая ему устойчивость к ударам и коррозии, а также блестящую и эстетичную поверхность. Хромированные покрытия имеют сниженный риск расслоения, а это означает, что вы можете рассчитывать на то, что покрытие прослужит долго. Хромирование также может равномерно покрывать поверхности неправильной формы, что обеспечивает лучшие результаты.
Каковы общие области применения хромирования латуни?
Вы часто будете видеть твердое хромирование на латуни, когда люди используют ее в декоративных целях — например, для вытяжек шкафов и смесителей для раковины — из-за привлекательного блеска хрома. Однако вы также увидите это на сантехнических материалах и оборудовании, таком как трубы и фитинги. Музыкальные инструменты также являются возможными кандидатами.
Можно ли никелировать латунь?
В отличие от хромирования, при котором в качестве драйвера используется электричество, при никелировании используется химическое восстановление.Мы погружаем изделие в водный раствор, содержащий агент, который снижает количество ионов никеля и способствует отложению.
В целом, он дает более гладкое покрытие по сравнению с гальваническим покрытием. Используя этот метод, мы также можем легко контролировать уровень толщины наносимого слоя, что дает вам точный результат, который вы предпочитаете.
Преимущества никелированной латуни
Если вам нужна превосходная коррозионная стойкость, вам необходимо нанесение покрытия на латунь химическим никелированием.В результате получается менее пористый, полностью охватывающий барьер, что означает меньший риск проникновения факторов окружающей среды. Вы также получите низкий коэффициент трения.
Каковы общие области применения химического никелирования латуни?
Вы часто будете видеть никелирование, используемое на латунных пулях, так как многие пользователи предпочитают уникальный внешний вид, улучшенную коррозионную стойкость и более быструю перезарядку. В отличие от стандартных латунных гильз, гильзы из никелированной латуни не потускнеют при многократном обращении.Другие области применения включают предметы, которые подвергаются повышенной нагрузке на окружающую среду и часто используются, например, автомобильные детали, шестерни, радиаторы, винты, кожухи аккумуляторных батарей и многое другое.
Чтобы узнать больше о покрытии латуни, заполните нашу контактную форму или позвоните нам по телефону 717-764-5171, чтобы запросить смету.
.